Pytanie 1
Obrazowanie portalowe w radioterapii służy do
Wynik: 30/40 punktów (75,0%)
Wymagane minimum: 20 punktów (50%)
Obrazowanie portalowe w radioterapii służy do
Która sekwencja obrazowania MR wykorzystuje impulsy RF o częstotliwości rezonansowej tłuszczu do tłumienia sygnału pochodzącego z tkanki tłuszczowej?
Który system informatyczny służy do archiwizacji i transmisji obrazów radiologicznych?
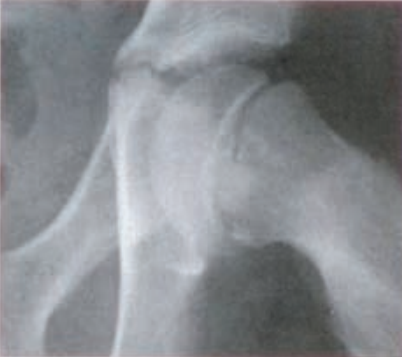
Na rentgenogramie przedstawione jest złamanie Saltera-Harrisa typu
Do wykonania stomatologicznego zdjęcia rentgenowskiego techniką kąta prostego promień centralny należy ustawić prostopadle do
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem
Podczas badania EEG otwarcie oczu powoduje
Które obszary napromieniowania powinien określić lekarz radioterapeuta u pacjenta z nowotworem stercza po wcześniejszej prostatektomii?
Rytm alfa i beta rejestruje się podczas badania
Ile razy i jak zmieni się wartość natężenia promieniowania X przy zwiększeniu odległości OF ze 100 cm do 200 cm?
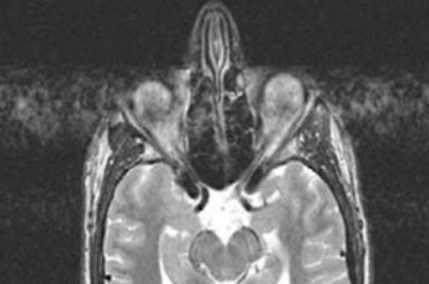
Co jest przyczyną artefaktu widocznego na obrazie MR?
„Ognisko zimne” w obrazie scyntygraficznym określa się jako
Do planowego badania TK klatki piersiowej z użyciem środka cieniującego pacjent powinien zgłosić się
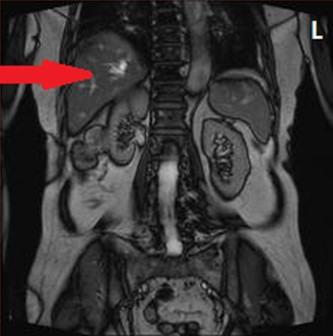
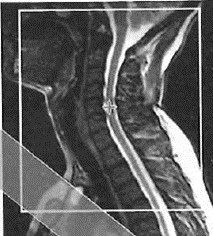
Na obrazie MR jamy brzusznej strzałką wskazano
W standardowym badaniu EEG elektrody P3, P4 i Pz umieszcza się na skórze głowy pacjenta nad płatami
W których projekcjach podstawowych wykonuje się standardowe badanie mammograficzne?
Wskaż przyczynę powstania artefaktu widocznego na obrazie MR.
Testy podstawowe z zakresu geometrii pola rentgenowskiego, przeznaczone do sprawdzenia zgodności pola wiązki promieniowania rentgenowskiego z symulacją świetlną, są wykonywane raz
W technice napromieniania SSD mierzona jest odległość źródła promieniowania od
Źródłem promieniowania protonowego stosowanego w radioterapii jest
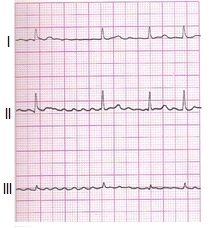
Zamieszczone badanie elektrokardiograficzne wykazało u pacjenta
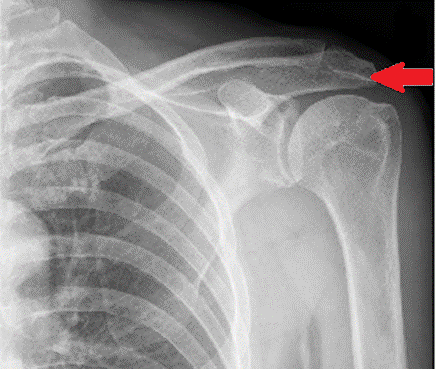
Na radiogramie stawu barkowego strzałką wskazano
Dobierz dla standardowego pacjenta projekcję, pozycję i sposób ułożenia kasety o wymiarach 30 cm x 40 cm do zdjęcia przeglądowego układu moczowego.
| Projekcja | Pozycja | Ułożenie kasety | |||
|---|---|---|---|---|---|
| 1. | AP | 3. | stojąca | 5. | poprzeczne |
| 2. | PA | 4. | leżąca | 6. | podłużne |
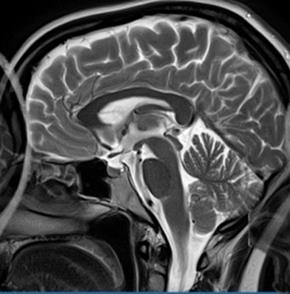
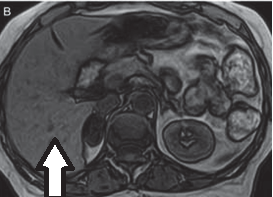
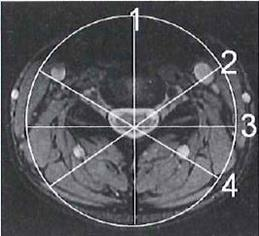
Na przekroju poprzecznym rezonansu magnetycznego strzałką oznaczono
Rumień skóry pojawiający się podczas radioterapii jest objawem
Zdjęcie rentgenowskie nadgarstka w przywiedzeniu dołokciowym jest wykonywane w celu uwidocznienia kości
Jednym z kryteriów poprawnie wykonanego badania spirometrycznego jest czas trwania natężonego wydechu, który powinien wynosić u osób powyżej 10 roku życia co najmniej
Testy specjalistyczne aparatów rentgenowskich do zdjęć wewnątrzustnych są przeprowadzane
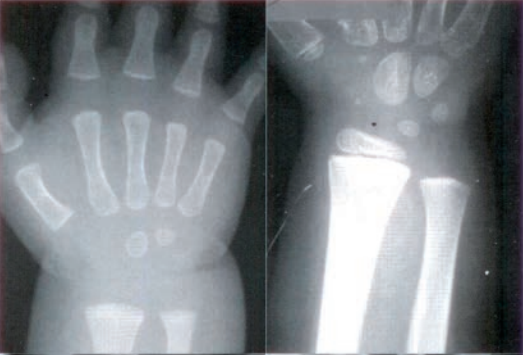
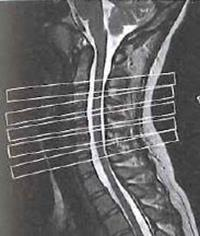
Zestaw rentgenogramów przedstawia
W pozytonowej tomografii emisyjnej PET zostaje zarejestrowane promieniowanie powstające podczas
Wskazaniem do wykonania scyntygrafii perfuzyjnej jest
Na którym obrazie MR jest widoczne pasmo saturacji?

W celu oceny wieku kostnego u dziecka praworęcznego, wykonuje się pojedyncze zdjęcie w projekcji
Na rycinie rentgenogramu w projekcji AP symbolem X oznaczono
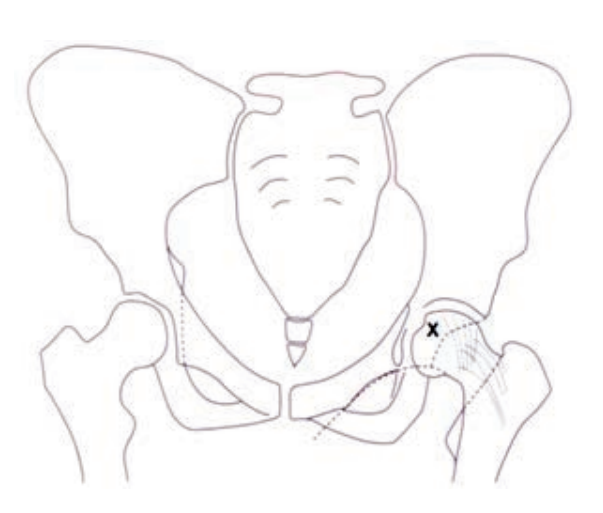
Miejscem wykonania pomiaru densytometrycznego z kości przedramienia jest
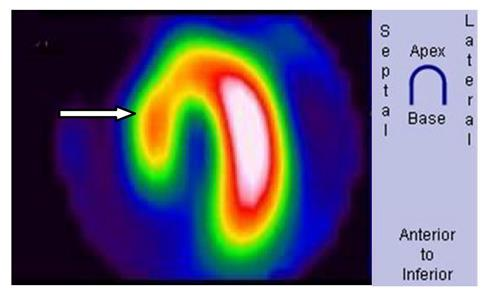
Na obrazie scyntygrafii perfuzyjnej serca strzałką wskazano ścianę
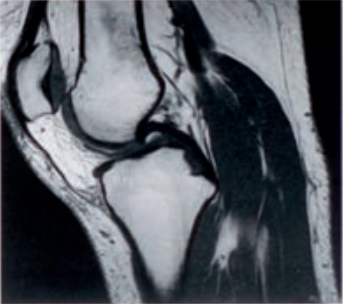
Którą metodę badania zastosowano w obrazowaniu stawu kolanowego?
Który załamek odzwierciedla szybką repolaryzację komór w zapisie EKG?
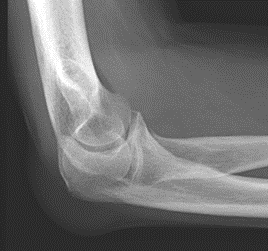
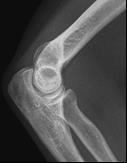
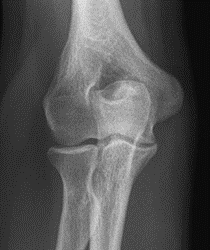
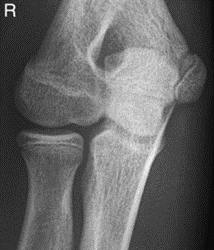
Które zdjęcie RTG stawu łokciowego zostało wykonane w projekcji skośnej w rotacji zewnętrznej?
Na jakim etapie procesu karcynogenezy dochodzi do inwazji miejscowej nowotworu i tworzenia przerzutów odległych?