Pytanie 1
Metodą, która nie służy do utrwalania próbek wody, jest
Wynik: 23/40 punktów (57,5%)
Wymagane minimum: 20 punktów (50%)
Metodą, która nie służy do utrwalania próbek wody, jest
Zabieg, który wykonuje się podczas pobierania próbki wody do analizy, mający na celu zachowanie jej składu chemicznego w trakcie transportu, określa się mianem
Który z etapów przygotowania próbek do analizy opisano w ramce?
| Proces polegający na usuwaniu wody z zamrożonego materiału na drodze sublimacji lodu, tzn. bezpośredniego jego przejścia w stan pary z pominięciem stanu ciekłego. |
Zgodnie z instrukcją dotyczącą pobierania próbek nawozów (na podstawie normy PN-EN 12579:2001), liczbę punktów pobierania próbek pierwotnych ustala się według wzoru nsp = 0,5·√V, gdzie V oznacza objętość jednostki badanej w m3. Wartość nsp zaokrągla się do liczby całkowitej, a dodatkowo nie może być mniejsza niż 12 ani większa niż 30.
Dlatego dla objętości V = 4900 m3, nsp wynosi
Wskaż metodę rozdzielenia układu, w którym fazą rozproszoną jest ciało stałe, a fazą rozpraszającą gaz.
| faza rozproszona | faza rozpraszająca | ||
|---|---|---|---|
| gaz | ciecz | ciało stałe | |
| gaz | - | piana | piana stała |
| ciecz | aerozol ciekły | emulsja | emulsja stała |
| ciało stałe | aerozol stały | zol | zol stały |
Aby oddzielić mieszankę etanolu i wody, konieczne jest przeprowadzenie procesu
Przedstawiony na rysunku zagłębnik stosuje się do pobierania próbek
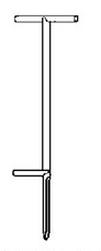
Na rysunku pokazano przyrząd do poboru próbek
Procedura przygotowania roztworu Zimmermana-Reinharda
70 g MnSO4·10H2O rozpuścić w 500 cm3 wody destylowanej, dodając ostrożnie 125 cm3 stężonego H2SO4 i 125 cm3 85% H3PO4, ciągle mieszając. Uzupełnić wodą destylowaną do objętości 1dm3.
Który zestaw ilości odczynników jest niezbędny do otrzymania 0,5 dm3 roztworu Zimmermana-Reinharda, zgodnie z podaną procedurą?
| MnSO4·10H2O [g] | Stężony H2SO4 [cm3] | 85% H3PO4 [cm3] | Woda destylowana [cm3] | |
|---|---|---|---|---|
| A. | 35 g | 62,5 cm3 | 62,5 cm3 | ok. 370 cm3 |
| B. | 35 g | 62,5 cm3 | 62,5 cm3 | ok. 420 cm3 |
| C. | 70 g | 125 cm3 | 125 cm3 | ok. 500 cm3 |
| D. | 70 g | 125 cm3 | 125 cm3 | ok. 800 cm3 |
Próbka wzorcowa to próbka
Po zmieszaniu wszystkie pierwotne próbki danej partii materiału tworzą próbkę
W procesie oddzielania osadu od roztworu, po przeniesieniu osadu na sączek, najpierw należy go
Jakie urządzenie wykorzystuje się do pobierania próbek gazów?
Który sposób przechowywania próbek żywności jest niezgodny z Rozporządzeniem Ministra Zdrowia?
| Fragment Rozporządzenia Ministra Zdrowia w sprawie pobierania i przechowywania próbek żywności przez zakłady żywienia zbiorowego typu zamkniętego |
| (...) Zakład przechowuje próbki, przez co najmniej 3 dni, licząc od chwili, kiedy cała partia została spożyta w miejscu wyłącznym właściwym do tego celu oraz w warunkach zapewniających utrzymanie temperatury +4°C lub niższej, w zależności od przechowywanego produktu. Miejsce przechowywania próbek musi być tak zabezpieczone, aby dostęp do niego posiadał tylko kierujący zakładem lub osoba przez niego upoważniona. |
Na podstawie zamieszczonych w tabeli opisów metod rozdzielania mieszanin, dobierz odpowiadające im nazwy.
| Tabela. Metody rozdzielania mieszanin | |
|---|---|
| Lp. | Opis metody |
| I. | Zlewanie cieczy znad osadu. |
| II. | Przeprowadzenie ciekłego rozpuszczalnika w stan pary. |
| III. | Wyodrębnianie z mieszaniny ciał stałych lub cieczy składnika przy pomocy rozpuszczalnika tak dobranego, aby rozpuszczał żądany związek chemiczny. |
| IV. | Powolne opadanie cząstek substancji stałej w cieczy pod wpływem własnego ciężaru. |
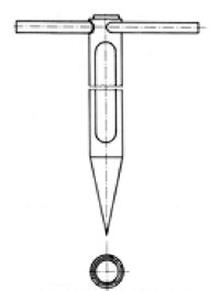
Na rysunku przedstawiono urządzenie służące do poboru próbek

Próbka pobrana z próbki ogólnej, która odzwierciedla cechy partii produktu, określa się jako próbka
Aby rozpuścić próbkę tłuszczu o wadze 5 g, wykorzystuje się 50 cm3 mieszanki 96% alkoholu etylowego oraz eteru dietylowego, połączonych w proporcji objętościowej 1 : 2. Jakie ilości cm3 każdego ze składników są potrzebne do przygotowania 150 cm3 tej mieszanki?
Na podstawie informacji zawartych w tabeli określ, który parametr spośród podanych należy oznaczyć w pierwszej kolejności.
| Tabela. Sposoby utrwalania próbek wody i ścieków, miejsce analizy, dopuszczalny czas przechowywania próbek | ||||
|---|---|---|---|---|
| Oznaczany parametr | Rodzaj naczynia do przechowywania próbki | Sposób utrwalania próbki | Miejsce wykonania analizy | Dopuszczalny czas przechowywania próbki |
| Chlorki | szklane lub polietylenowe | - | laboratorium | 96 godzin |
| Chlor pozostały | szklane | - | w miejscu pobrania próbki | - |
| ChZT | szklane | zakwaszenie do pH<2, schłodzenie do temperatury 2-5°C | laboratorium | 24 godziny |
| Kwasowość | szklane lub polietylenowe | schłodzenie do temperatury 2-5°C | laboratorium | 4 godziny |
| Mangan | szklane lub polietylenowe | zakwaszenie do pH<2, schłodzenie do temperatury 2-5°C | laboratorium | 48 godziny |
Aby wykonać czynności analityczne wskazane w ramce, należy użyć:
| Otrzymaną do badań próbkę badanego roztworu rozcieńczyć wodą destylowaną w kolbie miarowej o pojemności 100 cm3 do kreski i dokładnie wymieszać. Następnie przenieść pipetą 10 cm3 tego roztworu do kolby stożkowej, dodać ok. 50 cm3 wody destylowanej. |
Próbki wody, które mają być badane pod kątem zawartości krzemu, powinny być przechowywane w pojemnikach
Podczas pobierania skoncentrowanego roztworu kwasu solnego konieczne jest pracowanie w włączonym dygestorium oraz zastosowanie
Jak definiuje się próbkę wzorcową?
Aspirator jest urządzeniem wykorzystywanym do pobierania próbek
Na podstawie danych w tabeli określ, jaką masę próbki należy pobrać, jeżeli wielkość ziarna wynosi 1·10-5 m.
| Wielkość ziaren lub kawałków [mm] | Poniżej 1 | 1-10 | 11-50 | Ponad 50 |
|---|---|---|---|---|
| Pierwotna próbka (minimum) [g] | 100 | 200 | 1000 | 2500 |
W celu uzyskania 500 g mieszaniny oziębiającej o temperaturze -18oC należy zmieszać
| Tabela. Mieszaniny oziębiające | ||
|---|---|---|
| Temperatura mieszaniny [°C] | Skład mieszaniny | Stosunek masowy |
| -2 | Woda + chlorek amonu | 10 : 3 |
| -15 | Woda + rodanek amonu | 10 : 13 |
| -18 | Lód + chlorek amonu | 10 : 3 |
| -21 | Lód + chlorek sodu | 3 : 1 |
| -22 | Lód + chlorek amonu + azotan(V) amonu | 25 : 5 : 11 |
| -25 | Lód + azotan(V) amonu | 1 : 1 |
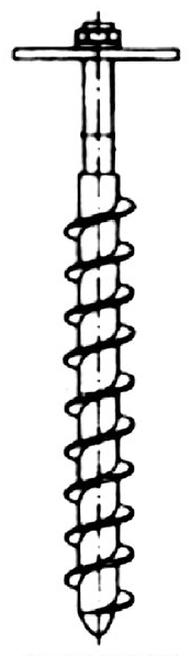
Zgłębniki o konstrukcji przypominającej świder są wykorzystywane do pobierania próbek różnych materiałów
Dekantacja to metoda
Jaką próbkę stanowi woreczek gleby pobranej zgodnie z instrukcją?
| Instrukcja pobierania próbek glebowych | |
| Próbki pierwotne pobiera się laską glebową z wierzchniej warstwy gleby 0-20 cm, kolejno wykonując czynności: – w miejscu pobierania próbki pierwotnej (pojedynczej), rolę świeżo zaoraną przydeptać, – pionowo ustawić laskę do powierzchni gleby, – wcisnąć laskę do oporu (na wysokość poprzeczki ograniczającej), – wykonać pełny obrót i wyjąć laskę, – zawartość wgłębienia (zasobnika) przenieść do pojemnika skrobaczki. Po pobraniu próbek pojedynczych, całość wymieszać i napełnić kartonik lub woreczek. | |
Do rozpuszczania próbek wykorzystuje się wodę królewską, która stanowi mieszaninę stężonych kwasów
Próbki pobrano z materiału o objętości \( 100 \, \text{m}^3 \), wysypanego z opakowania. Liczba miejsc poboru próbek pierwotnych z tego materiału wynosi:
$$ n = 0{,}5 \cdot \sqrt{V} $$ gdzie:
\( V \) – objętość jednostki badanej w \( \text{m}^3 \)
\( n \) – liczba miejsc poboru próbek
Na rysunku przedstawiono urządzenie stosowane do pobierania próbek
Na podstawie informacji zawartych w tabeli wskaż mieszaninę oziębiającą o temperaturze -21 °C.
| Temperatura mieszaniny | Skład mieszaniny | Stosunek masowy |
| -15 °C | lód + octan sodu | 10:9 |
| -18 °C | lód + chlorek amonu | 10:3 |
| -21 °C | lód + chlorek sodu | 3:1 |
| -25 °C | lód + azotan amonu | 1:9 |
Na podstawie danych zawartych w tabeli określ, do oznaczania którego parametru próbka musi być utrwalona w niskim pH.
| Oznaczany parametr | Rodzaj naczynia do przechowywania | Sposób utrwalania | Dopuszczalny czas przechowywania |
|---|---|---|---|
| barwa | szklane lub polietylenowe | - schłodzenie do temperatury 2-5°C | 24 h |
| fosforany ogólne | szklane lub polietylenowe | - zakwaszenie kwasem siarkowym(VI) - schłodzenie do temperatury 2-5°C | 4 h 48 h |
| BZT | szklane | - schłodzenie do temperatury 2-5°C - przechowywanie w ciemności | 24 h |
| azot azotanowy(V) | szklane lub polietylenowe | - schłodzenie do temperatury 2-5°C - dodanie 2 cm3 chloroformu do 1 dm3 próbki | 24 h 48 h |
Jakie czynniki wpływają na zmiany jakościowe w składzie próbki?
Na rysunku przedstawiono przyrząd do pobierania próbek

Jakie metody można zastosować do rozdzielania i koncentracji składników próbki?
Z próbek przygotowuje się ogólną próbkę
Losowo należy pobierać próbki z opakowań
Materiał uzyskany przez zmieszanie prób pobranych w ustalonych odstępach czasu określa się mianem próbki