Pytanie 1
Wskaż, do jakiego typu należą zamieszczone równania reakcji.
| I. 2 Mg + O2 → 2 MgO |
| II. 2 KMnO4 → K2MnO4 + MnO2 + O2 |
| III. BaCl2 + H2SO4→ BaSO4 + 2 HCl |
Wynik: 27/40 punktów (67,5%)
Wymagane minimum: 20 punktów (50%)
Wskaż, do jakiego typu należą zamieszczone równania reakcji.
| I. 2 Mg + O2 → 2 MgO |
| II. 2 KMnO4 → K2MnO4 + MnO2 + O2 |
| III. BaCl2 + H2SO4→ BaSO4 + 2 HCl |
W laboratorium chemicznym przewody instalacji rurowych są oznaczane różnymi kolorami, zgodnie z obowiązującymi normami. Polska Norma PN-70 N-01270/30 określa kolor dla wody jako
Ogólna próbka, jednostkowa lub pierwotna powinna
Sączenie osadów kłaczkowatych odbywa się przy użyciu sączków
Waga przedstawiona na rysunku umożliwia ważenie substancji z dokładnością do

Aby przygotować 0,5 dm3 roztworu HCl o stężeniu 0,2 mol/dm3, jaką kolbę miarową o pojemności należy wykorzystać?
Aby odcedzić galaretowaty osad, konieczne jest użycie sączka
Na rysunku przedstawiono ogrzewanie kolby z cieczą w łaźni
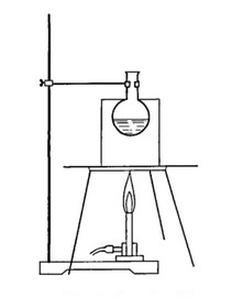
Proces mineralizacji próbki, który polega na jej spopieleniu w piecu muflowym w temperaturze 300-500°C i rozpuszczeniu pozostałych resztek w kwasach w celu oznaczenia zawartości metali ciężkich, to mineralizacja
Proces przesiewania próbki prowadzi się za pomocą urządzenia przedstawionego na rysunku

Woda, która została poddana dwukrotnej destylacji, to woda
Którego związku chemicznego, z uwagi na jego silne właściwości higroskopijne, nie powinno się używać w analizie miareczkowej jako substancji podstawowej?
Zaleca się schładzanie próbek wody transportowanych do laboratorium do temperatury
Ile gramów chlorku baru powinno się rozpuścić w wodzie, aby uzyskać 200 cm3 roztworu o stężeniu 10% i gęstości 1,203 g/cm3?
W trakcie korzystania z odczynnika opisanego na etykiecie, należy szczególnie zwrócić uwagę na zagrożenia związane
Miesięczne zapotrzebowanie laboratorium analitycznego na 2-propanol wynosi 500 cm3. Na jak długo wystarczy ta substancja?
Czego się używa w produkcji z porcelany?
Resztki szkła, osadników czy inne odpady stałe powstałe w laboratorium analitycznym powinny być umieszczone
Wagi laboratoryjne można klasyfikować według nośności oraz precyzji na
Zestaw przedstawiony na rysunku służy do
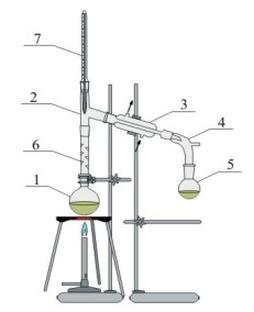
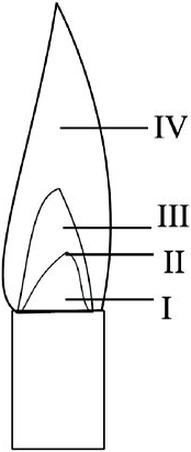
Na rysunku przedstawiającym płomień palnika gazowego najwyższa temperatura płomienia znajduje się w strefie
Gęstość próbki cieczy wyznacza się przy użyciu
Jakie urządzenie służy do pomiaru temperatury topnienia substancji chemicznych?
Odpady z rozpuszczalników organicznych, takich jak benzen czy aceton, zawierające co najmniej 80% danego rozpuszczalnika, należy
Technika oddzielania płynnych mieszanin, w której wykorzystuje się różnice w prędkości migracji składników przez odpowiednią bibułę, nazywa się
Wskaż zbiór substancji, które po rozpuszczeniu w wodzie stają się elektrolitami?
Do 300 g wody o temperaturze 30oC dodano 120 g substancji, co zaowocowało powstaniem roztworu nasyconego. Jaką ma rozpuszczalność ta substancja w temperaturze 30oC?
W trzech probówkach umieszczono roztwory: wodorotlenku sodu, chlorku sodu i kwasu octowego. W celu identyfikacji zbadano ich odczyn za pomocą uniwersalnego papierka wskaźnikowego, a następnie fenoloftaleiny. Barwy wskaźników w badanych roztworach przedstawiono w tabeli:
| Wskaźnik | Barwa wskaźnika | ||
|---|---|---|---|
| próbówka nr 1 | próbówka nr 2 | próbówka nr 3 | |
| uniwersalny papierek wskaźnikowy | żółty | czerwony | niebieski |
| fenoloftaleina | bezbarwny | bezbarwny | malinowa |
Proces oddzielania składników jednorodnej mieszaniny, polegający na eliminacji jednego lub większej ilości składników z roztworu lub substancji stałej przy użyciu odpowiednio wybranego rozpuszczalnika, to
Zgodnie z danymi zawartymi w tabeli wskaźników roztwór obojętny będzie miał barwę
| Wskaźnik | Zakres zmiany barwy (w jednostkach pH) | Barwa w środowisku | |
|---|---|---|---|
| kwaśnym | zasadowym | ||
| błękit tymolowy | 1,2 – 2,8 | czerwona | żółta |
| oranż metylowy | 3,1 – 4,4 | czerwona | żółta |
| czerwień metylowa | 4,8 – 6,0 | czerwona | żółta |
| czerwień chlorofenolowa | 5,2 – 6,8 | żółta | czerwona |
| błękit bromotymolowy | 6,0 – 7,6 | żółta | niebieska |
| czerwień fenolowa | 6,6 – 8,0 | żółta | czerwona |
| błękit tymolowy | 8,0 – 9,6 | żółta | niebieska |
| fenoloftaleina | 8,2 – 10,0 | bezbarwna | czerwona |
| żółcień alizarynowa | 10,1 – 12,0 | żółta | zielona |
Aby oszacować czystość MgCO3, poddano prażeniu próbkę o wadze 5 g tej soli aż do osiągnięcia stałej masy. W trakcie prażenia zachodzi reakcja:
MgCO3 → MgO + CO2 Całkowity ubytek masy wyniósł 2,38 g.
(Masy molowe reagentów to: MgCO3 – 84 g/mol, MgO – 40 g/mol, CO2 – 44 g/mol) Jaką czystość miała próbka węglanu magnezu?
Próbka, którą analizujemy, to bardzo rozcieńczony wodny roztwór soli nieorganicznych, który ma być poddany analizie. Proces, który można zastosować do zagęszczenia tego roztworu, to
Gdzie należy przechowywać cyjanek potasu KCN?
W celu uzyskania czystej substancji próbkę zawierającą nitroanilinę poddano krystalizacji. Oblicz masę odważki nitroaniliny, pobranej do krystalizacji, jeśli uzyskano 1,5 g czystego związku, a wydajność krystalizacji wynosiła 75%.
W trakcie destylacji cieczy wykorzystuje się tzw. kamienie wrzenne, ponieważ
Podczas łączenia bezwodnego etanolu z wodą występuje zjawisko kontrakcji. Gdy zmieszamy 1000 cm3 wody oraz 1000 cm3 etanolu, otrzymujemy roztwór o objętości
Aby pobrać dokładnie 20 cm3 próbkę wody do przeprowadzenia analiz, należy zastosować
Przyrząd przedstawiony na rysunku służy do pobierania próbek substancji
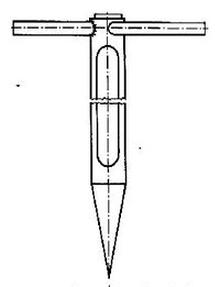
Przedstawiony piktogram powinien być zamieszczony na butelce zawierającej

Zgodnie z zasadami BHP w laboratorium, po zakończeniu pracy z odczynnikami chemicznymi należy: