Pytanie 1
Chorobą układu oddechowego typu obturacyjnego jest
Wynik: 22/40 punktów (55,0%)
Wymagane minimum: 20 punktów (50%)
Chorobą układu oddechowego typu obturacyjnego jest
W systemie międzynarodowym czwarty górny ząb mleczny po stronie prawej oznacza się symbolem
W badaniu cystografii wstępującej środek kontrastowy należy podać
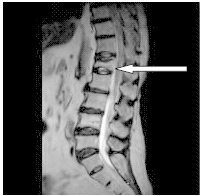
Na obrazie rezonansu magnetycznego strzałką oznaczono patologiczny kręg
Strzykawka automatyczna do podawania kontrastu jest stosowana przy wykonywaniu
Obrazowanie portalowe w radioterapii służy do
Teleterapia polega na napromienowaniu
Zadaniem technika elektroradiologa w pracowni naczyniowej jest
Które ciało obce w obszarze badania nie stanowi przeciwwskazania do wykonania MR?
W technice napromieniania SSD mierzona jest odległość źródła promieniowania od
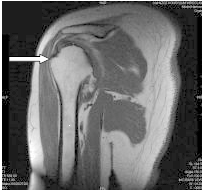
Którą strukturę anatomiczną oznaczono na obrazie rezonansu magnetycznego?
Jak konwencjonalnie frakcjonuje się dawkę w teleradioterapii?
Scyntygrafia kości „whole body” jest wskazana podczas diagnostyki
Jak określa się rekonstrukcję obrazów TK, której wynikiem są obrazy dwuwymiarowe tworzone w dowolnej płaszczyźnie przez wtórną obróbkę zestawionych ze sobą wielu przekrojów poprzecznych?
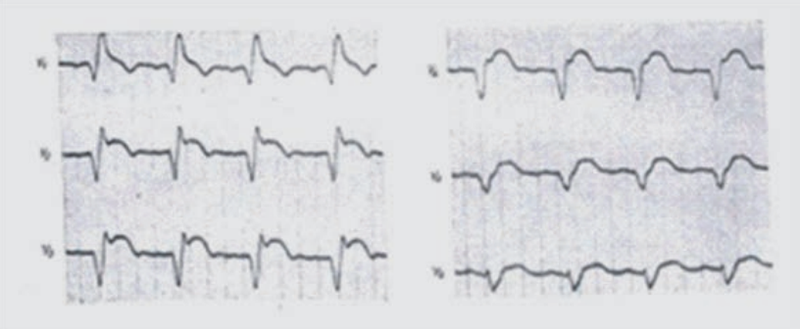
Na elektrokardiogramie zarejestrowano
Parametrem krwi, który powinien zostać oznaczony u pacjenta przed wykonaniem badania MR z kontrastem jest
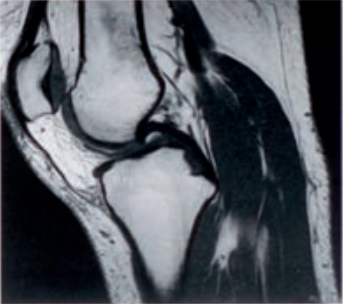
Którą metodę badania zastosowano w obrazowaniu stawu kolanowego?
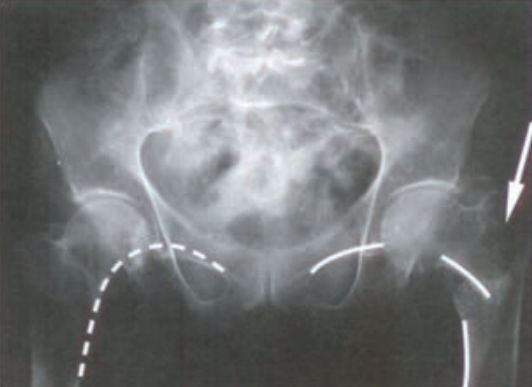
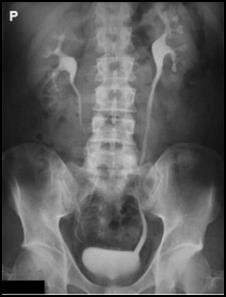
Radiogram przedstawia
Największa wartość energii promieniowania stosowanego w radioterapii jest generowana przy użyciu
Jednym z kryteriów poprawnie wykonanego badania spirometrycznego jest czas trwania natężonego wydechu, który powinien wynosić u osób powyżej 10 roku życia co najmniej
Obiektywną metodą badania słuchu jest audiometria
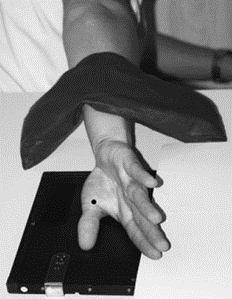
Na ilustracji przedstawiono ułożenie pacjenta do zdjęcia rentgenowskiego
Które urządzenia pomocnicze służą do unieruchomienia pacjenta do zabiegu radioterapii?
Który radioizotop stosuje się do badania scyntygraficznego kości?
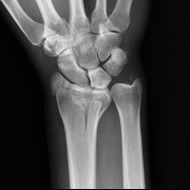
Na obrazie radiologicznym nadgarstka uwidoczniono złamanie nasady
Kolonoskopia to badanie, które ma na celu ocenę błony śluzowej
Jak oznacza się w systemie międzynarodowym czwarty górny ząb mleczny po stronie prawej?
Który radioizotop jest emiterem promieniowania alfa?
W badaniu EEG elektrody referencyjne przymocowane do płatka ucha to
Na radiogramie uwidoczniono
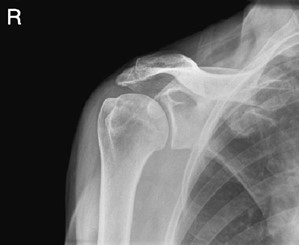
Zamieszczony rentgenogram został zarejestrowany podczas wykonania
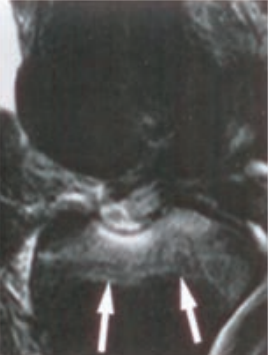
Obraz stawu kolanowego otrzymano metodą
W radiologii stomatologicznej ząb o numerze 23 to kieł
Badanie metodą Dopplera umożliwia
Promieniowanie rentgenowskie jest
Który środek ochrony radiologicznej pacjenta należy zastosować podczas wykonywania zdjęcia bocznego kręgosłupa szyjnego?
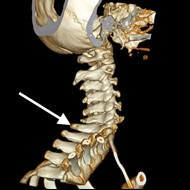
Na obrazie TK kręgosłupa strzałką wskazano wyrostek
Do zadań technika elektroradiologa w pracowni hemodynamicznej należy
Proces chemicznego wywoływania radiogramów polega na
W badaniu MR nadgarstka w ułożeniu na supermana pacjent leży na