Pytanie 1
Na diagramie słupkowym przedstawiono wyniki analizy sitowej surowca w formie proszkowej. W jakiej kolejności zamontowano sita w wytrząsarce, licząc je od naczynia zbierającego?
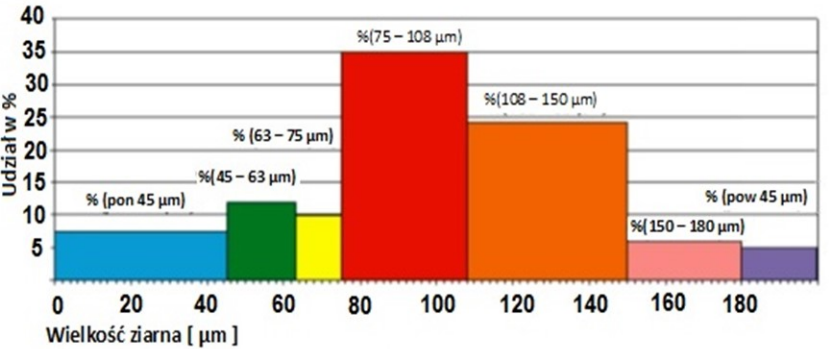
Wynik: 18/40 punktów (45,0%)
Wymagane minimum: 20 punktów (50%)
Na diagramie słupkowym przedstawiono wyniki analizy sitowej surowca w formie proszkowej. W jakiej kolejności zamontowano sita w wytrząsarce, licząc je od naczynia zbierającego?

Określ zawartość amoniaku w analizowanej próbce, jeżeli na jej zmiareczkowanie zużyto 20,0 cm3 roztworu HCl o stężeniu 0,1 mol/dm3.
Dostanie się do środowiska bakterii Salmonella, które były hodowane na pożywkach mikrobiologicznych, może skutkować
Na jakiej pożywce wykonuje się posiew kłuty preparatu mikrobiologicznego?
Ile wynosi mnożnik analityczny żelaza oznaczanego wagowo w postaci Fe2O3?
| MFe = 55,845 g/mol | MFe2O3 = 159,687 g/mol |
W oznaczeniach kompleksonometrycznych dużej grupy kationów metali jako titrant stosowany jest związek chemiczny o ogólnym wzorze Na2H2Y. Przebieg oznaczenia przedstawia schematyczny zapis równania reakcji. Który z jonów metali nie jest oznaczany tą metodą?
| Me(H2O)xn+ + H2Y2- ↔ MeYn-4 + 2H3O+ + (x-2) H2O |
Proces kondensacji i osuszania substancji termolabilnych, takich jak białka oraz kwasy nukleinowe, za pomocą suszenia zamrożonego materiału w obniżonym ciśnieniu poprzez sublimację lodu, określany jest jako
Przy separacji osadu z roztworu za pomocą wirówki laboratoryjnej istotne jest, aby rotor wirówki
Jaką objętość kwasu solnego o stężeniu 0,5 mol/dm3 należy wykorzystać do całkowitego zobojętnienia 100 cm3 roztworu wodorotlenku sodu o stężeniu 0,4 mol/dm3?
Na zamieszczonym wykresie cyfrą 2 oznaczono odchylenie

Oznaczono zawartość cynku w stopie metodą kompleksometryczną. W tym celu odważono 0,50 g stopu i przeprowadzono do roztworu. Próbkę do badań przygotowano w kolbie miarowej o pojemności 250 cm3. Następnie do trzech kolb stożkowych odpipetowano po 50 cm3 roztworu z przygotowanej próbki do badań. Próbki miareczkowano roztworem EDTA o stężeniu 0,01 mmol/cm3. Zużyta średnia objętość roztworu EDTA wyniosła 32,5 cm3. Korzystając z zamieszczonego wzoru, oblicz procentową zawartość cynku w stopie.
| mZn = V · CEDTA · 65,37 · W |
| mZn – masa cynku; mg V – objętość zużytego roztworu EDTA w trakcie miareczkowania; cm3 CEDTA – stężenie molowe roztworu EDTA; mmol/cm3 65,37 – masa molowa cynku; mg/mmol W – współmierność kolby miarowej i pipety; 5 |
Do analizy pobrano próbkę o masie 200 mg. Na podstawie informacji zamieszczonych w tabeli określ, w której skali będzie wykonana ta analiza.
| Wielkość próbki | Skala analizy |
|---|---|
| > 0,1 g | makro |
| 0,01 – 0,1 g | semimikro |
| 0,0001 – 0,01 g | mikro |
| < 10-4 g | ultramikro |
W analizach kompleksometrycznych dużej grupy kationów metali jako titrant wykorzystuje się związek chemiczny o ogólnym wzorze Na2H2Y. Przebieg analizy przedstawiono w formie równania reakcji:
Me(H2O)xn+ + H2Y2- ↔ MeYn-4 + 2H3O+ + (x-2) H2O Który z kationów metali nie jest oznaczany tą techniką?
W mikrobiologicznych badaniach, dezynfekcja ma na celu eliminację
Zamieszczony w ramce opis określa liczbę
| Liczba gramów fluorowca, przeliczona na gramy jodu, który w określonych warunkach ulega reakcji addycji do atomów węgla związanych wiązaniem wielokrotnym, zawartych w 100 g badanego tłuszczu. Jest ona proporcjonalna do liczby wiązań wielokrotnych w tłuszczach. |
Jaką substancję podstawową powinno się użyć do ustalania miana roztworu wodorotlenku sodu?
Proces strącania osadu, który polega na wiązaniu na nim jonów lub cząsteczek, które w roztworze nie wytrąciłyby się samodzielnie, określa się mianem
Przedstawiony na rysunku zestaw jest stosowany podczas oznaczania
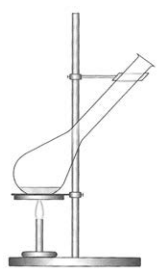
Urządzenie, które umożliwia pomiar gęstości na podstawie masy oraz objętości analizowanej próbki, to
Roztwór, który powstaje z mieszaniny słabego kwasu oraz jego soli z mocną zasadą lub słabej zasady i jej soli z mocnym kwasem, to
W ramce przedstawiono równania reakcji zachodzące podczas pośredniego jodometrycznego oznaczania
| 2Cu2+ + 4I- →2CuI + I2 I2 + S2O32- → 2I- + S4O62- |
Dokładność metody definiowana jest na podstawie ustalonej wartości
Brak odpowiedzi na to pytanie.
Jak określane są enzymy, które katalizują przenoszenie różnych grup funkcyjnych?
Brak odpowiedzi na to pytanie.
Ezy oraz igły stosowane w mikrobiologii należy wyjaławiać
Brak odpowiedzi na to pytanie.
Na schemacie przedstawiono procesy, które zachodzą podczas przygotowania próbek do badań z wykorzystaniem
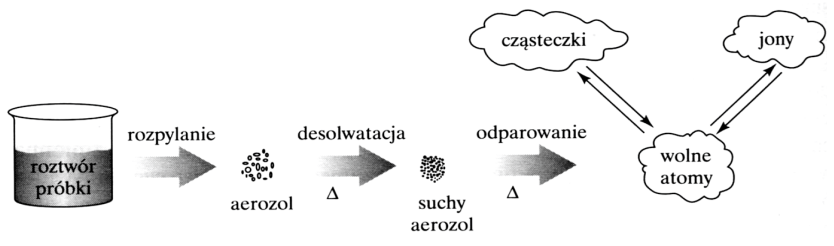
Brak odpowiedzi na to pytanie.
Wartość logarytmu stosunku natężenia wiązki padającej do natężenia wiązki przechodzącej przez badany ośrodek (log I0/I) nazywana jest
Brak odpowiedzi na to pytanie.
Który z poniższych związków chemicznych (w odpowiednio przygotowanej postaci roztworu) stanowi odczynnik grupowy dla kationów IV grupy?
Brak odpowiedzi na to pytanie.
Na podstawie danych zamieszczonych w tabeli określ zależność lepkości cieczy od temperatury.
| Ciecz | Lepkość [Pa×s×10-3] | |||
|---|---|---|---|---|
| 0°C | 10°C | 30°C | 60°C | |
| Aceton | 0,397 | 0,361 | 0,296 | 0,228 |
| Toluen | 0,700 | 0,667 | 0,517 | 0,381 |
| Woda | 1,792 | 1,308 | 0,801 | 0,469 |
Brak odpowiedzi na to pytanie.
Ustalenie wartości miana roztworu wodorotlenku sodu na wodoroftalan potasu jest rekomendowane przez IUPAC, ponieważ wodoroftalan potasu jest substancją
Brak odpowiedzi na to pytanie.
Na podstawie informacji zamieszczonych w tabeli wskaż wzór związku, który wytrąci się w postaci osadu.
| Badany kation | Odczynnik grupowy | NaOH | Barwienie płomienia |
|---|---|---|---|
| Mg2+ | brak | biały osad | |
| K+ | brak | fiołkowy | |
| Na+ | brak | żółty |
Brak odpowiedzi na to pytanie.
Dział analizy objętościowej, który dotyczy reakcji zobojętniania, to
Brak odpowiedzi na to pytanie.
Zjawisko, w którym obce jony są mechanicznie zatrzymywane przez szybko rosnący kryształ, określane jest mianem
Brak odpowiedzi na to pytanie.
Analiza cech ropy naftowej realizowana za pomocą wiskozymetru Englera, polegająca na pomiarze czasu wypływu 200 cm3 ropy naftowej w temperaturze 20°C oraz czasu wypływu tej samej objętości wody destylowanej, dotyczy oceny
Brak odpowiedzi na to pytanie.
Na etykiecie odczynnika chemicznego zawarte są następujące informacje. Z informacji wynika, że odczynnik ten może być zastosowany do sporządzenia roztworu o stężeniu około 0,1 mol/dm3 z dokładnością do
| NH4SCN amonu tiocyjanian | 0,1 mol/l |
| Stężenie po rozcieńczeniu do 1000 ml w 20°C | 0,1 mol/l ± 0,2 % |
Brak odpowiedzi na to pytanie.
Roztwór zawierający aniony I grupy analitycznej poddano identyfikacji metodą chromatografii cienkowarstwowej. Na chromatogramie uwidoczniono dwie plamki w odległości 5,6 cm i 3,5 cm od linii startu. Odległość czoła eluenta od linii startu wyniosła 10,1 cm, a wartości wskaźników Rf wzorców anionów wynoszą jak w tabeli. Które z anionów zawierała badana próbka?
| Anion | Cl- | Br- | I- | SCN- |
|---|---|---|---|---|
| Wskaźnik Rf | 0,243 | 0,352 | 0,554 | 0,648 |
Brak odpowiedzi na to pytanie.
Toksyczność względną zanieczyszczeń opisuje wzór:
Korzystając z danych z tabeli, oblicz toksyczność względną węglowodorów.
| Zanieczyszczenia emitowane do ekosystemu powietrza | NDS [ppm] |
|---|---|
| CO | 40,0 |
| CxHy | 19,3 |
| SO2 | 1,4 |
| NOx | 0,5 |

Brak odpowiedzi na to pytanie.
Metoda obrączkowa jest wykorzystywana do rozpoznawania jonu
Brak odpowiedzi na to pytanie.
W celu oceny jakości masła wykonano oznaczenie liczby kwasowej LK, liczby zmydlania LZ i liczby nadtlenkowej LOO. Wyniki zapisano w tabeli.
Wartość liczby estrowej LE w badanym maśle wynosi
| Liczba | Wartość zmierzona |
|---|---|
| LZ | 196,8 mg KOH/1g |
| LK | 1,2 mg KOH/1g |
| LE | ? |
| LOO | 4,25 milirównoważnika aktywnego tlenu/ kg |
Brak odpowiedzi na to pytanie.
Związek chemiczny, który posiada skrót Gly-Ala-Leu-Ala-Tyr i został zidentyfikowany w trakcie badań analitycznych, to
Brak odpowiedzi na to pytanie.
W tabeli przedstawiono gęstość wodnych roztworów gliceryny w temperaturze 20°C w zależności od jej stężenia wyrażonego w % wagowych.
Z informacji zawartych w tabeli wynika, że stężenie gliceryny o gęstości 1,10 g/cm³ wynosi
| % wagowy gliceryny | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
|---|---|---|---|---|---|---|---|---|---|---|
| [g/cm3] gęstość | 1,022 | 1,047 | 1,072 | 1,099 | 1,126 | 1,153 | 1,180 | 1,208 | 1,235 | 1,261 |
Brak odpowiedzi na to pytanie.