Pytanie 1
Parametrem krwi, który powinien zostać oznaczony u pacjenta przed wykonaniem badania MR z kontrastem, jest
Wynik: 27/40 punktów (67,5%)
Wymagane minimum: 20 punktów (50%)
Parametrem krwi, który powinien zostać oznaczony u pacjenta przed wykonaniem badania MR z kontrastem, jest
Audiometria impedancyjna polega na pomiarze
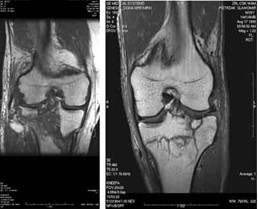
Którą metodą i w której płaszczyźnie zostało wykonane badanie stawu kolanowego zobrazowane na zdjęciach?
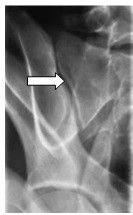
Na radiogramie uwidoczniono złamanie nasady
Jak określa się rekonstrukcję obrazów TK, której wynikiem są obrazy dwuwymiarowe tworzone w dowolnej płaszczyźnie przez wtórną obróbkę zestawionych ze sobą wielu przekrojów poprzecznych?
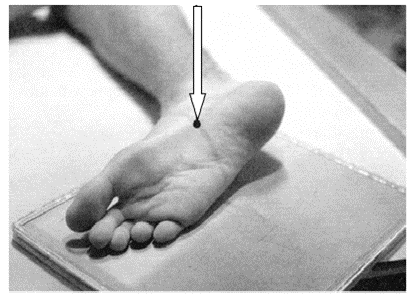
Na zamieszczonej ilustracji przedstawiono ułożenie pacjenta do wykonania zdjęcia rentgenowskiego
Osłony na gonady dla osób dorosłych powinny posiadać równoważnik osłabienia promieniowania nie mniejszy niż
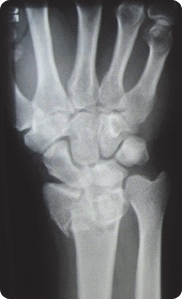
Którą strukturę anatomiczną zaznaczono strzałką na rentgenogramie?
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
W którym okresie ciąży wykonanie u kobiety zdjęcia rentgenowskiego klatki piersiowej jest najbardziej szkodliwe dla płodu?
Zgodnie z obowiązującą procedurą radiologiczną zdjęcie jamy brzusznej przy podejrzeniu zapalenia nerek zostanie wykonane w projekcji
W scyntygrafii dynamiczne badanie najczęściej rozpoczyna się
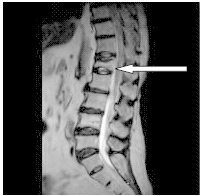
Na obrazie rezonansu magnetycznego strzałką oznaczono patologiczny kręg
W brachyterapii MDR stosowane są dawki promieniowania
W radioterapii konwencjonalnej pacjent jest leczony promieniowaniem pochodzącym
Limfografia to badanie kontrastowe
Które informacje należy zamieścić na strzykawce z radiofarmaceutykiem przygotowanym przez technika elektroradiologa?
Folia wzmacniająca umieszczona w kasecie rentgenowskiej emituje pod wpływem promieniowania X światło
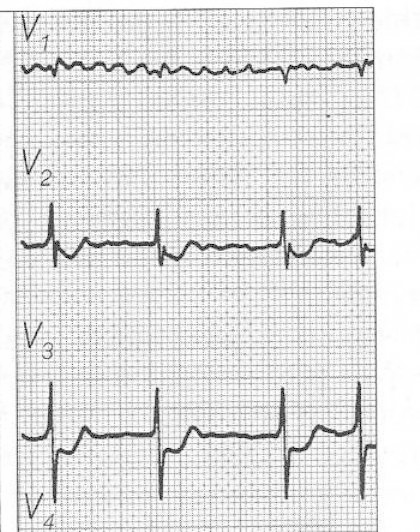
Zamieszczony elektrokardiogram przedstawia
Kto jest odpowiedzialny za wykonywanie testów podstawowych kontroli jakości gammakamery w Zakładzie Medycyny Nuklearnej?
Kolonoskopia to badanie, które ma na celu ocenę błony śluzowej
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Jak zgodnie ze standardem należy ustawić pacjenta do badania rentgenowskiego w skosie tylnym prawym?
Które zdjęcia należy wykonać pacjentom z chorobą reumatoidalną stawów kolanowych?
Zadaniem technika elektroradiologii w pracowni badań naczyniowych jest
Technik elektroradiolog do badania MR kręgosłupa lędźwiowego powinien ułożyć pacjenta:
Zdjęcie rentgenowskie nadgarstka w przywiedzeniu dołokciowym jest wykonywane w celu uwidocznienia kości
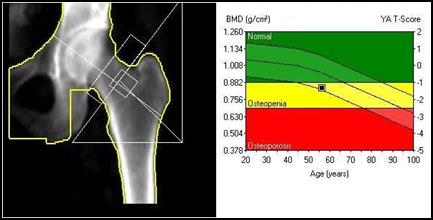
Zamieszczone na ilustracji obrazy dotyczą badania
W radiologii stomatologicznej ząb o numerze 23 to kieł
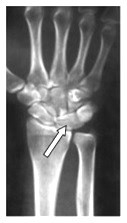
Na obrazie radiologicznym nadgarstka strzałką zaznaczona jest kość
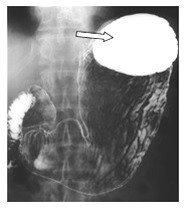
Który element żołądka zaznaczono strzałką na zdjęciu rentgenowskim?
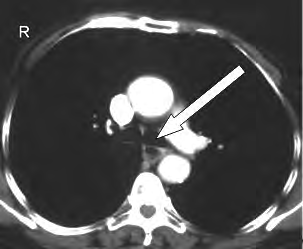
Na obrazie TK klatki piersiowej w przekroju poprzecznym strzałką oznaczono
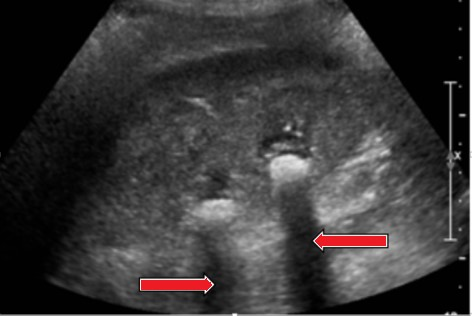
Który artefakt wskazano strzałkami na obrazie USG nerki?
W medycynie nuklearnej wykorzystuje się:
Wskazaniem do wykonania scyntygrafii perfuzyjnej jest
Miejscem wykonania pomiaru densytometrycznego z kości przedramienia jest
Które czynności wykonuje technik elektroradiolog w pracowni „gorącej”?
W systemie międzynarodowym czwarty górny ząb mleczny po stronie prawej oznacza się symbolem
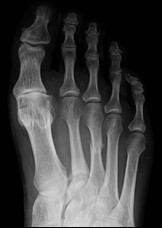
Na radiogramie stopy uwidocznione jest złamanie trzonu
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez