Pytanie 1
Metoda oczyszczania substancji oparta na różnicach w rozpuszczalności poszczególnych składników w określonym rozpuszczalniku to
Wynik: 30/40 punktów (75,0%)
Wymagane minimum: 20 punktów (50%)
Metoda oczyszczania substancji oparta na różnicach w rozpuszczalności poszczególnych składników w określonym rozpuszczalniku to
Podczas pipetowania menisk górny określa się dla roztworów
Sód powinien być przechowywany
Nie należy używać gorącej wody do mycia
Oddzielanie płynnej mieszaniny wieloskładnikowej poprzez odparowanie, a następnie skraplanie jej komponentów, to proces
Na podstawie zamieszczonych w tabeli opisów metod rozdzielania mieszanin, dobierz odpowiadające im nazwy.
| Tabela. Metody rozdzielania mieszanin | |
|---|---|
| Lp. | Opis metody |
| I. | Zlewanie cieczy znad osadu. |
| II. | Przeprowadzenie ciekłego rozpuszczalnika w stan pary. |
| III. | Wyodrębnianie z mieszaniny ciał stałych lub cieczy składnika przy pomocy rozpuszczalnika tak dobranego, aby rozpuszczał żądany związek chemiczny. |
| IV. | Powolne opadanie cząstek substancji stałej w cieczy pod wpływem własnego ciężaru. |
Z analizy wykresu wynika, że substancją o najniższej rozpuszczalności w wodzie w temperaturze 100°C jest
Jednym z sposobów oddzielania jednorodnych mieszanin jest
Jakim kolorem zazwyczaj oznacza się przewody w instalacji gazowej w laboratorium?
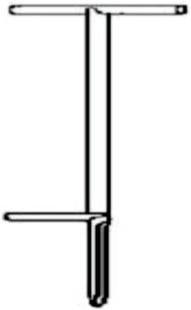
Na rysunku przedstawiony jest przyrząd do poboru próbek
Ekstrakcję w trybie ciągłym przeprowadza się
Materiał uzyskany przez zmieszanie prób pobranych w ustalonych odstępach czasu określa się mianem próbki
Na diagramie przedstawiającym proces pobierania prób środowiskowych do analizy literą Y oznaczono próbkę
Ropa naftowa stanowi mieszankę węglowodorów. Jaką metodę wykorzystuje się do jej rozdzielania na składniki?
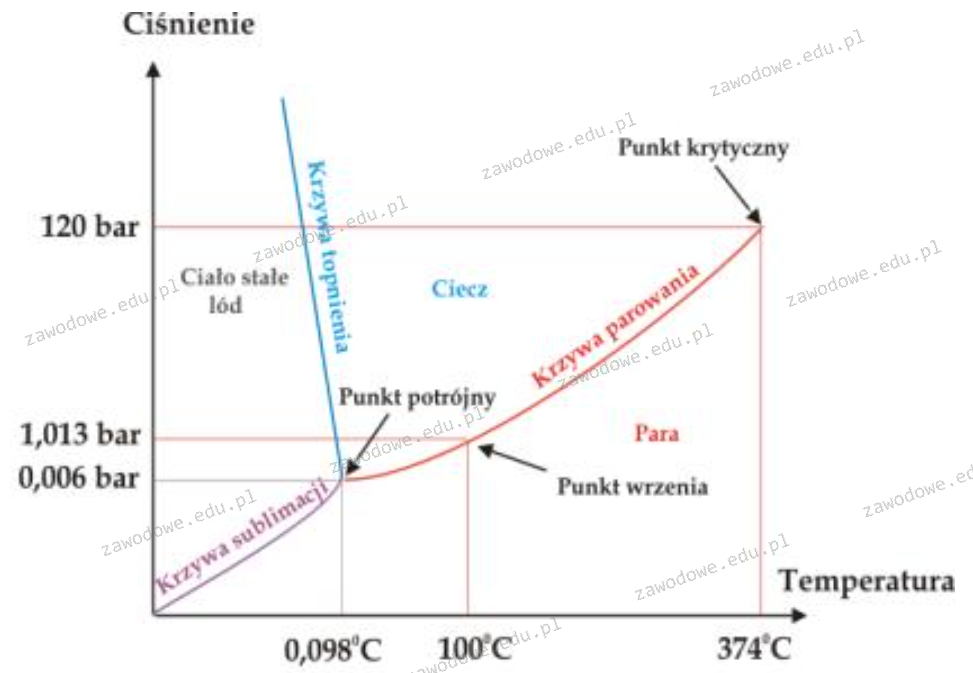
Korzystając z wykresu wskaż, w jakiej postaci występuje woda w temperaturze 10°C i pod ciśnieniem 100 barów.
Podczas pomiaru masy substancji w naczyniu wagowym na wadze technicznej, dla zrównoważenia masy na szalce zastosowano odważniki: 10 g, 5 g, 500 mg, 200 mg, 200 mg, 50 mg, 20 mg, 10 mg oraz 10 mg. Masa substancji razem z naczynkiem wyniosła
Skalę wzorców do oznaczenia barwy przygotowano w cylindrach Nesslera o pojemności 100 cm3. Barwa oznaczona w tabeli jako X wynosi
| Skala wzorców do barwy | ||||
|---|---|---|---|---|
| Ilość wzorcowego roztworu podstawowego cm3 (c=500 mg Pt/dm3) | 0 | 1,0 | 2,0 | 3,0 |
| Barwa w stopniach mg Pt/dm3 | 0 | 5 | X | 15 |
Deminimalizowaną wodę można uzyskać przez
Którą z poniższych czynności należy wykonać, aby zapewnić wysoką dokładność pomiaru masy substancji podczas przygotowywania próbki do analizy chemicznej?
Odczynnik, który nie został wykorzystany, należy zutylizować zgodnie z informacjami zawartymi na etykiecie
Osoba pracująca z lotnym rozpuszczalnikiem straciła przytomność. Jakie działania należy podjąć, aby udzielić pierwszej pomocy?
Aby zregenerować rozpuszczalnik organiczny, należy wykonać proces
Przedstawiony piktogram powinien być zamieszczony na butelce zawierającej

Ile masy kwasu mrówkowego jest wymagane do uzyskania 11,2 dm3 tlenku węgla(II) (w warunkach normalnych) w procesie odwodnienia kwasu mrówkowego (M = 46 g/mol) za pomocą kwasu siarkowego(VI), zakładając efektywność procesu na poziomie 70%?
Na podstawie informacji zawartych w tabeli wskaż mieszaninę oziębiającą o temperaturze -21 °C.
| Temperatura mieszaniny | Skład mieszaniny | Stosunek masowy |
| -15 °C | lód + octan sodu | 10:9 |
| -18 °C | lód + chlorek amonu | 10:3 |
| -21 °C | lód + chlorek sodu | 3:1 |
| -25 °C | lód + azotan amonu | 1:9 |
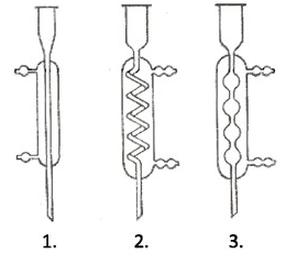
Rysunek przedstawia chłodnice:
Która z metod pozwala na oddzielanie składników mieszaniny na podstawie różnic w ich zachowaniu w układzie składającym się z dwóch faz, z których jedna jest fazą stacjonarną, a druga porusza się w określonym kierunku względem niej?
Do grupy reagentów o szczególnym zastosowaniu nie wlicza się
Ilustracja przedstawia fragment szklanej pipety wielomiarowej

Butle gazowe (czasy butli) napełnione wodorem są oznaczone kolorem
Podczas pobierania próby wody do oznaczania metali ciężkich zaleca się stosowanie butelek wykonanych z:
Naczynia miarowe, skalibrowane "na wlew" (IN) to:
Na etykiecie odważki analitycznej znajduje się napis: Z odważki tej można przygotować
Odważka analityczna azotan(V) srebra(I) AgNO3 0,1 mol/dm3 |
Mianowanie roztworu KMnO4 następuje według poniższej procedury:
Około 0,2 g szczawianu sodu, ważonego z dokładnością ±0,1 mg, przenosi się do kolby stożkowej, rozpuszcza w około 100 cm3 wody destylowanej, następnie dodaje się 10 cm3 roztworu kwasu siarkowego(VI) i podgrzewa do temperatury około 70 °C. Miareczkowanie przeprowadza się roztworem KMnO4 do momentu uzyskania trwałego, jasnoróżowego koloru.
Powyższa procedura odnosi się do miareczkowania
W celu sprawdzenia stężenia kwasu siarkowego(VI) odważono 1 g badanego kwasu i przeprowadzono analizę miareczkową, w której zużyto 20,4 \( \text{cm}^3 \) roztworu NaOH.
Stężenie procentowe badanego kwasu, obliczone na podstawie wzoru wynosi
$$ C_p = \frac{0,02452 \cdot V_{NaOH}}{mp} \cdot 100\% $$gdzie:
\( C_p \) – stężenie procentowe badanego kwasu; \( \% \)
\( 0,02452 \) – współczynnik przeliczeniowy; \( \text{g/cm}^3 \)
\( V_{NaOH} \) – objętość roztworu NaOH, zużyta w miareczkowaniu; \( \text{cm}^3 \)
\( mp \) – odważka badanego kwasu; g
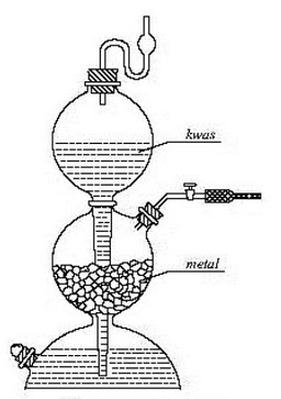
Na rysunku przedstawiono aparat
Jakie jest przeznaczenie pieca muflowego?
Pierwotna próbka jest zbierana
Etykieta roztworu kwasu azotowego(V) o koncentracji 6 mol/dm3 powinna zawierać nazwę substancji oraz
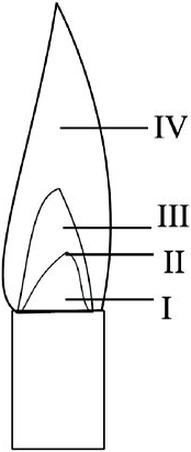
Na rysunku przedstawiającym płomień palnika gazowego najwyższa temperatura płomienia znajduje się w strefie