Pytanie 1
Przy transporcie próbek wody zaleca się, aby próbki były
Wynik: 28/40 punktów (70,0%)
Wymagane minimum: 20 punktów (50%)
Przy transporcie próbek wody zaleca się, aby próbki były
Butle gazowe (czasy butli) napełnione wodorem są oznaczone kolorem
Część partii pobrana w sposób jednorazowy z jednego źródła towaru zapakowanego lub z jednego opakowania jednostkowego określana jest mianem próbki
Sód metaliczny powinien być przechowywany w laboratorium
Korzystając z danych w tabeli wskaż, ile cm3 36% roztworu HCl należy użyć, aby przygotować 250 cm3 0,1-molowego roztworu tego kwasu.
| % wagowy [%] | d420 [g/cm3] | m HCl w 100 cm3 [g/100cm3] | CM HCl [mol/dm3] |
|---|---|---|---|
| 30 | 1,1492 | 34,48 | 9,46 |
| 32 | 1,1593 | 37,10 | 10,17 |
| 34 | 1,1691 | 39,75 | 10,90 |
| 36 | 1,1789 | 42,44 | 11,64 |
Zdjęcie przedstawia palnik

Skuteczny środek do osuszania
Z podanych w tabeli danych wybierz sprzęt potrzebny do zmontowania zestawu do destylacji z parą wodną.
| 1 | 2 | 3 | 4 | 5 |
| manometr | kociołek miedziany | chłodnica powietrzna | kolba destylacyjna | odbieralnik |
Który symbol literowy umieszczany na naczyniach miarowych wskazuje na kalibrację do "wlewu"?
Woda, która została poddana dwukrotnej destylacji, to woda
W nieopisanej butelce prawdopodobnie znajduje się roztwór zasadowy. Wskaż odczynnik, który pozwoli to zweryfikować?
Do wykonania preparatu według zamieszczonej procedury należy przygotować wagę, łyżeczkę, palnik gazowy, trójnóg, bagietkę, szczypce metalowe oraz
| Procedura otrzymywania tlenku magnezu przez prażenie węglanu magnezu. Odważoną ilość węglanu magnezu ubić dokładnie w tyglu (wcześniej zważonym) i przykryć pokrywką. Początkowo ogrzewać niewielkim kopcącym płomieniem, a następnie gdy tygiel ogrzeje się, ogrzewać silniej w temperaturze czerwonego żaru przez około 20 minut. Po zakończeniu prażenia tygiel odstawić do ostudzenia chroniąc przed wilgocią. Zważyć tygiel z preparatem i obliczyć wydajność. |
Niemetal o kolorze fioletowoczarnym, który łatwo przechodzi w stan gazowy, to
Stosunek masowy miedzi do siarki w siarczku miedzi(I) wynosi
| 16S Siarka 32 | 29Cu Miedź 63,55 |
Do grupy reagentów o szczególnym zastosowaniu nie wlicza się
Do 200 g roztworu NaOH (M = 40 g/mol) o stężeniu 10 % dodano wodę destylowaną w kolbie miarowej o pojemności 500 cm3 do znaku. Jakie jest stężenie molowe powstałego roztworu?
Dla cieczy bezbarwnej odczyt w biurecie pokazanej na rysunku wynosi

Transformacja zolu w żel to zjawisko określane jako
Na etykiecie kwasu siarkowego(VI) znajduje się zapis:
Określ gęstość kwasu siarkowego(VI).
KWAS SIARKOWY MIN. 95% CZ.D.A. H2SO4 M = 98,08 g/mol 1 l – 1,84 kg |
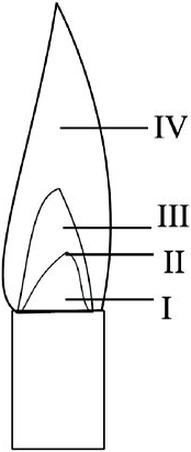
Na rysunku przedstawiającym płomień palnika gazowego najwyższa temperatura płomienia znajduje się w strefie
Jakie środki należy zastosować do gaszenia pożaru metali, takich jak magnez, sód czy potas?
Jakie urządzenie służy do pomiaru temperatury topnienia substancji chemicznych?
Rysunek przedstawia

W którym wierszu tabeli podano ilości substancji i wody, potrzebne do sporządzenia 350 g roztworu o stężeniu 7%?
| Masa substancji | Masa wody | |
|---|---|---|
| A. | 24,5 g | 350 g |
| B. | 24,5 g | 325,5 g |
| C. | 7 g | 343 g |
| D. | 7 g | 350 g |
Oblicz stężenie molowe 250 cm3 roztworu NaOH, w którym znajduje się 0,5 g substancji. Masa molowa NaOH wynosi 40 g/mol
Odważka analityczna przygotowana w fabryce zawiera 0,1 mola EDTA. Posiadając taką jedną odważkę analityczną, jakie roztwory można przygotować?
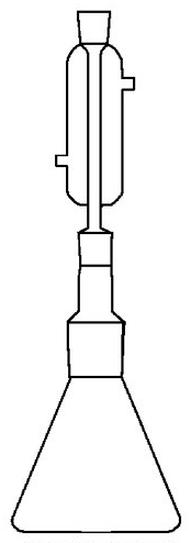
Zestaw przedstawiony na rysunku może służyć do
W trakcie reakcji estryfikacji opisanej równaniem CH3COOH + C2H5OH ↔ CH3COOC2H5 + H2O użyto molowego stosunku alkoholu do kwasu wynoszącego 1:10. W rezultacie tego
Który z wymienionych roztworów NaOH, o określonych stężeniach, nie jest roztworem mianowanym?
Na opakowaniu fenolu umieszcza się przedstawiony na rysunku znak ostrzegawczy, który oznacza, że jest to substancja

Na podstawie danych zawartych w tabeli wskaż, które opakowania zawierają produkt zgodny ze specyfikacją.
| WŁAŚCIWOŚCI | NORMA KLASY A wg specyfikacji produktu | OPAKOWANIE | ||
|---|---|---|---|---|
| 1 | 2 | 3 | ||
| POSTAĆ | Bezbarwna ciecz, bez zanieczyszczeń. Dopuszcza się niebieskawе zabаrwienie i obecność skrystalizowanego osadu | Bezbarwna ciecz | ||
| Zawartość ługu sodowego (NaOH), min, % masy | 46,0 | 46,5 | 46,8 | 48,0 |
| Węglan sodu (Na₂CO₃), nie więcej niż, % masy | 0,4 | 0,3 | 0,3 | 0,2 |
| Chlorek sodu (NaCl), nie więcej niż, % masy | 0,020 | 0,015 | 0,014 | 0,011 |
| Chloran sodu (NaClO₃), nie więcej niż, % masy | 0,007 | 0,006 | 0,005 | 0,002 |
| Siarczan sodu (Na₂SO₄), nie więcej niż, % masy | 0,040 | 0,038 | 0,035 | 0,029 |
| Zawartość żelaza (Fe₂O₃), max, WT. PPM | 15 | 15 | 15 | 10 |
Naważkę NaOH o masie 0,0400 g rozpuścić w małej ilości wody, a następnie przelać ten roztwór do kolby miarowej o pojemności 500 cm3 i uzupełnić kolbę miarową wodą do tzw. kreski. Masa molowa NaOH wynosi 40,0 g/mol. Jakie jest stężenie molowe przygotowanego roztworu?
Z etykiety wynika, że dany związek mógł być

Czy próbkę laboratoryjną przechowuje się w lodówce, gdy występuje w niej
W chemicznym laboratorium apteczka pierwszej pomocy powinna zawierać
Do systemu odprowadzania ścieków, w formie rozcieńczonego roztworu wodnego o maksymalnej masie 100 g na raz, można wprowadzić
Aby pobrać dokładnie 20 cm3 próbkę wody do przeprowadzenia analiz, należy zastosować
Użycie płuczek jest konieczne w trakcie procesu
Wybierz poprawny zapis jonowy spośród podanych reakcji, w których otrzymywany jest siarczan(VI) baru.
Ropa naftowa stanowi mieszankę węglowodorów. Jaką metodę wykorzystuje się do jej rozdzielania na składniki?