Pytanie 1
Dokładność metody definiowana jest na podstawie ustalonej wartości
Wynik: 28/40 punktów (70,0%)
Wymagane minimum: 20 punktów (50%)
Dokładność metody definiowana jest na podstawie ustalonej wartości
Na podstawie zamieszczonego fragmentu opisu wykonania ćwiczenia ustal, który wskaźnik jakości wody jest określany.
| Oznaczenie polega na określeniu ilości tlenu zużywanej do utleniania substancji organicznych w badanej próbce w ciągu n dób inkubacji w temperaturze 20°C. Ilość tę, w przeliczeniu na 1 dm³ wody, oblicza się jako różnicę zawartości tlenu przed i po inkubacji próbki. |
Jakie jest przeznaczenie próby jodowej, m.in. w produkcji piwa?
Klasyfikacja kwasowości soku owocowego jest związana z metodami
Lepkość oleju napędowego w temperaturze 40°C wynosi 3 mm2/s. Jaką lepkość to określa?
Wartość liczby estrowej (LE), określona ilością miligramów KOH potrzebnych do zmydlenia estrów w 1 g analizowanego tłuszczu, wskazuje
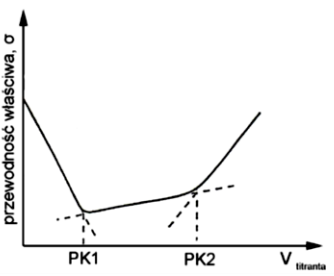
Rysunek przedstawia krzywą miareczkowania
Podłoże, które zawiera wyłącznie substancje niezbędne do rozwoju mikroorganizmów, określane jest jako
W trakcie oznaczania węglanu sodu przy użyciu wodorotlenku sodu metodą Wardera warto miareczkować próbkę od razu przy umiarkowanym mieszaniu, ponieważ mogą się rozpuszczać cząsteczki CO2 z atmosfery, co skutkuje
Zamieszczony opis dotyczy barwienia bakterii metodą
| − fiolet krystaliczny, 2-3 minuty, |
| − płyn Lugola, 1-2 minuty, |
| − alkohol aż do odbarwienia, ok. 30 sekund, |
| − woda – spłukanie, |
| − fuksyna w roztworze fenolowym (rozcieńczenie1:10), 20 sekund, |
| − woda – spłukanie |
Reakcja, na której opiera się oznaczenie liczby zmydlania (LZ) tłuszczów, to
W jakich dziedzinach wykorzystuje się wskaźniki metalochromowe?
Jakim urządzeniem mierzy się zasolenie gleby?
Na podstawie zamieszczonego opisu wskaż, którą metodę stosuje się do oznaczania zawartości kwasu acetylosalicylowego.
| Oznaczenie zawartości kwasu acetylosalicylowego w preparacie farmaceutycznym |
| Oznaczenie polega na hydrolizie tego kwasu na gorąco, za pomocą mianowanego roztworu wodorotlenku sodu o stężeniu 0,1 mol/dm3, do salicylanu i octanu sodu. Nadmiar NaOH odmiareczkowuje się mianowanym roztworem kwasu siarkowego(VI) wobec fenoloftaleiny jako wskaźnika. |
W celu identyfikacji cukru sporządzono jego roztwór i przelano do trzech probówek. Następnie przeprowadzono doświadczenia, których wyniki zapisano w tabeli:
Badanym cukrem była
| Badany roztwór | Dodany odczynnik | Obserwacje |
|---|---|---|
| Probówka 1. | Cu(OH)2 | Zawiesina Cu(OH)2 rozpuściła się, a roztwór przyjął szafirową barwę |
| Cu(OH)2 | Po ogrzaniu probówki pojawił się ceglasto-czerwony osad | |
| Probówka 2. | [Ag(NH3)2]+ | Po ogrzaniu na ściankach probówki pojawiło się srebro metaliczne |
| Probówka 3. | Br2(aq) + roztwór NaHCO3 | Woda bromowa uległa odbarwieniu |
Jaką objętość rozcieńczalnika zużyto na przygotowanie wskazanego w opisie rozcieńczenia próbki mleka?
| Wykonać dziesiętne rozcieńczenia mleka z 10 cm3 próbki. Pierwsze rozcieńczenie wykonać w kolbie o pojemności 250 cm3: do 90 cm3 rozcieńczalnika dodać 10 cm3 próby, dokładnie wymieszać; z tego rozcieńczenia pobrać 0,5 cm3 i przenieść do 4,5 cm3 rozcieńczalnika. Postępować w ten sam sposób, aż do uzyskania rozcieńczenia 1:100000. |
Jakie jest odpowiednie wskaźnik w kompleksometrycznym oznaczaniu magnezu?
Wartości iloczynów rozpuszczalności związków srebra wynoszą odpowiednio: Osad której soli srebra wytrąci się jako pierwszy podczas dodawania jonów Ag+ do roztworu zawierającego jony I-, Br-, Cl- oraz CN-?
| Związek chemiczny | Iloczyn rozpuszczalności |
|---|---|
| AgCl | 1,8·10-10 |
| AgBr | 5,3·10-13 |
| AgCN | 1,4·10-16 |
| AgI | 8,3·10-17 |
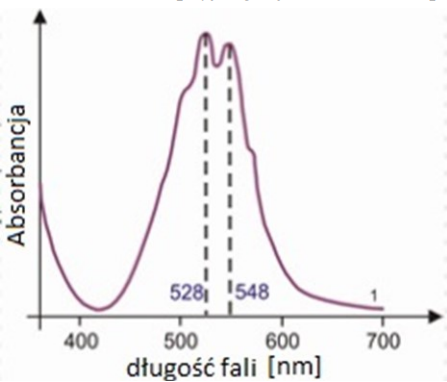
Która z przedstawionych na wykresie długości fali widma absorpcyjnego jonów MnO4- powinna być stosowana jako długość analityczna?
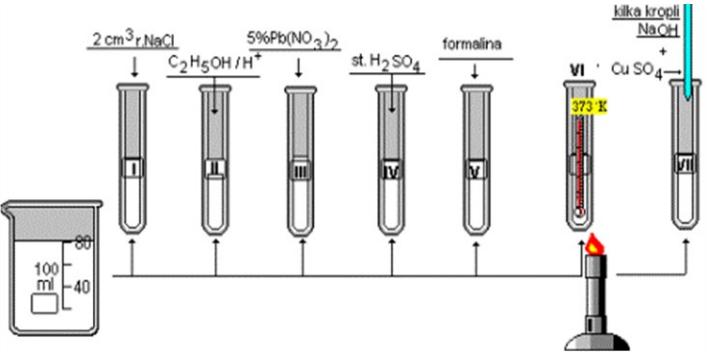
Na rysunku przedstawiono schemat doświadczenia pozwalającego na zbadanie właściwości
Wśród wskaźników stosowanych w analizach kompleksometrycznych znajdują się
Do kationów trzeciej grupy analitycznej, wytrącanych w postaci siarczków roztworem AKT w środowisku amoniakalnym, należą:
| A. Ba2+, Ca2+, Sr2+ |
| B. Fe2+, Mg2+, Pb2+, Al3+, Ca2+ |
| C. Ni2+, Co2+, Fe2+, Fe3+, Mn2+, Zn2+ |
| D. Pb2+, Cu2+, Cd2+, Cr3+, Ag+, K+, Al3+ |
Białka, których cząsteczki mają wiązania peptydowe, w reakcji z jonami miedzi(II) w środowisku zasadowym tworzą kompleks o barwie fioletowej. Stopień intensywności barwy jest proporcjonalny do liczby wiązań peptydowych. Tę zależność można wykorzystać do oznaczeń
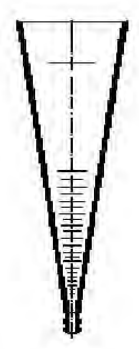
Na rysunku przedstawiono sprzęt stosowany do
Oznaczono zawartość cynku w stopie metodą kompleksometryczną. W tym celu odważono 0,50 g stopu i przeprowadzono do roztworu. Próbkę do badań przygotowano w kolbie miarowej o pojemności 250 cm3. Następnie do trzech kolb stożkowych odpipetowano po 50 cm3 roztworu z przygotowanej próbki do badań. Próbki miareczkowano roztworem EDTA o stężeniu 0,01 mmol/cm3. Zużyta średnia objętość roztworu EDTA wyniosła 32,5 cm3. Korzystając z zamieszczonego wzoru, oblicz procentową zawartość cynku w stopie.
| mZn = V · CEDTA · 65,37 · W |
| mZn – masa cynku; mg V – objętość zużytego roztworu EDTA w trakcie miareczkowania; cm3 CEDTA – stężenie molowe roztworu EDTA; mmol/cm3 65,37 – masa molowa cynku; mg/mmol W – współmierność kolby miarowej i pipety; 5 |
Przeprowadzano analizę jakościową próbki według schematu:
Badana próbka zawierała kation
| badany roztwór zawierający jony X2+ | |
| + roztwór HCl | |
| XCl2↓ biały osad | |
| + H2O: ogrzać | |
| roztwór X2+: podzielić na 2 części | |
| + roztwór KI | oziębić |
| XI2 żółty osad | XCl2↓ biały osad |
W kolbie o pojemności 250 cm3 stworzono roztwór zawierający 1,4025 g KOH. Jaką wartość pH powinien mieć otrzymany roztwór?
MKOH = 56,1 g/mol
Do czego używa się polarymetru?
Wykonano identyfikację opisaną w schemacie:
BaCl2 + X — biały osadJaki wzór reprezentuje substrat X?
Przedstawiony wzór opisuje titrant stosowany podczas miareczkowania
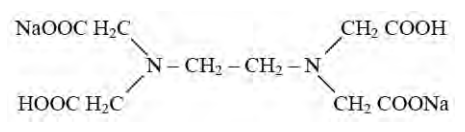
W tabeli przedstawiono charakterystykę
| Charakterystyka wybranych metod optycznych stosowanych w analizie instrumentalnej | ||
|---|---|---|
| Metoda | Obserwowane zjawisko | Pomiar |
| 1 | załamanie światła | współczynnik załamania światła padającego na powierzchnię próbki |
| 2 | skręcanie płaszczyzny światła spolaryzowanego | kąt skręcenia płaszczyzny polaryzacji światła |
| 3 | rozproszenie promieniowania | natężenie wiązki światła rozproszonego wychodzącego z kuwety pomiarowej |
Ile miligramów wapnia (MCa = 40,0 g/mol) znajdowało się w analizowanym roztworze, jeśli do zmiareczkowania próbki wykorzystano 20 cm3 0,0100-molowego roztworu EDTA?
Raport z analizy próbki wody nie zawiera
Ile wynosi refrakcja molowa kwasu octowego o gęstości równej 1,0498 g/cm3, jeżeli współczynnik załamania światła wynosi 1,3874, a masa molowa kwasu octowego jest równa 60,054 g/mol?
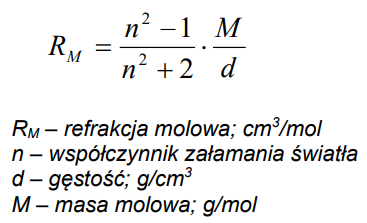
Działanie, które ma na celu określenie relacji pomiędzy wartościami mierzonymi dla wzorcowych próbek a odczytami systemu pomiarowego, realizowane w specyficznych warunkach, to
W Polsce normy dotyczące pyłów zawieszonych PM10 są określone na trzech poziomach (dobowych):
- poziom dopuszczalny 50 ug/m3 - oznacza, że jakość powietrza nie jest zadowalająca, ale nie wywołuje poważnych skutków dla zdrowia ludzi.
- poziom informacyjny 200 ug/m3 - oznacza, że stan powietrza jest zły i należy ograniczyć aktywności na świeżym powietrzu, gdyż normę przekroczono czterokrotnie.
- poziom alarmowy 300 ug/m3 - wskazuje, że jakość powietrza jest bardzo zła, norma przekroczona sześciokrotnie i konieczne jest zdecydowane ograniczenie pobytu na zewnątrz, a najlepiej pozostać w domu, szczególnie dla osób chorych.
Na stacji Monitoringu Środowiska przeprowadzono pomiary zanieczyszczenia powietrza pyłem PM10, uzyskując średnią dobową wartość 0,25 mg/m3. Z analizy wynika, że
W tabeli przedstawiono fragment opisu parametrów
| Zakresy pomiarowe | Przewodnictwo: 0,01 µS/cm÷500 mS/cm Zasolenie: 0,0÷1999 mg/l NaCl 2.0÷50,0 g/l NaCl |
| Błąd pomiaru (± 1 cyfra) | Przewodnictwo ≤ 0,5%, Zasolenie ≤ 0,5%, |
| Temperatura odniesienia | 20 lub 25°C. Ustawienie fabryczne: 25°C |
| Warunki otoczenia | Temperatura pracy: 0°C do 50°C, temperatura przechowywania: -15°C do 65°C, 80% wilgotności względnej (bez kondensacji) |
W wyniku badań mikrobiologicznych wody przeznaczonej do produkcji soków, po 3 dniach inkubacji stwierdzono w 1 ml próbki 100 j.t.k. bakterii, w tym 2 j.t.k Escherichia coli.
Ustal jakość wody na podstawie informacji zamieszczonych w tabeli.
| Wymagania mikrobiologiczne, jakim powinna odpowiadać woda | ||
|---|---|---|
| Lp. | Parametr | Najwyższa dopuszczalna wartość liczby jednostek tworzących kolonię [j.t.k] |
| 1 | Escherichia coli | 0 |
| 2 | Enterokoki | 0 |
| 3 | Pseudomonas aeruginosa | 0 |
| 4 | Ogólna liczba mikroorganizmów w (36±2) °C po 48h | 20 |
| 5 | Ogólna liczba mikroorganizmów w (22±2) °C po 72h | 100 |
Wskaż grupę związków chemicznych powodujących twardość niewęglanową wody.
| A. | CaSO4, MgCl2, Ca(NO3)2, MgSO4 |
| B. | CaCl2, Ca(HCO3)2, MgCl2, MnSO4 |
| C. | Ca(NO3)2, Ca(HCO3)2, MgCl2, MnSO4 |
| D. | CaCO3, Mg(HCO3)2, MgSO4, Ca(NO3)2 |
Podłoże do izolacji i identyfikacji bakterii hemolizujących powinno zawierać