Pytanie 1
Zamieszczony piktogram przedstawia substancję o klasie i kategorii zagrożenia:

Wynik: 33/40 punktów (82,5%)
Wymagane minimum: 20 punktów (50%)
Zamieszczony piktogram przedstawia substancję o klasie i kategorii zagrożenia:

Proces chemiczny, który polega na przejściu substancji w stanie stałym do roztworu, związany z reakcją tej substancji z rozpuszczalnikiem, to
Skuteczny środek do osuszania
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
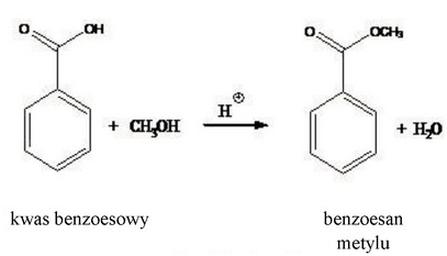
Do reakcji estryfikacji użyto 150 g kwasu benzoesowego (M = 122,12 g/mol), w wyniku której otrzymano czysty preparat benzoesanu metylu (M = 136,2 g/mol). Ile gramów benzoesanu metylu otrzymano, jeżeli reakcja przebiegała z wydajnością 92%?
Jakie procesy towarzyszy efekt egzotermiczny?
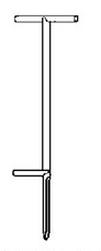
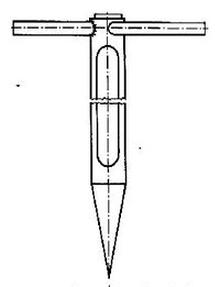
Przedstawiony na rysunku zagłębnik stosuje się do pobierania próbek
Aby przygotować roztwór wzorcowy potrzebny do oznaczania miana, konieczne jest użycie odczynnika chemicznego o czystości przynajmniej
Którego z poniższych naczyń laboratoryjnych nie powinno się używać do podgrzania 100 cm3wody?
Który z podanych związków chemicznych można wykorzystać do oceny całkowitego usunięcia jonów chlorkowych z osadu?
Urządzeniem pomiarowym nie jest
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Określ, jakie informacje powinny być zarejestrowane w ewidencji wydania substancji niebezpiecznych, stosowanych w badaniach laboratoryjnych?
Aby rozpuścić próbkę tłuszczu o wadze 5 g, wykorzystuje się 50 cm3 mieszanki 96% alkoholu etylowego oraz eteru dietylowego, połączonych w proporcji objętościowej 1 : 2. Jakie ilości cm3 każdego ze składników są potrzebne do przygotowania 150 cm3 tej mieszanki?
W próbkach obecne są składniki, które znacznie różnią się pod względem zawartości. Składnik, którego procentowy udział w próbce jest niższy od 0,01%, nazywamy
Według zasady pierwszeństwa, znajdując na opakowaniu zbiorczym odczynnika piktogramy pokazane na rysunku, należy zwrócić szczególną uwagę na to, że substancja jest
Technika oddzielania płynnych mieszanin, w której wykorzystuje się różnice w prędkości migracji składników przez odpowiednią bibułę, nazywa się
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Które równanie przedstawia reakcję otrzymywania mydła?
| CH3COOH + NaOH →CH3COONa + H2O | 2 CH3COOH + Na2O →2 CH3COONa + H2O | 2 C2H5COOH + 2 Na →2 C2H5COONa + H2↑ | C17H35COOH + NaOH →C17H35COONa + H2O |
Do przechowywania zamrożonych próbek wody stosuje się naczynia wykonane
Jakim przyrządem nie jest możliwe określenie gęstości cieczy?
Piknometr służy do określania
Jakie proporcje objętościowe powinny być zastosowane do zmieszania roztworu etanolu o stężeniu 30% (V/V) z roztworem o stężeniu 70% (V/V), aby uzyskać roztwór o stężeniu 50% (V/V)?
Piktogramem przedstawionym na rysunku znakuje się opakowanie substancji

Jakie urządzenie wykorzystuje się do określania lepkości płynów?
Aby wykonać chromatografię cienkowarstwową, należy przygotować eluent składający się z toluenu, acetonu oraz kwasu mrówkowego w proporcjach objętościowych 10:4:1. Jakie ilości poszczególnych składników powinny być wykorzystane do uzyskania 300 cm3 eluentu?
Najskuteczniejszą techniką separacji ketonu oraz kwasu karboksylowego obecnych w roztworze benzenowym jest
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Aby oszacować czystość MgCO3, poddano prażeniu próbkę o wadze 5 g tej soli aż do osiągnięcia stałej masy. W trakcie prażenia zachodzi reakcja:
MgCO3 → MgO + CO2 Całkowity ubytek masy wyniósł 2,38 g.
(Masy molowe reagentów to: MgCO3 – 84 g/mol, MgO – 40 g/mol, CO2 – 44 g/mol) Jaką czystość miała próbka węglanu magnezu?
Na podstawie zamieszczonych informacji, wskaż ilości odczynników, które są niezbędne do przygotowania skali wzorców do kolorymetrycznego oznaczania rozpuszczalnych fosforanów(V).
| Przygotowanie skali wzorców do kolometrycznego oznaczania fosforanów(V) | ||||||||
| Do ośmiu cylindrów Nesslera o pojemności 100 cm3 odmierzyć kolejno wzorcowy roztwór roboczy KH2PO4 według poniższej tabeli SKALA WZORCÓW (PO43-) i uzupełnić wodą do kreski. Do każdego cylindra dodać 2 cm3 roztworu molibdenianu amonu (heksaamonoheptamolibdenian(VI)), wymieszać, dodać 0,2 cm3 roztworu SnCl2 i ponownie wymieszać. | ||||||||
| SKALA WZORCÓW (PO43-) | ||||||||
| Wzorcowy roztwór roboczy [cm3] | 0,0 | 0,5 | 1,0 | 2,0 | 3,0 | 5,0 | 7,0 | 10,0 |
| Zawartość PO43- [mg] | 0,0 | 0,005 | 0,01 | 0,02 | 0,03 | 0,05 | 0,07 | 0,10 |
| Roztwór | KH₂PO₄ | (NH₄)₆Mo₇O₂₄ | SnCl₂ |
|---|---|---|---|
| A. | 28,5 cm³ | 8,0 cm³ | 0,16 cm³ |
| B. | 0,285 cm³ | 16,0 cm³ | 1,6 cm³ |
| C. | 28,5 cm³ | 16,0 cm³ | 1,6 cm³ |
| D. | 0,285 cm³ | 8,0 cm³ | 16 cm³ |
Reagenty o czystości na poziomie 99,999% — 99,9999% to reagenty
Aby ustalić miano roztworu wodnego NaOH, należy zastosować
Technika kwartowania (ćwiartkowania) pozwala na redukcję masy próbki ogólnej
Przyrząd przedstawiony na rysunku służy do pobierania próbek substancji
Z podanego wykazu wybierz sprzęt potrzebny do zmontowania zestawu do sączenia pod próżnią.
| 1 | 2 | 3 | 4 | 5 | 6 |
| pompka wodna | lejek z długą nóżką | kolba okrągłodenna | kolba ssawkowa | lejek sitowy | chłodnica powietrzna |
Jakie jest stężenie molowe roztworu, jeśli w 100 cm3 roztworu znajduje się 5,6 g KOH?
MK = 39 g/mol, MO = 16 g/mol, MH = 1 g/mol
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Które z poniższych działań należy wykonać przed rozpoczęciem pracy z nowym szkłem laboratoryjnym?