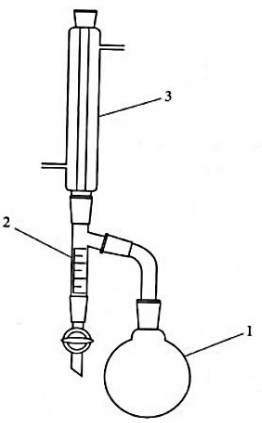
Pytanie 1
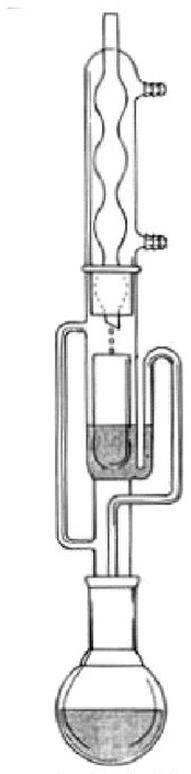
Przedstawiony na rysunku aparat służy do
Wynik: 23/40 punktów (57,5%)
Wymagane minimum: 20 punktów (50%)
Przedstawiony na rysunku aparat służy do

Raport z analizy próbki wody nie zawiera
Jakie jest zastosowanie psychrometru aspiracyjnego?
Oznaczanie jonów cynku przy użyciu EDTA stanowi przykład miareczkowania
Jaką metodę można wykorzystać do oznaczania białek w produktach żywnościowych?
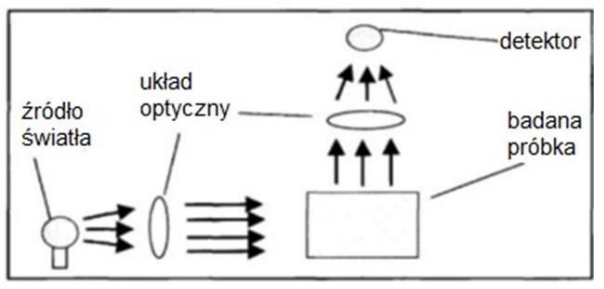
Na schemacie przedstawiono procesy, które zachodzą podczas przygotowania próbek do badań z wykorzystaniem
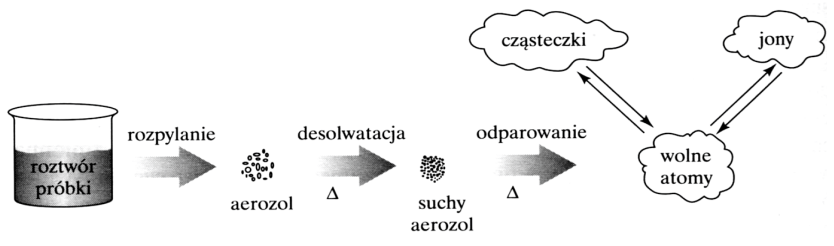
W jakich instrumentalnych metodach optycznych wykorzystuje się zjawiska absorpcji oraz rozpraszania promieniowania elektromagnetycznego?
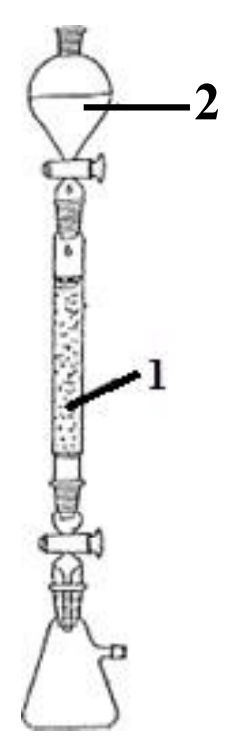
Na rysunku przedstawiono zestaw do chromatografii kolumnowej. Cyfrą 1 oznaczono
Na ilustracji przedstawiono bieg promieni świetlnych
Badanie tłuszczów, w tym m.in. ustalenie ilości mg KOH, potrzebnego do neutralizacji wolnych kwasów tłuszczowych znajdujących się w jednym gramie tłuszczu, dotyczy określenia liczby
Aby zmierzyć kąt skręcenia płaszczyzny światła spolaryzowanego przechodzącego przez analizowaną substancję, należy zastosować metodę
Jaka była zawartość jonów żelaza (II) w oznaczanym roztworze, jeżeli na jego zmiareczkowanie zużyto \( 10 \, \text{cm}^3 \) roztworu \( \text{KMnO}_4 \) o stężeniu \( 0{,}02 \, \text{mol/dm}^3 \)?
Wzór do obliczeń:
$$ m_{Fe} = 5 \cdot c_{mol} \cdot V \cdot M_{Fe} $$
gdzie: \( V \) – objętość roztworu \( \text{KMnO}_4 \) zużyta w czasie miareczkowania [\( \text{dm}^3 \)], \( M_{Fe} = 56 \, \text{g/mol} \), \( c_{mol} \) – stężenie molowe roztworu \( \text{KMnO}_4 \) [\( \text{mol/dm}^3 \)]
Jaką funkcję pełni batometr?
Gęstość granulatów tworzyw sztucznych można określić przy użyciu
Widoczne bez użycia mikroskopu skupisko mikroorganizmów, które powstało z jednej komórki na płytce z podłożem hodowlanym, to
Spektrofotometria w podczerwieni (IR) to technika bazująca na absorpcji promieniowania w zakresie długości fal
Z analizy danych w tabeli rozpuszczalności wynika, że w formie osadu z roztworu wytrąci się
| Na+ | Fe2+ | Pb2+ | Mg2+ | Fe3+ | Ag+ | Zn2+ | |
|---|---|---|---|---|---|---|---|
| SO42- | ↓ | ↓ | |||||
| Br- | ↓ | ↓ | |||||
| Cl- | ↓ | ↓ | |||||
| S2- | ↓ | ↓ | ↓ | ↓ | ↓ | ↓ |
Wskaź kationy, które są możliwe do wykrycia poprzez próbę płomieniową?
Do oceny kwasowości mleka wykorzystuje się metodę miareczkowania
Możliwość stwierdzenia obecności jonów żelaza (III) w próbce można uzyskać poprzez dodanie roztworu
W mikrobiologii metoda sterylizacji przy użyciu suchego, gorącego powietrza zalicza się do
Wykonano jodometryczne oznaczenie zawartości kwasu askorbinowego dla 4 próbek tabletek witaminy C, uzyskując wyniki. Na podstawie informacji zawartych w opisie i wyników analizy można stwierdzić, że zawartość witaminy C
| Opis Na opakowaniach tabletek witaminy C producenci deklarują zawartość 200 mg kwasu askorbinowego. Zgodnie z normą odchylenia od deklarowanej zawartości substancji leczniczej nie mogą przekraczać ±10% dla tabletek o zawartości poniżej 100 mg i ±5% dla tabletek o deklarowanej zawartości 100 mg i więcej. | ||||
| Próbka | 1 | 2 | 3 | 4 |
| Zawartość kwasu askorbinowego | 198,5 mg | 211 mg | 201 mg | 205 mg |
Czym jest eluent?
Dla czterech różnych próbek gleb lekkich o odczynie kwaśnym oznaczono zawartość metali w mg/kg suchej masy. Wyniki zestawiono w tabeli:
Graniczne zawartości metali śladowych w powierzchniowej warstwie gleb bardzo lekkich | |||||
|---|---|---|---|---|---|
| Stopień zanieczyszczenia gleb | Zawartość metali w mg/kg suchej masy | ||||
| Pb | Cd | Zn | Cu | Ni | |
| 0 zawartość naturalna | 30 | 0,3 | 50 | 15 | 10 |
| 1 zawartość podwyższona | 70 | 1 | 100 | 30 | 30 |
| 2 słabe zanieczyszczenie | 100 | 2 | 300 | 50 | 50 |
| 3 średnie zanieczyszczenie | 500 | 3 | 700 | 150 | 100 |
| 4 silne zanieczyszczenie | 2500 | 5 | 3000 | 300 | 400 |
| 5 bardzo silne zanieczyszczenie | >2500 | >5 | >3000 | >300 | >400 |
| Metal | Próbka 1. | Próbka 2. | Próbka 3. | Próbka 4. |
|---|---|---|---|---|
| Pb | 180,0 | 15,0 | 25,0 | 29,0 |
| Cd | 1,6 | 0,3 | 0,2 | 0,6 |
| Zn | 40,0 | 55,5 | 48,0 | 37,0 |
| Cu | 328,0 | 25,0 | 8,0 | 56,0 |
| Ni | 135,0 | 8,0 | 8,0 | 19,0 |
Oznaczono zawartość cynku w stopie metodą kompleksometryczną. W tym celu odważono 0,50 g stopu i przeprowadzono do roztworu. Próbkę do badań przygotowano w kolbie miarowej o pojemności 250 cm3. Następnie do trzech kolb stożkowych odpipetowano po 50 cm3 roztworu z przygotowanej próbki do badań. Próbki miareczkowano roztworem EDTA o stężeniu 0,01 mmol/cm3. Zużyta średnia objętość roztworu EDTA wyniosła 32,5 cm3. Korzystając z zamieszczonego wzoru, oblicz procentową zawartość cynku w stopie.
| mZn = V · CEDTA · 65,37 · W |
| mZn – masa cynku; mg V – objętość zużytego roztworu EDTA w trakcie miareczkowania; cm3 CEDTA – stężenie molowe roztworu EDTA; mmol/cm3 65,37 – masa molowa cynku; mg/mmol W – współmierność kolby miarowej i pipety; 5 |
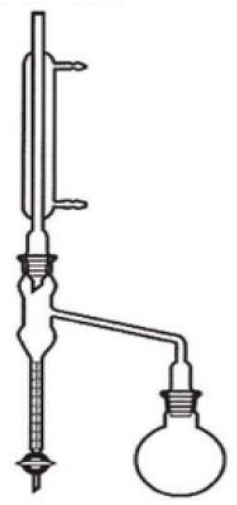
Zawartość wody w produktach spożywczych można oznaczyć za pomocą przedstawionego na rysunku aparatu Deana-Starka metodą
Na ilustracji przedstawiono schemat

Na podstawie danych w tabeli określ, który odczynnik należy dobrać, aby wykryć fenyloalaninę metodą chromatografii bibułowej i cienkowarstwowej.
| Substancje wykrywane | Odczynnik | Skład | Efekt barwny |
|---|---|---|---|
| Kwasy karboksylowe | Zieleń bromokrezolowa | 3% roztwór w metanolu z dodatkiem NaOH | Żółte plamy na zielonym tle |
| Aminokwasy | Ninhydryna | 1-2% roztwór w acetonie | Ogrzanie do temp. 110°C charakterystyczne zabarwienie |
| Lipidy | Błękit bromotymolowy | 0,04% roztwór w NaOH o stęż. 0,01 mol/dm3 | Żółte plamy na zielonym tle |
| Barbiturany | Azotan(V) rtęci(II) | 1% roztwór wodny | Czarne lub białe plamy na szarym tle |
Podłoża o płynnej konsystencji stosuje się w celu
Do zmiareczkowania próbki wodorotlenku sodu o objętości 25 cm3 wykorzystano 20 cm3 roztworu kwasu solnego o stężeniu 0,1020 mol/dm3. Jakie jest stężenie molowe roztworu NaOH?
Analiza cech ropy naftowej realizowana za pomocą wiskozymetru Englera, polegająca na pomiarze czasu wypływu 200 cm3 ropy naftowej w temperaturze 20°C oraz czasu wypływu tej samej objętości wody destylowanej, dotyczy oceny
Jakie urządzenie należy wykorzystać do określenia temperatury wrzenia cieczy?
Karminowoczerwony kolor płomienia palnika w trakcie analiz chemicznych sugeruje obecność w roztworze jonów
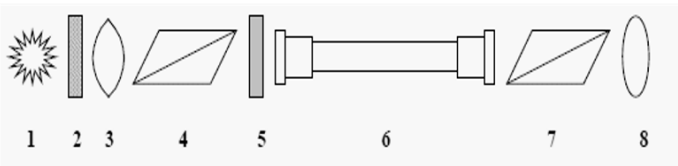
Na rysunku przedstawiającym schemat polarymetru, cyfrą 4 oznaczono
Określenie stężenia jonów Fe3+ w wodzie pitnej powinno być zrealizowane przy użyciu metody
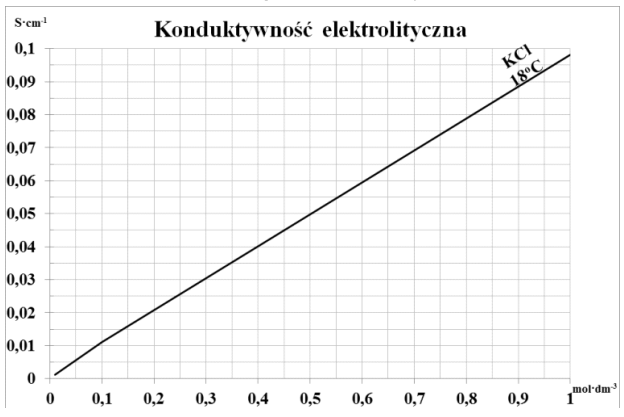
W celu wyznaczenia stężenia badanej próbki chlorku potasu, wykonano krzywą wzorcową zależności konduktywności elektrolitycznej od stężenia. Przewodność badanego roztworu wyniosła 0,045 S∙cm-1. Stężenie badanego roztworu KCl wynosi
Przedstawione reakcje zachodzą w produktach żywnościowych podczas fermentacji
| C12H22O11 + H2O → C6H12O6 + C6H12O6 |
| C6H12O6 → 2 CH3 −CH(OH) −COOH |
Lepkość dynamiczna wody
| Tabela. Gęstość (d) i lepkość dynamiczna wody (η) w danej temperaturze (T). | ||
| T [K] | d [g/cm3] | η [cP] |
| 293 | 0,99823 | 1,0050 |
| 298 | 0,99707 | 0,8937 |
| 303 | 0,99567 | 0,8007 |
| 308 | 0,99406 | 0,7225 |
| 313 | 0,99222 | 0,6560 |
| 318 | 0,99025 | 0,5988 |
| 323 | 0,98807 | 0,5494 |
| 328 | 0,98573 | 0,5064 |
| 333 | 0,98324 | 0,4688 |
Na podstawie przedstawionych wyników pomiarów zawartości tlenu, pH, suchej pozostałości oraz zawartości jonów rtęci w wodzie wskaż, która próbka wody jest prawidłowo zaklasyfikowana.
| Próbka | Wynik pomiaru wskaźnika | |||
|---|---|---|---|---|
| Zawartość O2 [mg/dm3] | pH | Sucha pozostałość [mg/dm3] | Zawartość Hg2+ [mg/dm3] | |
| 1 | 4 | 9 | 1200 | 0,006 |
| 2 | 5 | 8,5 | 600 | 0,0001 |
| 3 | 5,5 | 9 | 900 | 0,0001 |
| Klasa | Wartości dopuszczalne | |||
| I | 6 i powyżej | 6,5 ÷ 8 | 500 i poniżej | 0,001 i poniżej |
| II | 5 i powyżej | 6,5 ÷ 9 | 1000 i poniżej | 0,005 i poniżej |
| III | 4 i powyżej | 6 ÷ 9 | 1200 i poniżej | 0,01 i poniżej |
| Numer próbki wody | Klasa wody | |
|---|---|---|
| A. | 1 | II |
| B. | 2 | II |
| C. | 2 | I |
| D. | 3 | III |
Zestaw przedstawiony na rysunku służy do oznaczania zawartości
Opis schematu:
1 - kolba okrągłodenna
2 - odbieralnik
3 - chłodnica zwrotna