Pytanie 1
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Wynik: 38/40 punktów (95,0%)
Wymagane minimum: 20 punktów (50%)
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Na którym obrazie MR jest widoczne pasmo saturacji?
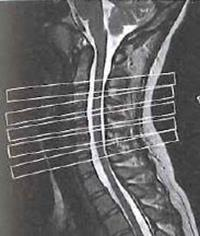

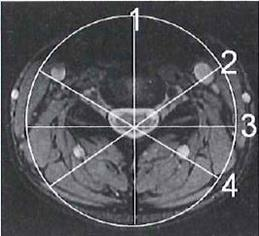
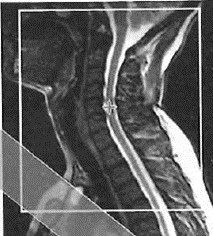
W leczeniu izotopowym tarczycy podaje się
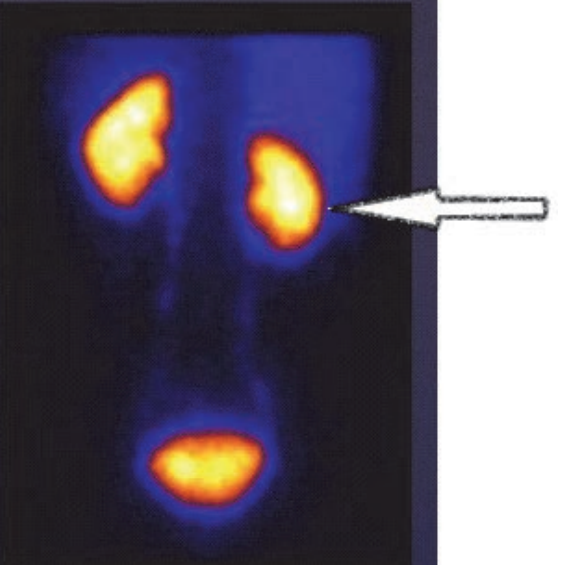
Który obszar napromieniania wskazano na ilustracji strzałką?
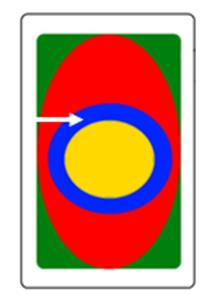
Rytm alfa i beta rejestruje się podczas badania
Rozpoczęcie badania TK nerek po 20-30 sekundach od początku podania środka kontrastowego umożliwia diagnostykę
Radiogram przedstawia
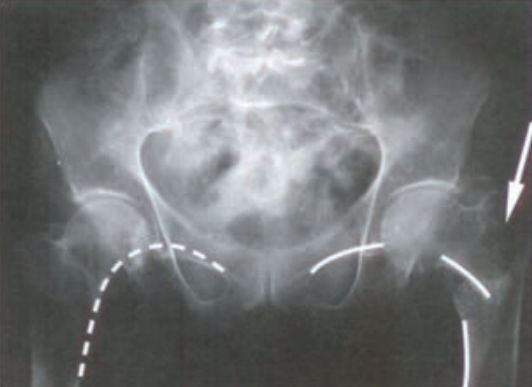
W jaki sposób należy ustawić promień centralny w stosunku do ramienia i przedramienia, by wykonać zdjęcie rentgenograficzne stawu łokciowego u pacjenta z przykurczem?
Które badanie, zgodnie z zakresem kompetencji, może samodzielnie wykonać technik elektroradiolog?
Zdjęcie rentgenowskie nadgarstka w przywiedzeniu dołokciowym jest wykonywane w celu uwidocznienia kości
Który wynik badania tympanometrycznego potwierdza, że słuch badanego pacjenta jest w granicach normy?
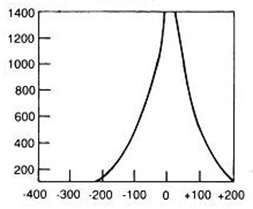
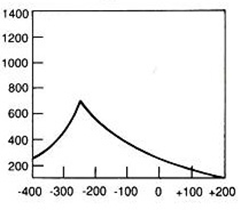
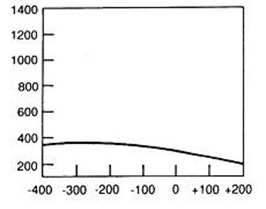
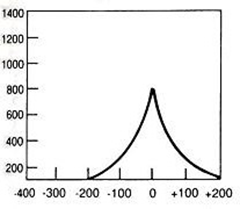
W standardowym badaniu EEG elektrody P3, P4 i Pz umieszcza się na skórze głowy pacjenta nad płatami
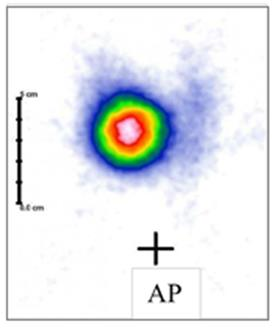
„Ognisko zimne” w obrazie scyntygraficznym określa się jako
Jaka jest moc dawki pochłoniętej w brachyterapii HDR?
Do zdjęcia rentgenowskiego kręgosłupa piersiowego w projekcji AP pacjenta należy ułożyć
Ligand stosuje się
W badaniu audiometrycznym do oceny przewodnictwa kostnego wybranego ucha słuchawkę kostną należy przyłożyć do
W diagnostyce mammograficznej punktowy ucisk sutka stosuje się w projekcji
Glukoza podawana pacjentowi w badaniu PET jest znakowana radioaktywnym
Do wczesnych odczynów popromiennych po radioterapii zalicza się
Jaki rozmiar kasety należy zastosować, wykonując standardowe zdjęcie stawu kolanowego w projekcji bocznej?
Więzka promieniowania X to
Brachyterapia polegająca na wielokrotnym wsuwaniu i wysuwaniu źródła promieniowania do tego samego aplikatora nosi nazwę
Na scyntygramie strzałką oznaczono
Która sekwencja obrazowania MR wykorzystuje impulsy RF o częstotliwości rezonansowej tłuszczu do tłumienia sygnału pochodzącego z tkanki tłuszczowej?
Jednostką indukcji magnetycznej jest
W standardowym badaniu elektrokardiologicznym elektrodę C4 należy umocować
Na scyntygramie tarczycy został uwidoczniony guzek
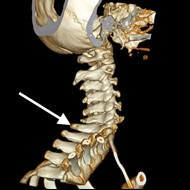
Na obrazie TK kręgosłupa strzałką wskazano wyrostek
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
Brachyterapia polegająca na wielokrotnym wsuwaniu i wysuwaniu źródła promieniowania do tego samego aplikatora nosi nazwę
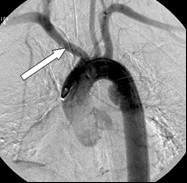
Na obrazie cyfrowej angiografii subtrakcyjnej strzałką zaznaczono
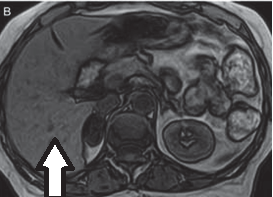
Na przekroju poprzecznym rezonansu magnetycznego strzałką oznaczono
Rutynowe badanie koronarografii prawej tętnicy wieńcowej wykonywane jest w rzucie skośnym przednim
Obrazy DDR są tworzone w trakcie
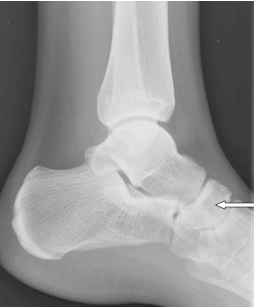
Na radiogramie strzałką oznaczono
Podczas wykonywania badania EEG elektrodę P4 umieszcza się w okolicy
W zapisie EKG zespół QRS odzwierciedla
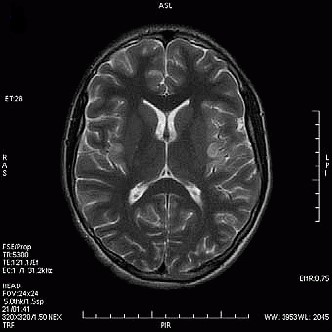
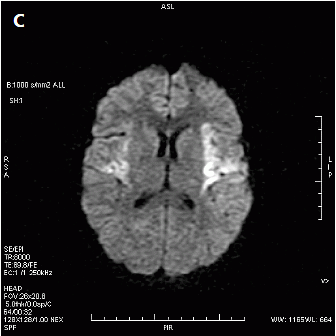
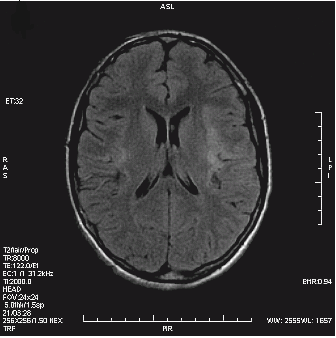
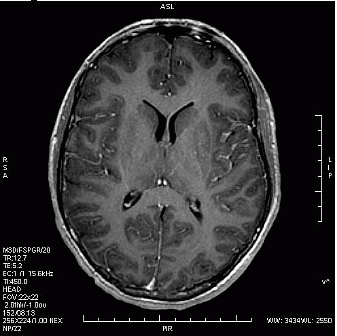
Który obraz MR mózgu został wykonany w sekwencji DWI?
Badanie gęstości mineralnej kości metodą DXA należy wykonać