Pytanie 1
Podczas reakcji chlorku żelaza(III) z wodorotlenkiem potasu dochodzi do wytrącenia wodorotlenku żelaza(III) w formie
Wynik: 17/40 punktów (42,5%)
Wymagane minimum: 20 punktów (50%)
Podczas reakcji chlorku żelaza(III) z wodorotlenkiem potasu dochodzi do wytrącenia wodorotlenku żelaza(III) w formie
Odpady, które w przeważającej mierze składają się z osadów siarczków metali ciężkich, nazywa się
Proces mineralizacji próbki, który polega na jej spopieleniu w piecu muflowym w temperaturze 300-500°C i rozpuszczeniu pozostałych resztek w kwasach w celu oznaczenia zawartości metali ciężkich, to mineralizacja
Który z podanych związków chemicznych można wykorzystać do oceny całkowitego usunięcia jonów chlorkowych z osadu?
Proces wydobywania składnika z cieczy lub ciała stałego w mieszance wieloskładnikowej poprzez jego rozpuszczenie w odpowiednim rozpuszczalniku to
Na podstawie informacji zawartych w tabeli określ, który parametr spośród podanych należy oznaczyć w pierwszej kolejności.
| Tabela. Sposoby utrwalania próbek wody i ścieków, miejsce analizy, dopuszczalny czas przechowywania próbek | ||||
|---|---|---|---|---|
| Oznaczany parametr | Rodzaj naczynia do przechowywania próbki | Sposób utrwalania próbki | Miejsce wykonania analizy | Dopuszczalny czas przechowywania próbki |
| Chlorki | szklane lub polietylenowe | - | laboratorium | 96 godzin |
| Chlor pozostały | szklane | - | w miejscu pobrania próbki | - |
| ChZT | szklane | zakwaszenie do pH<2, schłodzenie do temperatury 2-5°C | laboratorium | 24 godziny |
| Kwasowość | szklane lub polietylenowe | schłodzenie do temperatury 2-5°C | laboratorium | 4 godziny |
| Mangan | szklane lub polietylenowe | zakwaszenie do pH<2, schłodzenie do temperatury 2-5°C | laboratorium | 48 godziny |
Aby przygotować zestaw do filtracji, należy zebrać
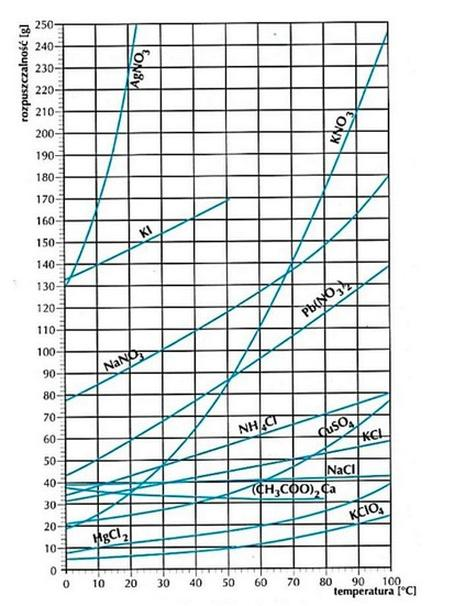
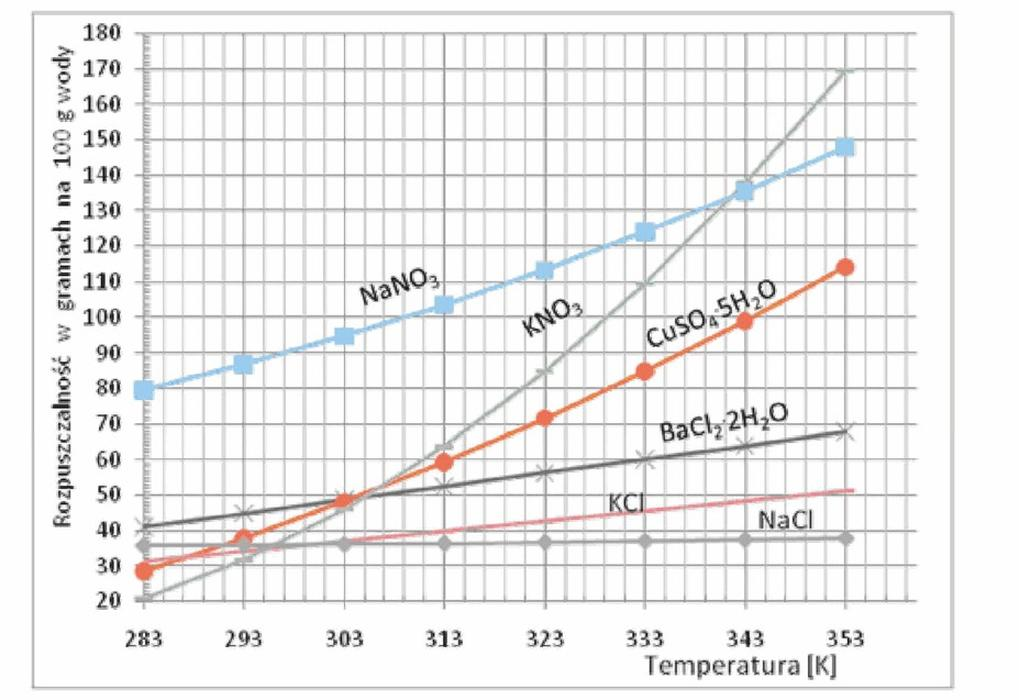
Na podstawie wykresu wskaż substancję, której rozpuszczalność rośnie najszybciej w przedziale temperatury od 10°C do 20°C.
Zestaw do filtracji pod obniżonym ciśnieniem powinien obejmować między innymi
Przeprowadzono reakcję 13 g cynku z kwasem solnym zgodnie z równaniem: Zn + 2 HCl → ZnCl2 + H2↑. Otrzymano 1,12 dm3 wodoru (w warunkach normalnych). Masy molowe to: MZn = 65 g/mol, MH = 1g/mol, MCl = 35,5g/mol. Jaka jest wydajność tego procesu?
Jakie substancje są potrzebne do uzyskania nierozpuszczalnego wodorotlenku cynku?
Czystość konkretnego odczynnika chemicznego wynosi: 99,9-99,99%. Jakiego rodzaju jest ten odczynnik?
Na rysunku przedstawiono pipetę

Na podstawie informacji zawartych w tabeli, wskaż liczbę próbek pierwotnych, które należy pobrać z partii materiału o objętości \( 100 \, \text{m}^3 \).
Wzór: \( n = 0{,}5 \cdot \sqrt{V} \)
\( V \) – objętość jednostki pobierania \( \text{m}^3 \)
\( n \) – liczba miejsc pobieranych próbek pierwotnych
Wartość \( n \) zaokrągla się do liczby całkowitej.
Minimalna liczba miejsc poboru \( n = 12 \), maksymalna \( n = 30 \)
Wskaź sprzęt laboratoryjny, który znajduje się w zestawie do filtracji pod obniżonym ciśnieniem?
Na rysunku przedstawiono przyrząd do pobierania próbek

Przebieg: Po zważeniu dwóch suchych zlewek, odważ kolejno: do jednej 3,63 g Co(NO3)2·6H2O, a do drugiej 3,75 g Na2CO3·10H2O. Następnie do obu zlewek wlej 25 cm3 gorącej wody i mieszając za pomocą bagietki doprowadź do całkowitego rozpuszczenia soli. Do roztworu Co(NO3)2 dodaj gorący roztwór Na2CO3 podczas mieszania. Otrzymany roztwór schłodź w łaźni wodnej z 3 kostkami lodu do temperatury pokojowej. Schłodzony roztwór przefiltruj przy użyciu zestawu do sączenia pod próżnią. Osad na lejku przepłucz wodą destylowaną, aż osiągnie obojętny odczyn przesączu. Przesączony osad osusz z sączkiem międzyposiadającym złożone arkusze bibuły w temperaturze pokojowej. Po wyschnięciu osad zważ i oblicz wydajność. Określ, jaki czynnik wpływa na skład jakościowy uzyskanego węglanu kobaltu(II)?
Najskuteczniejszą techniką separacji ketonu oraz kwasu karboksylowego obecnych w roztworze benzenowym jest
Przedstawiony sposób dotyczy pobierania próbki wody do przeprowadzenia badań
| Sposób pobierania próbki wody do przeprowadzenia badań: - próbki pobrać do sterylnych butelek; - przed przystąpieniem do pobierania wody zdjąć z kurka wszelkie urządzenia, zeskrobać zanieczyszczenia, następnie całkowicie otwierając i zamykając zawór, wielokrotnie płukać; - metalowy kurek wysterylizować płomieniem, a kurek z tworzywa sztucznego alkoholem etylowym; - kurek otworzyć do połowy przepływu i spuszczać wodę przez około 2-3 minuty do osiągnięcia stałej temperatury; - pobrać próbkę wody napełniając butelkę do około ¾ objętości i natychmiast zamknąć korkiem. |
Aby odróżnić urządzenia w laboratorium chemicznym, rury do próżni maluje się w kolorze
Etykiety chemikaliów zawierają zwroty H, które informują o rodzaju zagrożenia. Cyfra "3" pojawiająca się po literze "H" w oznaczeniu, definiuje rodzaj zagrożenia?
Z uwagi na higroskopijne właściwości tlenku fosforu(V) powinien on być przechowywany w warunkach bez dostępu
Aby podnieść stężenie mikroelementów w roztworze, próbkę należy poddać
Technika kwartowania (ćwiartkowania) pozwala na redukcję masy próbki ogólnej
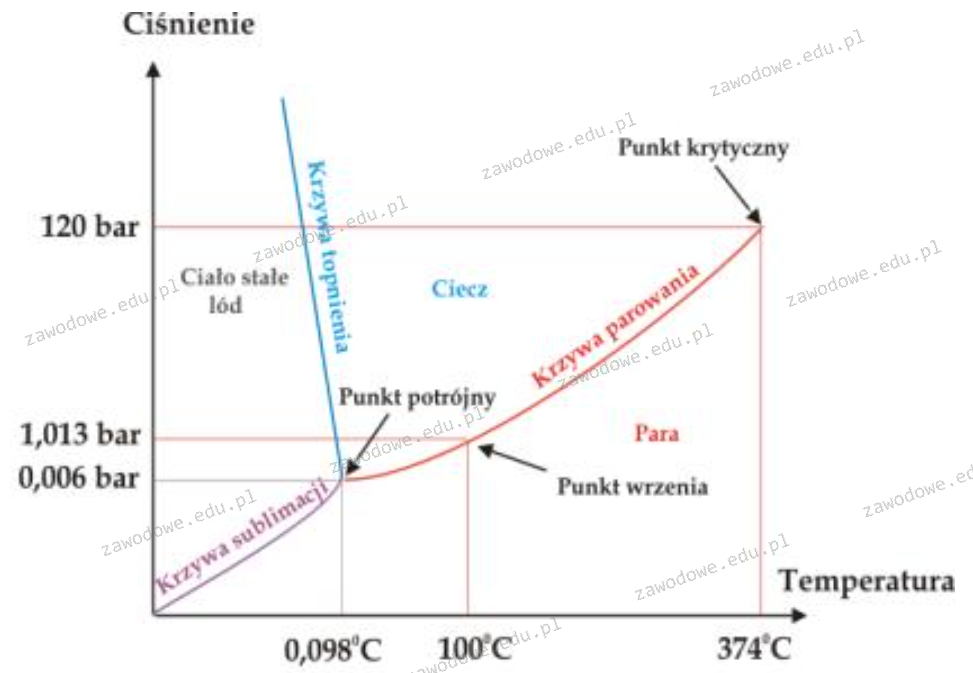
Korzystając z wykresu wskaż, w jakiej postaci występuje woda w temperaturze 10°C i pod ciśnieniem 100 barów.
Na podstawie danych zawartych w tabeli wskaż, który dodatek należy zastosować, w celu konserwacji próbek wody przeznaczonych do oznaczania jej twardości.
| Tabela. Techniki konserwacji próbek wody | |
|---|---|
| Stosowany dodatek lub technika | Rodzaje próbek, do których dodatek lub technika jest stosowana |
| Kwas siarkowy(VI) | zawierające węgiel organiczny, oleje lub tłuszcze, przeznaczone do oznaczania ChZT, zawierające aminy lub amoniak |
| Kwas azotowy(V) | zawierające związki metali |
| Wodorotlenek sodu | zawierające lotne kwasy organiczne lub cyjanki |
| Chlorek rtęci(II) | zawierające biodegradowalne związki organiczne oraz różne formy azotu i fosforu |
| Chłodzenie w temperaturze 4°C | zawierające mikroorganizmy, barwę, zapach, organiczne formy węgla, azotu i fosforu, przeznaczone do określenia kwasowości, zasadowości oraz BZT |
Proces przesiewania próbki prowadzi się za pomocą urządzenia przedstawionego na rysunku

Korzystając z wykresu określ, której substancji można rozpuścić najwięcej w temperaturze 30°C.
Metodą, która nie służy do utrwalania próbek wody, jest
Z podanych w tabeli danych wybierz sprzęt potrzebny do zmontowania zestawu do destylacji z parą wodną.
| 1 | 2 | 3 | 4 | 5 |
| manometr | kociołek miedziany | chłodnica powietrzna | kolba destylacyjna | odbieralnik |
Ze względu na czystość, substancja oznakowana zamieszczoną etykietą powinna być wykorzystywana głównie do

W tabeli zamieszczono temperatury wrzenia niektórych składników powietrza. Na podstawie tych danych podaj, który ze składników oddestyluje jako ostatni.
| Temperatura wrzenia °C | Składniki |
|---|---|
| -245,9 | Neon |
| -182,96 | Tlen |
| -195,8 | Azot |
| -185,7 | Argon |
Procedura przygotowania roztworu Zimmermana-Reinharda
70 g MnSO4·10H2O rozpuścić w 500 cm3 wody destylowanej, dodając ostrożnie 125 cm3 stężonego H2SO4 i 125 cm3 85% H3PO4, ciągle mieszając. Uzupełnić wodą destylowaną do objętości 1dm3.
Który zestaw ilości odczynników jest niezbędny do otrzymania 0,5 dm3 roztworu Zimmermana-Reinharda, zgodnie z podaną procedurą?
| MnSO4·10H2O [g] | Stężony H2SO4 [cm3] | 85% H3PO4 [cm3] | Woda destylowana [cm3] | |
|---|---|---|---|---|
| A. | 35 g | 62,5 cm3 | 62,5 cm3 | ok. 370 cm3 |
| B. | 35 g | 62,5 cm3 | 62,5 cm3 | ok. 420 cm3 |
| C. | 70 g | 125 cm3 | 125 cm3 | ok. 500 cm3 |
| D. | 70 g | 125 cm3 | 125 cm3 | ok. 800 cm3 |
Aby zebrać próbki gazów, wykorzystuje się
Sprzęt laboratoryjny przedstawiony na ilustracji stanowi element zestawu do

Połączono równe ilości cynku i bromu, a następnie poddano je reakcji Zn + Br2 → ZnBr2. W tych warunkach stopień reakcji cynku wynosi (masy atomowe: Zn – 65u, Br – 80u)?
Wskaż zbiór substancji, które po rozpuszczeniu w wodzie stają się elektrolitami?
Po zmieszaniu wszystkie pierwotne próbki danej partii materiału tworzą próbkę
Jaką metodę wykorzystuje się w laboratorium do rozdzielenia osadu AgCl od cieczy macierzystej w probówkach?
Jakiego odczynnika chemicznego, oprócz Na2Cr2O7, należy użyć do sporządzenia mieszaniny chromowej do czyszczenia sprzętu szklarskiego w laboratorium?