Pytanie 1
Czas połowicznego zaniku jest wykorzystywany
Wynik: 31/40 punktów (77,5%)
Wymagane minimum: 20 punktów (50%)
Czas połowicznego zaniku jest wykorzystywany
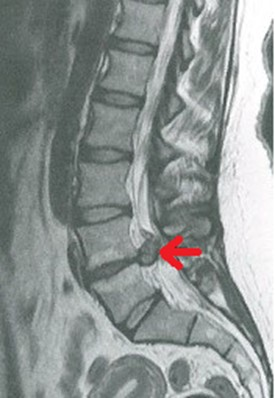
Na obrazie MR kręgosłupa lędźwiowego strzałką wskazano
Brachyterapia polega na napromieniowaniu pacjenta promieniowaniem
W radiografii mianem SID określa się
Do środków kontrastujących negatywnych należą
Pomiar densytometryczny BMD metodą DXA z kręgosłupa powinien obejmować kręgi
Które ciało obce w obszarze badania nie stanowi przeciwwskazania do wykonania MR?
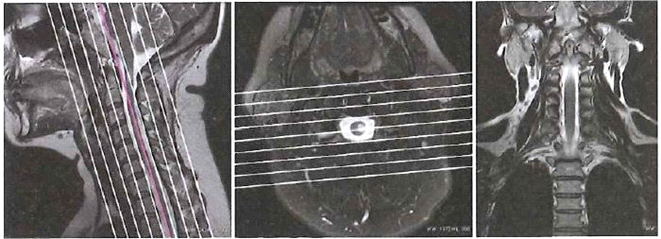
Obrazy MR kręgosłupa szyjnego przedstawiają etap planowania badania warstw
W celu unieruchomienia okolicy badanej podczas wykonywania zdjęcia nadgarstka u osoby dorosłej należy zastosować
Diagnozowanie metodą PET oparte jest na zjawisku
Zgodnie ze standardami do wykonania zdjęcia bocznego czaszki, należy zastosować kasetę o wymiarze
Glukoza podawana pacjentowi w badaniu PET jest znakowana radioaktywnym
Kryterium rozpoznawczym dla fali δ (delta) w badaniu EKG jest
Fistulografia to badanie kontrastowe
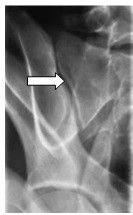
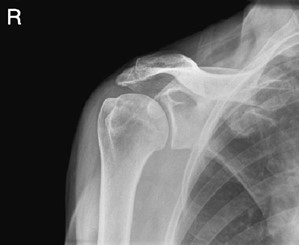
Którą strukturę anatomiczną zaznaczono strzałką na rentgenogramie?
W zapisie EKG linia izoelektryczna obrazuje
Promieniowanie jonizujące pośrednio to
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
Audiometria impedancyjna polega na pomiarze
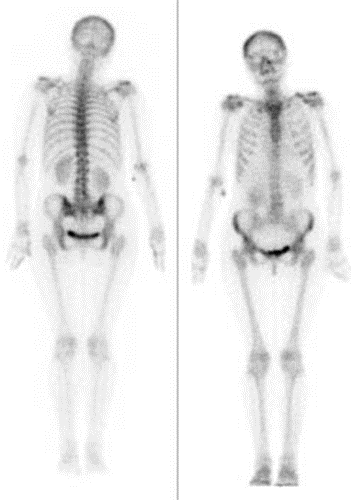
Scyntygrafia kości „whole body” jest wskazana podczas diagnostyki
Miejscem wykonania pomiaru densytometrycznego z kości przedramienia jest
Przedstawiony obraz został zarejestrowany podczas wykonania
Który środek kontrastujący stosuje się w badaniu metodą rezonansu magnetycznego?
Która sekwencja w obrazowaniu MR jest stosowana do uwidocznienia naczyń krwionośnych?
Na radiogramie uwidoczniono
Zwiększenie napięcia na lampie rentgenowskiej powoduje
Radiofarmaceutyki stosowane w medycynie nuklearnej powstają dzięki połączeniu radioizotopu
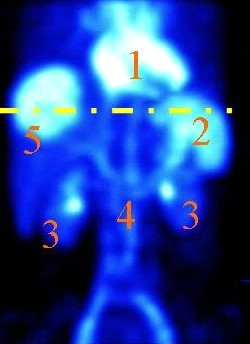
Który narząd na obrazie scyntygrafii znakowanej erytrocytami zaznaczono cyfrą 2?
Elementem pomocniczym w radioterapii, zapewniającym powtarzalność ułożenia w pozycji terapeutycznej, a także unieruchomienie pacjenta, jest
Bezwzględnym przeciwwskazaniem do badania spirometrycznego jest
Do czego służy do symulator rentgenowski wykorzystywany w procesie radioterapii?
Lordoza to fizjologiczna krzywizna kręgosłupa występująca
W radiografii mianem SID określa się
Podczas wykonywania zdjęcia rentgenowskiego lewobocznego czaszki promień centralny powinien przebiegać
Wskaż roczną dawkę graniczną dla osób zatrudnionych w warunkach narażenia na promieniowanie jonizujące.
Gruboziarnista folia wzmacniająca wpływa na zwiększenie na obrazie rentgenowskim nieostrości
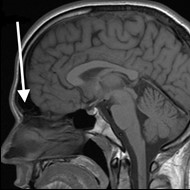
Na obrazie rezonansu magnetycznego głowy strzałką wskazano zatokę
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Podczas teleradioterapii piersi lewej narządem krytycznym jest
Wskazaniem do zastosowania brachyterapii w leczeniu radykalnym jest rak