Pytanie 1
Aby uzyskać Cr2O3, dichromian(VI) amonu został poddany rozkładowi. Po rozpoczęciu, egzotermiczna reakcja rozkładu przebiega samorzutnie.
(NH4)2Cr2O7 → Cr2O3 + 4 H2O + N2 Jak oceniasz zakończenie tej reakcji?
Wynik: 31/40 punktów (77,5%)
Wymagane minimum: 20 punktów (50%)
Aby uzyskać Cr2O3, dichromian(VI) amonu został poddany rozkładowi. Po rozpoczęciu, egzotermiczna reakcja rozkładu przebiega samorzutnie.
(NH4)2Cr2O7 → Cr2O3 + 4 H2O + N2 Jak oceniasz zakończenie tej reakcji?
Jakim przyrządem nie jest możliwe określenie gęstości cieczy?
Do przechowywania stężonego kwasu azotowego(V) w laboratorium należy stosować:
Jaką masę chlorku sodu można znaleźć w 150 g roztworu soli o stężeniu 5% (m/m)?
Podaj nazwę reagentu chemicznego, który w specyficznych warunkach reaguje tylko z jednym jonem, pierwiastkiem lub związkiem chemicznym?
Które spośród substancji wymienionych w tabeli pozwolą pochłonąć wydzielający się tlenek węgla(IV)?
| I | II | III | IV | V |
|---|---|---|---|---|
| Ca(OH)2(aq) | NaOH(s) | HNO3(stęż) | CuO(s) | CaO(s) |
Laboratoryjny aparat szklany, który wykorzystuje kwasy do wytwarzania gazów w reakcji z metalem lub odpowiednią solą, to
Odczynnik, który nie został wykorzystany, należy zutylizować zgodnie z informacjami zawartymi na etykiecie
Po przeprowadzeniu krystalizacji z 120 g kwasu szczawiowego uzyskano 105 g produktu o wysokiej czystości. Jaki był poziom zanieczyszczeń w kwasie szczawiowym?
W laboratorium chemicznym przewody instalacji rurowych są oznaczane różnymi kolorami, zgodnie z obowiązującymi normami. Polska Norma PN-70 N-01270/30 określa kolor dla wody jako
Na opakowaniu fenolu umieszcza się przedstawiony na rysunku znak ostrzegawczy, który oznacza, że jest to substancja

Na rysunku przedstawiono urządzenie stosowane do pobierania próbek
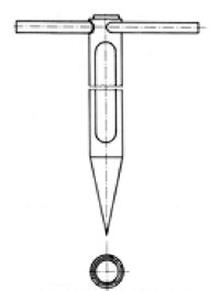
Jakie czynniki wpływają na zmiany jakościowe w składzie próbki?
Na podstawie danych zawartych w tabeli wskaż, które opakowania zawierają produkt zgodny ze specyfikacją.
| WŁAŚCIWOŚCI | NORMA KLASY A wg specyfikacji produktu | OPAKOWANIE | ||
|---|---|---|---|---|
| 1 | 2 | 3 | ||
| POSTAĆ | Bezbarwna ciecz, bez zanieczyszczeń. Dopuszcza się niebieskawе zabаrwienie i obecność skrystalizowanego osadu | Bezbarwna ciecz | ||
| Zawartość ługu sodowego (NaOH), min, % masy | 46,0 | 46,5 | 46,8 | 48,0 |
| Węglan sodu (Na₂CO₃), nie więcej niż, % masy | 0,4 | 0,3 | 0,3 | 0,2 |
| Chlorek sodu (NaCl), nie więcej niż, % masy | 0,020 | 0,015 | 0,014 | 0,011 |
| Chloran sodu (NaClO₃), nie więcej niż, % masy | 0,007 | 0,006 | 0,005 | 0,002 |
| Siarczan sodu (Na₂SO₄), nie więcej niż, % masy | 0,040 | 0,038 | 0,035 | 0,029 |
| Zawartość żelaza (Fe₂O₃), max, WT. PPM | 15 | 15 | 15 | 10 |
Etykieta roztworu kwasu azotowego(V) o koncentracji 6 mol/dm3 powinna zawierać nazwę substancji oraz
Do pojemników na odpady stałe, które są przeznaczone do utylizacji, nie można wprowadzać bezpośrednio cyjanków oraz związków kompleksowych zawierających jony cyjankowe z powodu
Aby uzyskać całkowicie bezwodny Na2CO3, przeprowadzono prażenie 143 g Na2CO3·10H2O (M = 286 g/mol). Po upływie zalecanego czasu prażenia odnotowano utratę masy 90 g. W związku z tym prażenie należy
Które równanie przedstawia reakcję otrzymywania mydła?
| CH3COOH + NaOH →CH3COONa + H2O | 2 CH3COOH + Na2O →2 CH3COONa + H2O | 2 C2H5COOH + 2 Na →2 C2H5COONa + H2↑ | C17H35COOH + NaOH →C17H35COONa + H2O |
Do rozpuszczania próbek wykorzystuje się wodę królewską, która stanowi mieszaninę stężonych kwasów
250 cm3 roztworu kwasu octowego o stężeniu 10% objętościowych zostało rozcieńczone pięciokrotnie. Jakie jest stężenie otrzymanego roztworu?
Rysunek przedstawia

Na rysunku przedstawiono
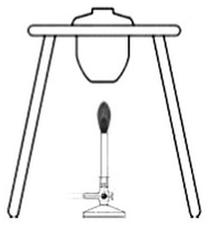
Do przechowywania zamrożonych próbek wody stosuje się naczynia wykonane
Które z poniższych równań ilustruje reakcję, w której powstają produkty gazowe?
Z uwagi na bezpieczeństwo pracy, ciecze żrące powinny być podgrzewane w łaźniach
Odpady z rozpuszczalników organicznych, takich jak benzen czy aceton, zawierające co najmniej 80% danego rozpuszczalnika, należy
Na rysunku przedstawiono przyrząd do pobierania próbek

Ustalanie miana roztworu polega na
Jakie jest pH 0,001-molowego roztworu NaOH?
Część partii pobrana w sposób jednorazowy z jednego źródła towaru zapakowanego lub z jednego opakowania jednostkowego określana jest mianem próbki
Jakie środki należy zastosować do gaszenia pożaru metali, takich jak magnez, sód czy potas?
Do metalowego sprzętu laboratoryjnego używanego w praktykach analitycznych zalicza się
Przedstawiony na rysunku zestaw służy do destylacji
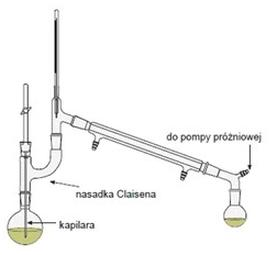
Po połączeniu 50 cm3 wody z 50 cm3 alkoholu etylowego, objętość otrzymanej mieszanki jest poniżej 100 cm3. Zjawisko to jest spowodowane
Które z poniższych działań należy wykonać przed rozpoczęciem pracy z nowym szkłem laboratoryjnym?
Wapno palone uzyskuje się poprzez prażenie wapienia według równania: CaCO3 → CaO + CO2. Ile kilogramów wapienia należy zastosować, aby w efekcie jego prażenia otrzymać 7 kg wapna palonego, jeśli wydajność reakcji wynosi 50%?
Masy molowe: MCa = 40 g/mol, MC = 12 g/mol, MO = 16 g/mol.
Z uwagi na higroskopijne właściwości tlenku fosforu(V) powinien on być przechowywany w warunkach bez dostępu
Na rysunku przedstawiono palnik gazowy
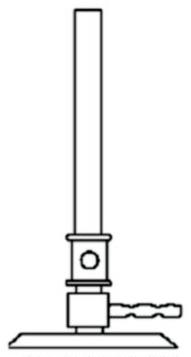
Jakim narzędziem dokonuje się poboru próbki wody?
Ile węglanu sodu trzeba odmierzyć, aby uzyskać 200 cm3 roztworu o stężeniu 8% (m/v)?