Pytanie 1
Oznaczanie jonów cynku przy użyciu EDTA stanowi przykład miareczkowania
Wynik: 19/40 punktów (47,5%)
Wymagane minimum: 20 punktów (50%)
Oznaczanie jonów cynku przy użyciu EDTA stanowi przykład miareczkowania
Zamieszczona instrukcja dotyczy wykonania preparatu mikroskopowego
| 1. Materiał nanieść na szkiełko podstawowe. 2. Po wyschnięciu, preparat utrwalić przez przeciągnięcie szkiełka podstawowego nad płomieniem palnika spirytusowego. 3. Następnie nanieść na szkiełko roztwór błękitu metylenowego i pozostawić do wyschnięcia. 4. Spłukać wodą destylowaną, pozostawić preparat do wyschnięcia. |
Zespół enzymów, obecny zarówno w organizmach roślinnych, jak i zwierzęcych, który katalizuje proces hydrolizy wiązań peptydowych w białkach oraz peptydach, to
Metalowe wskaźniki są wykorzystywane w analizach
Na zmiareczkowanie 10 cm3 NaOH zużyto 2 cm3 0,1-molowego roztworu H2SO4. Ilość wodorotlenku sodu w badanej próbce w g/100 cm3 wynosi (Na — 23 g/mol, O — 16 g/mol, H — 1 g/mol)
Jakim odczynnikiem grupowym IV grupy analitycznej kationów jest?
Jakie składniki odżywcze w żywności są identyfikowane za pomocą odczynników Fehlinga I i II?
Przedstawione reakcje zachodzą w produktach żywnościowych podczas fermentacji
| C12H22O11 + H2O → C6H12O6 + C6H12O6 |
| C6H12O6 → 2 CH3 −CH(OH) −COOH |
Rolę wskaźnika w oznaczeniu opisanym w ramce pełni
| Do kolby miarowej o pojemności 250 cm3 odpipetować 25 cm3 3% wody utlenionej i dopełnić wodą do kreski. Do kolby stożkowej o pojemności 250 cm3 odpipetować 20 cm3 próbki rozcieńczonej wody utlenionej, dodać 25 cm3 kwasu siarkowego(VI) (1+4) i miareczkować roztworem manganianu(VII) potasu o stężeniu 0,02 mol/dm3 do pojawienia się trwałego różowego zabarwienia. |
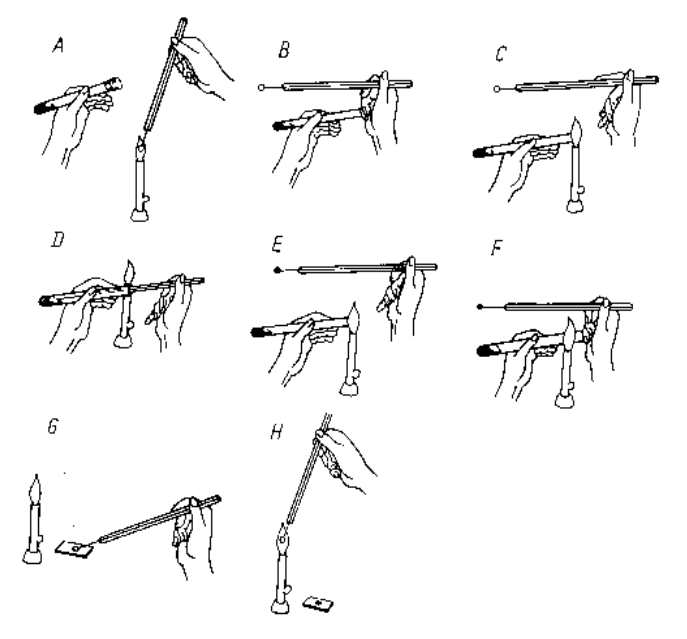
Wskaż nazwy sprzętów laboratoryjnych przedstawionych na rysunku.
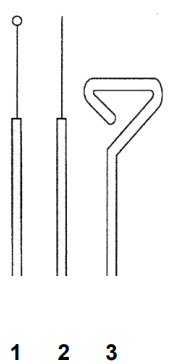
Wygięty pręt wykonany ze szkła, metalu lub plastiku, który służy do przeprowadzania posiewów na powierzchni i rozprowadzania materiału biologicznego, jest w mikrobiologii określany jako
Urządzenie, które mierzy absorpcję promieniowania elektromagnetycznego o danej długości fali przez cząsteczkę, to
Korzystając ze wzoru, oblicz zawartość tlenu (w procentach nasycenia X) w próbce wody, jeżeli stężenie rozpuszczonego w niej tlenu wynosi 7,7 mg/dm3, a temperatura wody jest równa 284 K.
| Temperatura °C | Rozpuszczalność O2 mg/dm3 |
|---|---|
| 0 | 14,64 |
| 1 | 14,22 |
| 3 | 13,44 |
| 5 | 12,74 |
| 7 | 12,11 |
| 9 | 11,53 |
| 11 | 11,00 |
| 13 | 10,53 |
| 15 | 10,08 |
| 17 | 9,66 |
| 19 | 9,27 |
| X = a · 100% b |
| gdzie: a – oznaczona zawartość tlenu rozpuszczonego w wodzie, mg/dm3 b – rozpuszczalność O2, mg/dm3 |
W wodzie poddawanej procesowi dezynfekcji mierzy się zawartość chloru wolnego. Co oznacza ten parametr?
Na etykiecie odczynnika chemicznego zawarte są następujące informacje. Z informacji wynika, że odczynnik ten może być zastosowany do sporządzenia roztworu o stężeniu około 0,1 mol/dm3 z dokładnością do
| NH4SCN amonu tiocyjanian | 0,1 mol/l |
| Stężenie po rozcieńczeniu do 1000 ml w 20°C | 0,1 mol/l ± 0,2 % |
Analiza wody basenowej w celu wykrycia bakterii polega na podgrzewaniu próbki w inkubatorze przez 48 godzin w temperaturze 36±2°C. Jaki proces jest opisany?
Aby przygotować podłoże do badań mikrobiologicznych, należy
Wykonano identyfikację opisaną w schemacie:
BaCl2 + X — biały osadJaki wzór reprezentuje substrat X?
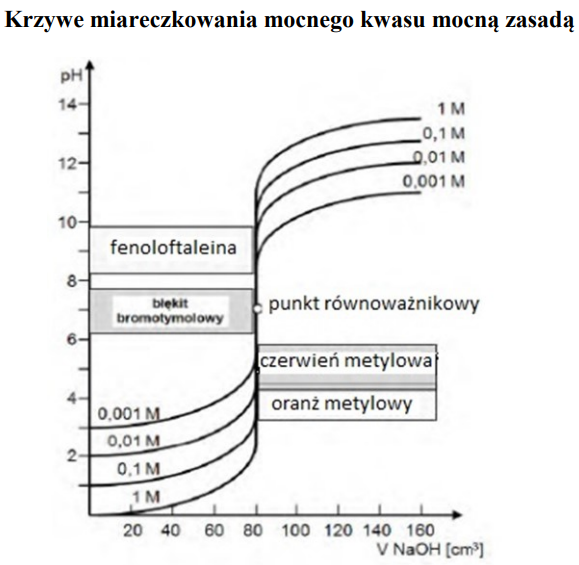
Rysunek przedstawia
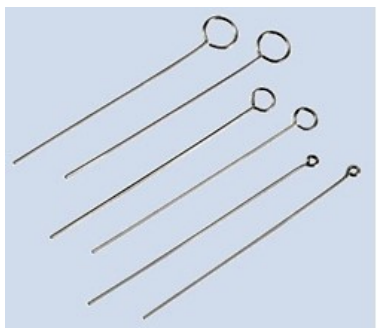
Opisana metoda miareczkowania zaliczana jest do
| Ilościowe oznaczenie cukrów polega na redukcji soli miedzi(II) roztworem cukru, a następnie dodaniu do próbki roztworu KI i odmiareczkowaniu wydzielonego jodu mianowanym roztworem tiosiarczanu sodu |
W makroanalizie wykorzystuje się próbki o ciężarze
Na rysunku przedstawiono aparat służący do badania zawartości wody w surowcach metodą
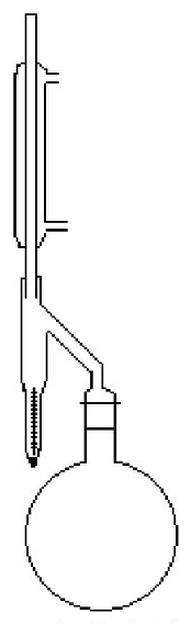
Ekstraktor przedstawiony na rysunku stosuje się do rozpuszczalników
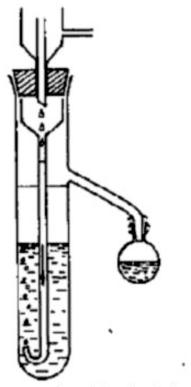
Z analizy wykresu wynika, że do miareczkowania 0,001-molowego roztworu mocnego kwasu za pomocą 0,001-molowego roztworu mocnej zasady nie można zastosować jako wskaźnika
Elektroforeza to zjawisko elektrokinetyczne, które wykorzystuje się w analizie
Zamieszczony opis definiuje wskaźniki stosowane w miareczkowaniu
| Substancje te zmieniają zabarwienie w zależności od zmiany stężenia jonów wodorowych w roztworze. Są to słabe kwasy lub zasady organiczne, których barwa niezdysocjowanej cząsteczki w roztworze wodnym różni się od barwy jonów. |
Skręcalność optyczną cukrów mierzy się przy użyciu
Podstawowe kryteria oceny jakości nafty to:
Na schemacie przedstawiającym sposób pobierania hodowli do badań ze skosu agarowego literą D oznaczono
Jaką metodę analityczną stosuje się do pomiaru przewodnictwa cieczy umieszczonej między dwiema elektrodami, do których dostarczany jest prąd zmienny?
W wodzie do picia identyfikacja stężenia jonów Fe3+ może być zrealizowana
Ogólna twardość próbki wody stosowanej w technologiach wynosi 16,5°n, a twardość węglanowa osiąga 7,2°n. Jaką wartość ma twardość stała?
Oznaczona twardość ogólna wody wynosi 2 mval/dm3. Wartość ta przeliczona na stopnie niemieckie, zgodnie z zamieszczonym przelicznikiem jednostek, wynosi
| 1 mval/dm3 – 2,8°dH (stopni niemieckich) |
W przedstawionym na rysunku urządzeniu próbki są poddawane

Próbkę tłuszczu poddano analizie, której wyniki zapisano w tabeli. Która substancja była zawarta w próbce?
| Odczynnik | Obserwacje |
|---|---|
| woda bromowa | odbarwienie wody bromowej |
Do analizy pobrano próbkę o masie 200 mg. Na podstawie informacji zamieszczonych w tabeli określ, w jakiej skali będzie wykonana ta analiza.
| Wielkość próbki | Skala analizy |
|---|---|
| > 0,1 g | makro |
| 0,01 – 0,1 g | semimikro |
| 0,0001 – 0,01 g | mikro |
| < 10-4 g | ultramikro |
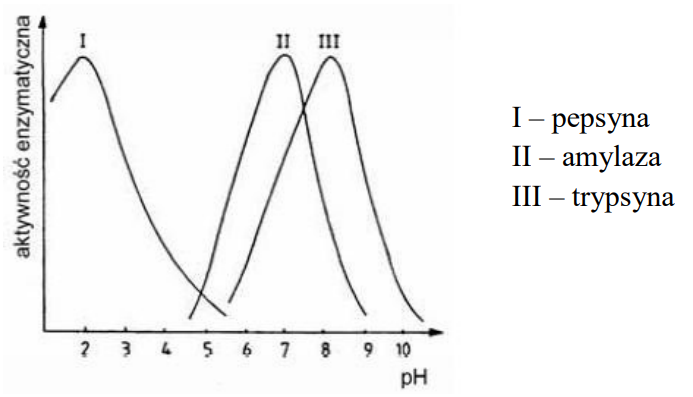
Na wykresie przedstawiono zależność aktywności enzymów od pH. Optimum aktywności amylazy występuje przy pH
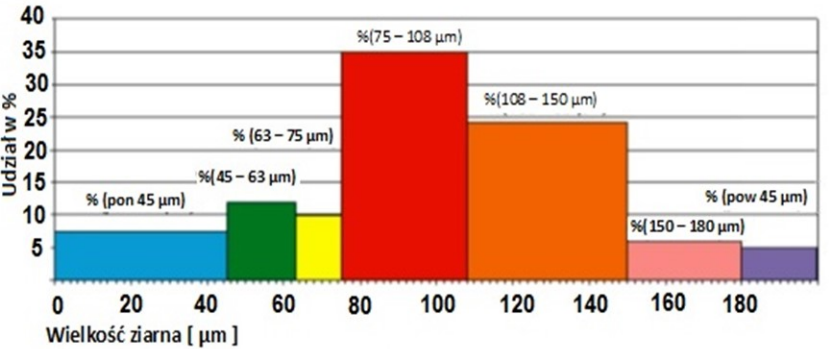
Na diagramie słupkowym przedstawiono wyniki analizy sitowej surowca w formie proszkowej. W jakiej kolejności zamontowano sita w wytrząsarce, licząc je od naczynia zbierającego?
Przyrząd, który konwertuje fizyczne lub chemiczne cechy substancji na sygnał analityczny, który można zaobserwować lub zarejestrować, to
Który z parametrów jakości wody jest nieprawidłowo opisany?
| Mętność | 0,19 NTU | |
| Barwa | Akceptowalna - 10 mg Pt/dm3 | |
| Jon amonowy | 0,15 mg NH4+/dm3 | |
| Twardość | Węglanowa | Stopnie niemieckie |
| 8,01°dH | 140 mg/dm3 | |