Pytanie 1
Jaką metodę wykorzystuje się w laboratorium do rozdzielenia osadu AgCl od cieczy macierzystej w probówkach?
Wynik: 24/40 punktów (60,0%)
Wymagane minimum: 20 punktów (50%)
Jaką metodę wykorzystuje się w laboratorium do rozdzielenia osadu AgCl od cieczy macierzystej w probówkach?
Podstawowy zestaw do filtracji, oprócz statywu i sączka, obejmuje
Butle gazowe (czasy butli) napełnione wodorem są oznaczone kolorem
Roztwór o dokładnej masie z odważki analitycznej powinien być sporządzony
W parownicy porcelanowej, w której znajduje się 2,5 g naftalenu, umieść krążek bibuły z niewielkimi otworami oraz odwrócony lejek szklany. Zatyczkę lejka zrób z korka z waty. Parownicę umieść w płaszczu grzejnym. Po delikatnym ogrzaniu parownicy, pary substancji przechodzą przez otwory w bibule i kondensują na wewnętrznych ściankach lejka... Powyższy opis dotyczy metody oczyszczania naftalenu przez
Nie należy podgrzewać cieczy w szczelnie zamkniętych pojemnikach, ponieważ
Jaki jest błąd względny pomiaru na wadze o precyzji 0,1 g dla próbki o wadze 1 g?
Jakie urządzenie jest wykorzystywane do procesu ekstrakcji?
Sprzęt laboratoryjny przedstawiony na ilustracji stanowi element zestawu do

W przypadku zanieczyszczeń szklanych naczyń osadami o charakterze nieorganicznym, takimi jak wodorotlenki, tlenki oraz węglany, do ich oczyszczania używa się
Wodę do badań mikrobiologicznych powinno się pobierać do butelek
Na podstawie informacji zawartych w tabeli określ, który parametr spośród podanych należy oznaczyć w pierwszej kolejności.
| Tabela. Sposoby utrwalania próbek wody i ścieków, miejsce analizy, dopuszczalny czas przechowywania próbek | ||||
|---|---|---|---|---|
| Oznaczany parametr | Rodzaj naczynia do przechowywania próbki | Sposób utrwalania próbki | Miejsce wykonania analizy | Dopuszczalny czas przechowywania próbki |
| Chlorki | szklane lub polietylenowe | - | laboratorium | 96 godzin |
| Chlor pozostały | szklane | - | w miejscu pobrania próbki | - |
| ChZT | szklane | zakwaszenie do pH<2, schłodzenie do temperatury 2-5°C | laboratorium | 24 godziny |
| Kwasowość | szklane lub polietylenowe | schłodzenie do temperatury 2-5°C | laboratorium | 4 godziny |
| Mangan | szklane lub polietylenowe | zakwaszenie do pH<2, schłodzenie do temperatury 2-5°C | laboratorium | 48 godziny |
W jakiej standardowej temperaturze są kalibrowane szklane naczynia pomiarowe?
W standardowym układzie destylacyjnym, który ma ukośną chłodnicę, wykorzystuje się chłodnicę
Jakie środki należy zastosować do gaszenia pożaru metali, takich jak magnez, sód czy potas?
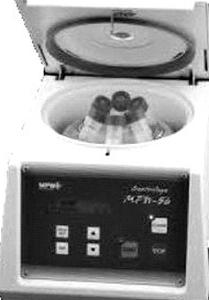
Na zdjęciu przedstawiono urządzenie służące do
Wskaź sprzęt konieczny do przeprowadzenia miareczkowania?
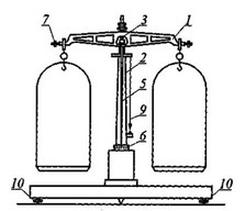
Waga przedstawiona na rysunku umożliwia ważenie substancji z dokładnością do

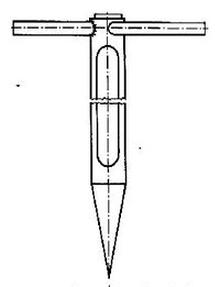
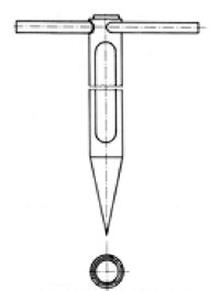
Na rysunku przedstawiono urządzenie stosowane do pobierania próbek
Aby odróżnić urządzenia w laboratorium chemicznym, rury do próżni maluje się w kolorze
Ekstrakcję w trybie ciągłym przeprowadza się
Aby obliczyć gęstość cieczy przy użyciu metody hydrostatycznej, należy zastosować
Procedura oznaczenia kwasowości mleka. Do wykonania analizy, zgodnie z powyższą procedurą, potrzebne są
| Do kolby stożkowej o pojemności 300 cm3 pobrać dokładnie 25 cm3 badanego mleka i rozcieńczyć wodą destylowaną do objętości 50 cm3. Dodać 2-3 krople fenoloftaleiny i miareczkować mianowanym roztworem wodorotlenku sodu do uzyskania lekko różowego zabarwienia. |
Aby przygotować miano kwasu solnego, konieczne jest odważenie węglanu sodu o masie wynoszącej około 400 mg. Jaką precyzję powinna mieć waga używana do odważenia węglanu sodu?
Wybierz spośród wymienionych właściwości tę, która nie dotyczy naczyń kwarcowych.
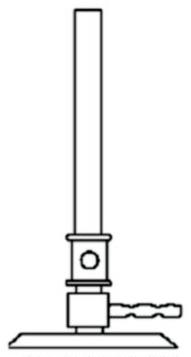
Na rysunku przedstawiono palnik gazowy
Aby uniknąć trwałego połączenia szlifowanych części sprzętu laboratoryjnego, co należy zrobić?
Średnia masa wody wypływająca z pipety o deklarowanej pojemności 25 cm3, w temperaturze 25°C wynosi 24,80 g. Korzystając z danych zamieszczonych w tabeli wskaż wartość poprawki kalibracyjnej dla tej pipety.
| Masa wody zajmującej objętość 1 dm3 w zależności od temperatury pomiaru | |
|---|---|
| Temperatura °C | Masa wody g |
| 20 | 997,17 |
| 21 | 997,00 |
| 22 | 996,80 |
| 23 | 996,59 |
| 24 | 996,38 |
| 25 | 996,16 |
| 26 | 995,93 |
| 27 | 995,69 |
| 28 | 995,45 |
| 29 | 995,18 |
| 30 | 994,92 |
Nie należy używać gorącej wody do mycia
Jaka minimalna pojemność powinna mieć miarka, aby jednorazowo zmierzyć 60,0 cm3 wody?
Na rysunku przedstawiono przyrząd do pobierania próbek

Urządzeniem pomiarowym nie jest
Rysunek przedstawia wagę techniczną. Numerem 7 oznaczono
Jak nazywa się naczynie o płaskim dnie, które wykorzystuje się do pozyskiwania substancji stałej poprzez stopniowe odparowanie rozpuszczalnika z roztworu?
Gęstość próbki cieczy wyznacza się przy użyciu
Komora przeszklona w formie dużej szafy, wyposażona w wentylator, która zapobiega wydostawaniu się szkodliwych substancji do atmosfery laboratorium oraz chroni przed pożarami i eksplozjami, to
Przy przygotowywaniu 100 cm3 roztworu o określonym stężeniu procentowym (m/V) konieczne jest odważenie wyliczonej ilości substancji, a następnie przeniesienie jej do
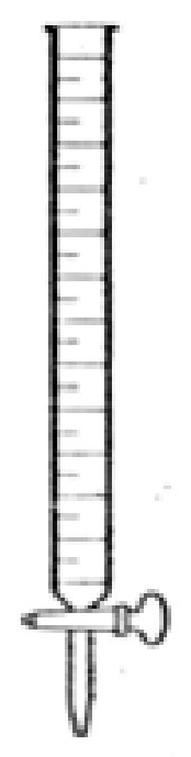
Przedstawiony sprzęt szklany to
Aby pobrać dokładnie 20 cm3 próbkę wody do przeprowadzenia analiz, należy zastosować
Przyrząd przedstawiony na rysunku służy do pobierania próbek substancji