Pytanie 1
Sączków o najmniejszych średnicach, nazywanych "twardymi" i oznaczonych kolorem niebieskim, używa się do filtracji osadów?
Wynik: 35/40 punktów (87,5%)
Wymagane minimum: 20 punktów (50%)
Sączków o najmniejszych średnicach, nazywanych "twardymi" i oznaczonych kolorem niebieskim, używa się do filtracji osadów?
Laboratoryjny aparat szklany, który wykorzystuje kwasy do wytwarzania gazów w reakcji z metalem lub odpowiednią solą, to
Waga przedstawiona na rysunku umożliwia ważenie substancji z dokładnością do

Jaką metodą nie można rozdzielać mieszanin?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Podczas analizowania zmienności składu wód płynących w skali rocznej, próbki wody powinny być zbierane i badane przynajmniej raz na
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Jakie jest stężenie roztworu HNO3, który powstał w wyniku połączenia 50 cm3 roztworu HNO3 o stężeniu 0,2 mol/dm3 oraz 25 cm3 roztworu HNO3 o stężeniu 0,5 mol/dm3?
Aby oddzielić połączenia szlifów, należy w miejscu ich styku wprowadzić
Którego z poniższych naczyń laboratoryjnych nie powinno się używać do podgrzania 100 cm3wody?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
W jakim celu używa się kamyczków wrzenne w trakcie długotrwałego podgrzewania cieczy?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Z próbek przygotowuje się ogólną próbkę
Aby rozpuścić próbkę tłuszczu o wadze 5 g, wykorzystuje się 50 cm3 mieszanki 96% alkoholu etylowego oraz eteru dietylowego, połączonych w proporcji objętościowej 1 : 2. Jakie ilości cm3 każdego ze składników są potrzebne do przygotowania 150 cm3 tej mieszanki?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Aby poprawić efektywność reakcji opisanej równaniem: HCOOH + C2H5OH ⇄ HCOOC2H5 + H2O, należy
Związki chromu(VI) oddziałują negatywnie na środowisko, ponieważ
Oblicz stężenie molowe 250 cm3 roztworu NaOH, w którym znajduje się 0,5 g substancji. Masa molowa NaOH wynosi 40 g/mol
Do 300 g wody o temperaturze 30oC dodano 120 g substancji, co zaowocowało powstaniem roztworu nasyconego. Jaką ma rozpuszczalność ta substancja w temperaturze 30oC?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Na podstawie informacji zawartych w tabeli, wskaż liczbę próbek pierwotnych, które należy pobrać z partii materiału o objętości \( 100 \, \text{m}^3 \).
Wzór: \( n = 0{,}5 \cdot \sqrt{V} \)
\( V \) – objętość jednostki pobierania \( \text{m}^3 \)
\( n \) – liczba miejsc pobieranych próbek pierwotnych
Wartość \( n \) zaokrągla się do liczby całkowitej.
Minimalna liczba miejsc poboru \( n = 12 \), maksymalna \( n = 30 \)
W tabeli zestawiono objętości molowe czterech gazów odmierzone w warunkach normalnych.
Dla którego spośród wymienionych w tabeli gazów objętość molowa najbardziej odchyla się od wartości obliczonej dla gazu doskonałego?
| Gaz | SO2 | CHCl3(para) | O3 | NH3 |
|---|---|---|---|---|
| Objętość molowa (dm3/mol) | 21,89 | 22,60 | 21,6 | 22,08 |
Aby uzyskać sole sodowe fenoli, należy stopić dany fenol z sodą (M = 106 g/mol), stosując 10% nadmiar w porównaniu do ilości stechiometrycznej, według równania:
2 ArOH + Na2CO3 → 2 ArONa + H2O + CO2 Ile sody jest wymagane do reakcji z 7,2 g 2-naftolu (M = 144 g/mol)?
Jakie procedury powinny być stosowane podczas ustalania miana roztworu?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Który z poniższych czynników nie mógł przyczynić się do błędnego określenia całkowitej liczby drobnoustrojów w surowym mleku?
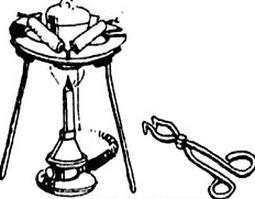
Przedstawiony zestaw stosowany jest w laboratorium do przeprowadzenia procesu
W tabeli przestawiono dane dotyczące wybranych roztworów wodnych wodorotlenku sodu.
Oblicz masę wodorotlenku sodu, jaką należy rozpuścić w 200,0 cm3 wody, aby otrzymać roztwór o gęstości 1,0428 g/cm3.
| d420 [g/cm3] | masa NaOH [g/100 cm3] |
|---|---|
| 1,0095 | 1,01 |
| 1,0207 | 2,04 |
| 1,0428 | 4,17 |
| 1,0648 | 6,39 |
| 1,0869 | 8,70 |
| 1,1089 | 11,09 |
Z etykiety wynika, że dany związek mógł być

Jakie zestawienie sprzętu laboratoryjnego wykorzystuje się do filtracji osadów?
Aby uzyskać drobnokrystaliczny osad BaSO4, należy wykonać poniższe kroki:
Do zlewki wlać 20 cm3 roztworu BaCl2, następnie dodać 100 cm3 wody destylowanej oraz kilka kropli roztworu HCl. Zawartość zlewki podgrzać na łaźni wodnej, a potem, ciągle mieszając, dodać 35 cm3 roztworu H2SO4.
Mieszaninę ogrzewać na łaźni wodnej przez 1 godzinę. Osad odsączyć i przepłukać kilkakrotnie gorącą wodą zakwaszoną kilkoma kroplami roztworu H2SO4.
Według przedstawionej procedury, do uzyskania osadu BaSO4 potrzebne są:
Chemikalia, dla których upłynął okres przydatności,
W którym z podanych równań reakcji dochodzi do zmiany stopni utlenienia atomów?
W jakim stosunku objętościowym należy połączyć roztwór o stężeniu 5 mol/dm3 z wodą destylowaną, aby uzyskać roztwór o stężeniu 3 mol/dm3?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Jak definiuje się próbkę wzorcową?