Pytanie 1
Piktogram nie jest konieczny dla
Wynik: 24/40 punktów (60,0%)
Wymagane minimum: 20 punktów (50%)
Piktogram nie jest konieczny dla
Substancje utleniające opisuje piktogram

Jaką masę wodorotlenku potasu trzeba odważyć, żeby przygotować 500 cm3 roztworu o stężeniu 0,02 mola? Masy molowe poszczególnych pierwiastków wynoszą: potas K - 39 g/mol, tlen O - 16 g/mol, wodór H - 1 g/mol?
W laboratorium chemicznym systemy wodne zazwyczaj oznacza się kolorem zielonym
Z analizy wykresu wynika, że substancją o najniższej rozpuszczalności w wodzie w temperaturze 100°C jest
Oddzielanie płynnej mieszaniny wieloskładnikowej poprzez odparowanie, a następnie skraplanie jej komponentów, to proces
Aby odcedzić galaretowaty osad, konieczne jest użycie sączka
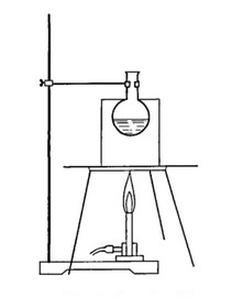
Na rysunku przedstawiono ogrzewanie kolby z cieczą w łaźni
Odważka analityczna wodorotlenku sodu, przygotowana fabrycznie, zawiera 0,1 mola NaOH. Jaką objętość wody destylowanej należy dodać w kolbie miarowej, aby uzyskać roztwór wodorotlenku sodu o stężeniu 0,0500 mol/dm3?
Zastosowanie łaźni wodnej nie jest zalecane w trakcie prac, w których stosuje się
50 cm3 alkoholu etylowego zmieszano w kolbie miarowej z 50 cm3 wody. W wyniku zjawiska kontrakcji objętość otrzymanego roztworu wyniosła 97,5 cm3. Ile wynosi stężenie procentowe (v/v) roztworu alkoholu w wodzie po zmieszaniu i stężenie procentowe roztworu alkoholu (v/v) po uzupełnieniu kolby wodą do 100 cm3?
| Stężenie procentowe (v/v) roztworu alkoholu w wodzie po zmieszaniu | Stężenie procentowe (v/v) roztworu alkoholu po uzupełnieniu kolby wodą do 100 cm3 | |
|---|---|---|
| A. | 49,2% | 48,0% |
| B. | 50,0% | 49,7% |
| C. | 51,3%, | 50,0% |
| D. | 53,3% | 50,2% |
Po połączeniu 50 cm3 wody z 50 cm3 alkoholu etylowego, objętość otrzymanej mieszanki jest poniżej 100 cm3. Zjawisko to jest spowodowane
Przedstawiony sposób dotyczy pobierania próbki wody do przeprowadzenia badań
| Sposób pobierania próbki wody do przeprowadzenia badań: - próbki pobrać do sterylnych butelek; - przed przystąpieniem do pobierania wody zdjąć z kurka wszelkie urządzenia, zeskrobać zanieczyszczenia, następnie całkowicie otwierając i zamykając zawór, wielokrotnie płukać; - metalowy kurek wysterylizować płomieniem, a kurek z tworzywa sztucznego alkoholem etylowym; - kurek otworzyć do połowy przepływu i spuszczać wodę przez około 2-3 minuty do osiągnięcia stałej temperatury; - pobrać próbkę wody napełniając butelkę do około ¾ objętości i natychmiast zamknąć korkiem. |
Aby przygotować zestaw do filtracji, należy zebrać
Destylacja to metoda
Jak nazywa się proces, w którym następuje wytrącenie ciała stałego z przesyconego roztworu w wyniku spadku temperatury?
W próbkach obecne są składniki, które znacznie różnią się pod względem zawartości. Składnik, którego procentowy udział w próbce jest niższy od 0,01%, nazywamy
Na etykiecie kwasu siarkowego(VI) znajduje się zapis:
Określ gęstość kwasu siarkowego(VI).
KWAS SIARKOWY MIN. 95% CZ.D.A. H2SO4 M = 98,08 g/mol 1 l – 1,84 kg |
Aby w badanej próbie w trakcie zmiany pH nastąpiła zmiana barwy na malinową, należy użyć
| Zmiany barw najważniejszych wskaźników kwasowo-zasadowych | ||||
|---|---|---|---|---|
| Wskaźnik | Barwa w środowisku | Zakres pH zmiany barwy | ||
| Kwasowym | Obojętnym | Zasadowym | ||
| oranż metylowy | czerwona | żółta | żółta | 3,2÷4,4 |
| lakmus (mieszanina substancji) | czerwona | fioletowa | niebieska | 4,5÷8,2 |
| fenoloftaleina | bezbarwna | bezbarwna | malinowa | 8,2÷10,0 |
| wskaźnik uniwersalny (mieszanina substancji) | czerwona (silnie kwaśne) pomarańczowa (słabo kwaśne) | żółta | niebieska (silnie zasadowe) zielona (słabo zasadowe) | co jeden stopień skali |
| herbata | żółta | czerwona-brunatna | brązowa | |
| sok z czerwonej kapusty | fioletowa | niebieska | zielona | |
Rysunek przedstawia

Naczynia z roztworem kwasu siarkowego(VI) o dużym stężeniu nie powinny być pozostawiane otwarte nie tylko za względów bezpieczeństwa, ale także dlatego, że kwas
Oblicz stężenie molowe 250 cm3 roztworu NaOH, w którym znajduje się 0,5 g substancji. Masa molowa NaOH wynosi 40 g/mol
Do narzędzi pomiarowych zalicza się
Zgodnie z danymi zawartymi w tabeli wskaźników roztwór obojętny będzie miał barwę
| Wskaźnik | Zakres zmiany barwy (w jednostkach pH) | Barwa w środowisku | |
|---|---|---|---|
| kwaśnym | zasadowym | ||
| błękit tymolowy | 1,2 – 2,8 | czerwona | żółta |
| oranż metylowy | 3,1 – 4,4 | czerwona | żółta |
| czerwień metylowa | 4,8 – 6,0 | czerwona | żółta |
| czerwień chlorofenolowa | 5,2 – 6,8 | żółta | czerwona |
| błękit bromotymolowy | 6,0 – 7,6 | żółta | niebieska |
| czerwień fenolowa | 6,6 – 8,0 | żółta | czerwona |
| błękit tymolowy | 8,0 – 9,6 | żółta | niebieska |
| fenoloftaleina | 8,2 – 10,0 | bezbarwna | czerwona |
| żółcień alizarynowa | 10,1 – 12,0 | żółta | zielona |
Dokonano pomiaru pH dwóch roztworów, uzyskując wartości pH= 2 oraz pH= 5. Wskaźnij poprawnie sformułowany wniosek.
Aby uzyskać Cr2O3, dichromian(VI) amonu został poddany rozkładowi. Po rozpoczęciu, egzotermiczna reakcja rozkładu przebiega samorzutnie.
(NH4)2Cr2O7 → Cr2O3 + 4 H2O + N2 Jak oceniasz zakończenie tej reakcji?
Który z poniższych czynników nie mógł przyczynić się do błędnego określenia całkowitej liczby drobnoustrojów w surowym mleku?
Którą substancję można bezpośrednio wyrzucić do odpadów komunalnych?
Oblicz, ile moli gazu można zebrać w pipecie gazowej o pojemności 500 cm3, jeśli gaz będzie gromadzony w warunkach normalnych. (W normalnych warunkach jeden mol gazu ma objętość 22,4 dm3)
Aby ustalić miano roztworu wodnego NaOH, należy zastosować
Jakie metody można zastosować do rozdzielania i koncentracji składników próbki?
Aby otrzymać roztwór AgNO3 (masa molowa AgNO3 to 169,8 g/mol) o stężeniu 0,1 mol/dm3, należy
Sprzęt laboratoryjny przedstawiony na ilustracji stanowi element zestawu do

Jakie urządzenie jest wykorzystywane do oczyszczania próbki gazowej?
Roztwory o ściśle określonym stężeniu, używane w analizach miareczkowych, nazywamy
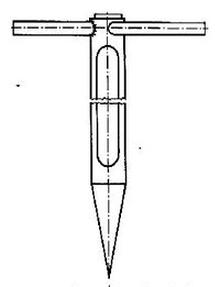
Przyrząd przedstawiony na rysunku służy do pobierania próbek substancji
Ile gramów 80% kwasu mrówkowego trzeba zważyć, aby uzyskać 200 g 20% roztworu tego kwasu?
Ze względu na czystość, substancja oznakowana zamieszczoną etykietą powinna być wykorzystywana głównie do

Ustalanie miana roztworu polega na
Zgodnie z zasadami BHP w laboratorium, po zakończeniu pracy z odczynnikami chemicznymi należy: