Pytanie 1
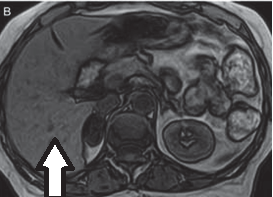
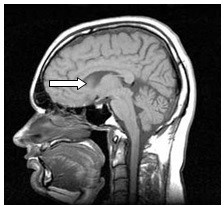
Którą strukturę anatomiczną oznaczono na zamieszczonym obrazie rezonansu magnetycznego?
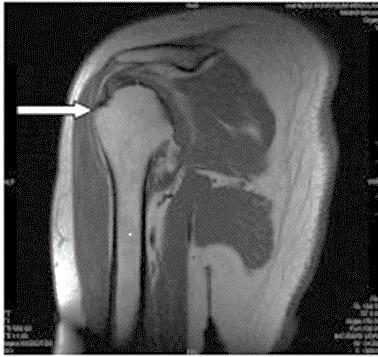
Wynik: 22/40 punktów (55,0%)
Wymagane minimum: 20 punktów (50%)
Którą strukturę anatomiczną oznaczono na zamieszczonym obrazie rezonansu magnetycznego?

Nieostrość geometryczna obrazu rentgenowskiego zależy od
Obrazy DDR są tworzone w trakcie
Która właściwość promieniowania X pozwala na skierowanie promienia centralnego na wybrany punkt topograficzny podczas wykonywania badania radiologicznego?
Przy ułożeniu do zdjęcia kręgów szyjnych CIII-CVII w projekcji przednio-tylnej lampa może być odchylona o kąt
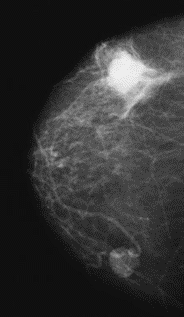
Na którym obrazie rentgenowskim sutka uwidoczniono zmianę patologiczną w obrębie węzłów chłonnych?
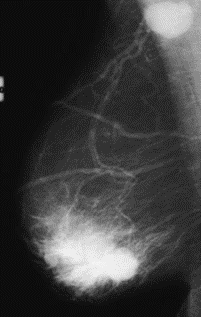
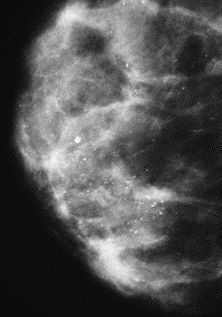
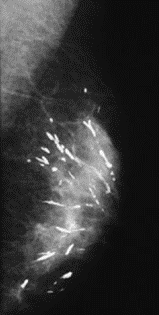
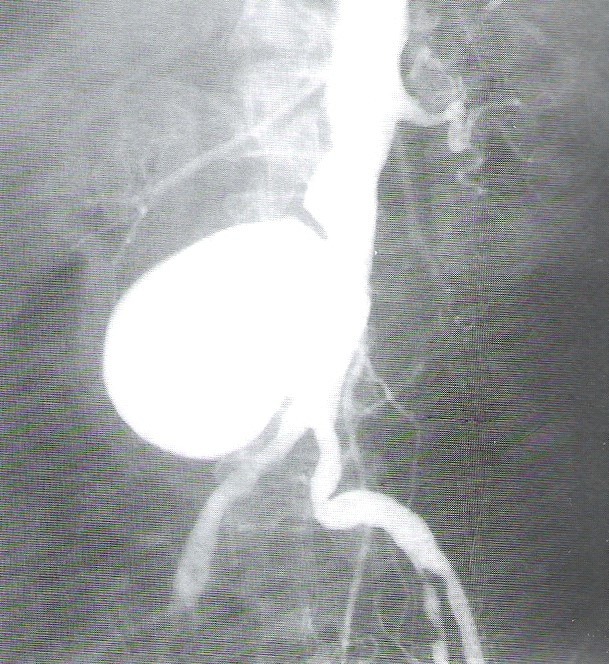
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
Jaki czas należy ustawić do wykonania zdjęcia rentgenowskiego dwójki górnej lewej?
| Tabela ekspozycji | |||
|---|---|---|---|
| wartości | czasu (s) | napięcia (kV) | natężenia (mA) |
| zęby przedtrzonowe i kły | 0,160 | 60 | 8 |
| siekacze | 0,120 | 60 | 8 |
| zęby trzonowe | 0,200 | 60 | 8 |
| ekspozycja zgryzowo-skrzydełkowa | 0,180 | 66 | 6 |
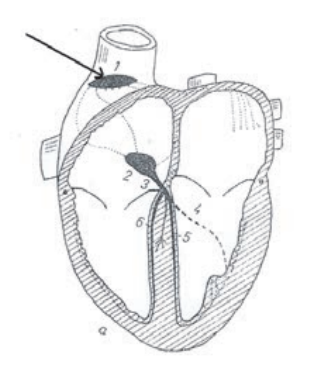
Na obrazie rentgenowskim strzałką zaznaczono
Jaka jest standardowa odległość OF do wykonania rentgenowskich zdjęć kości i stawów kończyny górnej?
Dobierz dla standardowego pacjenta projekcję, pozycję i sposób ułożenia kasety o wymiarach 30 cm x 40 cm do zdjęcia przeglądowego układu moczowego.
| Projekcja | Pozycja | Ułożenie kasety | |||
|---|---|---|---|---|---|
| 1. | AP | 3. | stojąca | 5. | poprzeczne |
| 2. | PA | 4. | leżąca | 6. | podłużne |
Zgodnie ze standardami do wykonania zdjęcia bocznego czaszki, należy zastosować kasetę o wymiarze
Do podstawowych projekcji stosowanych w diagnostyce mammograficznej należą
Strzałką na schemacie oznaczono
Po podaniu kontrastu obraz zmian nowotworowych w badaniu MR najlepiej uwidacznia się w sekwencji
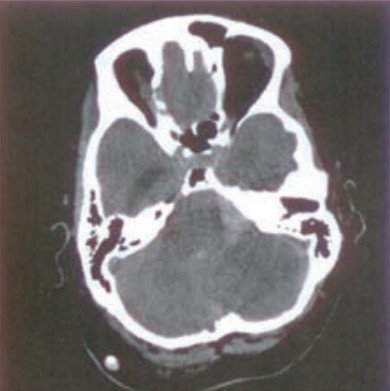
Świeżo wynaczyniona krew na obrazach TK głowy bez podania środka kontrastowego ukazuje się jako obszar
Cholangiografia to badanie radiologiczne
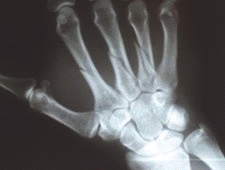
Na radiogramie uwidoczniono złamanie
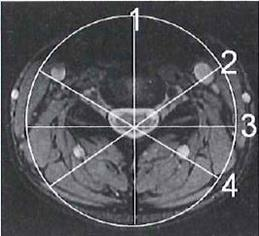
Na przekroju poprzecznym rezonansu magnetycznego strzałką oznaczono
Rozpraszanie promieniowania X, w wyniku którego następuje zwiększenie długości fali promieniowania, to zjawisko
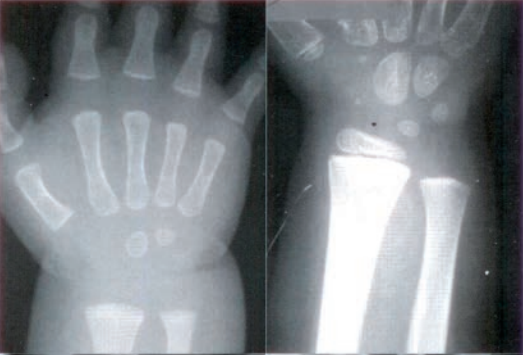
Zestaw rentgenogramów przedstawia
Skrótem CTV w radioterapii oznacza się
Badanie polegające na wprowadzeniu cewnika przez pęcherz moczowy do moczowodu i miedniczki nerkowej i podaniu środka kontrastującego to
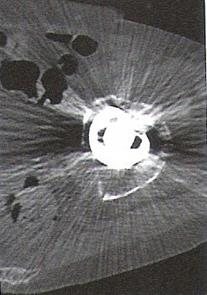
Zarejestrowany na obrazie TK artefakt jest spowodowany
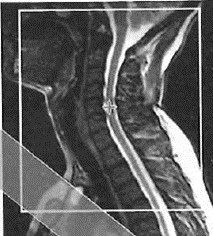
Na obrazie rezonansu magnetycznego strzałką wskazano patologiczny kręg
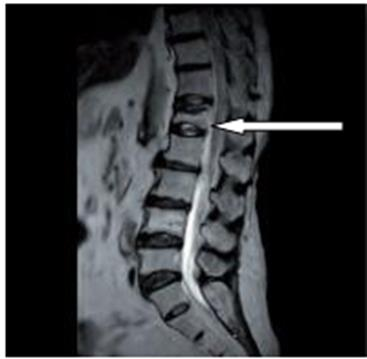
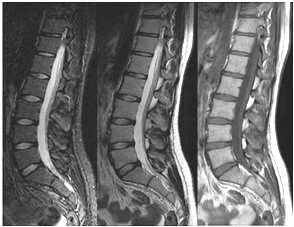
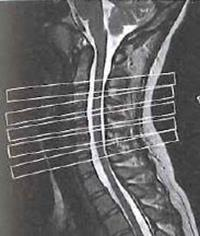
Które kolejne sekwencje badania kręgosłupa lędźwiowego uwidoczniono na przedstawionych obrazach?
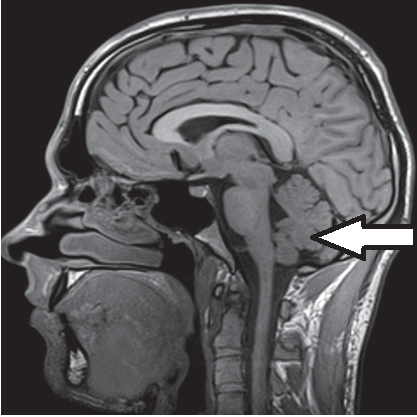
Którą strukturę anatomiczną oznaczono na obrazie rezonansu magnetycznego?
W obrazowaniu metodą rezonansu magnetycznego T1 oznacza czas
Zamieszczony obraz został wykonany metodą
Badanie cewki moczowej polegające na wstecznym wprowadzeniu środka kontrastowego to
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
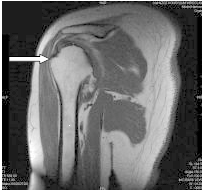
Którą strukturę anatomiczną oznaczono strzałką na obrazie rezonansu magnetycznego?
Która sekwencja w obrazowaniu MR jest stosowana do uwidocznienia naczyń krwionośnych?
Źródłem promieniowania protonowego stosowanego w radioterapii jest
Rutynowe badanie koronarografii prawej tętnicy wieńcowej wykonywane jest w rzucie skośnym przednim
W której projekcji należy wykonać badanie radiologiczne kręgosłupa lędźwiowego, by na otrzymanym zdjęciu wyrostki kręgów lędźwiowych układały się w charakterystyczny kształt piesków (teriera szkockiego)?
Zaznaczona strzałką struktura anatomiczna na obrazie rezonansu magnetycznego to
Gruboziarnista folia wzmacniająca wpływa na zwiększenie na obrazie rentgenowskim nieostrości
Na którym obrazie MR jest widoczne pasmo saturacji?

Ultrasonograficzne środki kontrastowe to