Pytanie 1
Na rysunku przedstawiono graficzną interpretację zależności wynikających z prawa
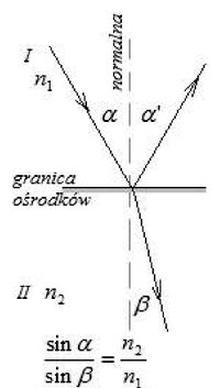
Wynik: 15/40 punktów (37,5%)
Wymagane minimum: 20 punktów (50%)
Na rysunku przedstawiono graficzną interpretację zależności wynikających z prawa

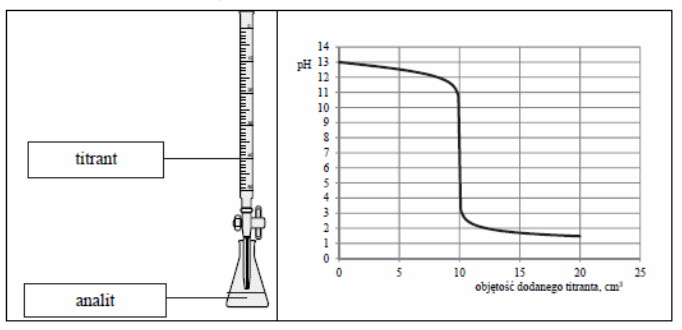
W jakich oznaczeniach analitycznych wykorzystuje się fenoloftaleinę jako wskaźnik?
Zamieszczony opis definiuje wskaźniki stosowane w miareczkowaniu
| Substancje te zmieniają zabarwienie w zależności od zmiany stężenia jonów wodorowych w roztworze. Są to słabe kwasy lub zasady organiczne, których barwa niezdysocjowanej cząsteczki w roztworze wodnym różni się od barwy jonów. |
Zjawisko dzielenia się składników mieszaniny pomiędzy fazę stacjonarną a ruchomą w układzie to proces widoczny w
Podłoże, które zawiera wyłącznie substancje niezbędne do rozwoju mikroorganizmów, określane jest jako
Stężenie wielopierścieniowych węglowodorów aromatycznych (WWA) w analizowanej próbce wynosi 4 g/dm3.
Po przeliczeniu jednostki na mg/m3 stężenie WWA będzie wynosić
Wyznaczanie punktu końcowego (PK) miareczkowania przy użyciu metod: graficznej, pierwszej pochodnej oraz Halina jest stosowane w
Wartość pH punktu równoważnikowego w miareczkowaniu mocnych kwasów przy użyciu mocnych zasad wynosi
Rozpuszczono próbkę technicznego chlorku sodu w wodzie, a jony chlorkowe strącono przy pomocy AgNO3, w postaci AgCl, którego masa po wysuszeniu wyniosła 1,5000 g. Oblicz ilość chloru w analizowanej próbce. Mnożnik analityczny dla chloru w AgCl to 0,2474.
Podstawą klasyfikacji kationów w analizie jakościowej jest wydzielanie trudno rozpuszczalnych osadów?
Jaką metodę wykorzystuje się do wykrywania i pomiaru ilościowego substancji optycznie czynnych?
Analizując próbkę wody powierzchniowej stwierdzono, że zawartość azotanów wynosi 4,5 mg/dm3, siarczanów 120 mg/dm3, a stężenie jonów chlorkowych 180 mg/dm3. Na podstawie danych zawartych w tabeli wskaż klasę czystości wody, z której została pobrana próbka.
| Wartości graniczne wskaźników jakości wody w klasach jakości wód powierzchniowych | |||||
|---|---|---|---|---|---|
| Wskaźnik [mg/dm³] | I klasa czystości | II klasa czystości | III klasa czystości | IV klasa czystości | V klasa czystości | Wartości dopuszczalne |
| azotany | 5,0 | 15,0 | 25,0 | 50,0 | >50,0 |
| siarczany | 100 | 150 | 250 | 300 | > 300 |
| chlorki | 100 | 200 | 300 | 400 | > 400 |
Zjawisko polegające na przepuszczaniu rozpuszczalnika przez membranę półprzepuszczalną z roztworu o wyższym stężeniu do roztworu o niższym stężeniu substancji rozpuszczonej określa się mianem
Wszelkie działania, które powinny zostać podjęte w celu usunięcia zidentyfikowanej niezgodności CCP (krytyczne punkty kontroli) w systemie HACCP, to działania
System HACCP – System Analizy Zagrożeń i Krytycznych Punktów Kontroli, stanowi zbiór wzajemnie powiązanych ze sobą procedur, które w całości tworzą system zarządzania bezpieczeństwem żywności.
Jakim urządzeniem mierzy się zasolenie gleby?
W laboratorium mikrobiologicznym do przeprowadzania jałowienia na zimno wykorzystuje się
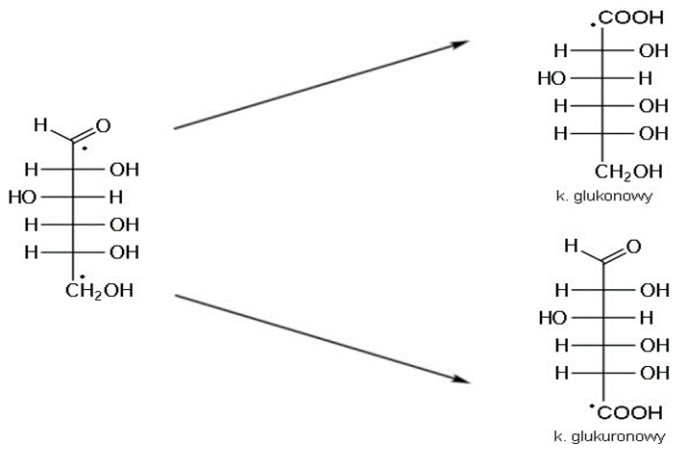
Kwas glukuronowy powstaje z glukozy w wyniku utlenienia
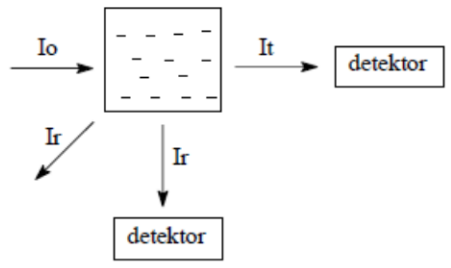
Pomiar intensywności światła rozproszonego Ir po przejściu przez roztwór koloidalny wykonuje się z zastosowaniem
Aby określić wartość absorbancji substancji X, zmierzono, przy tych samych długościach fali, absorbancję mieszaniny X i Y oraz osobno substancji Y.
Jeśli AX+Y = 0,84, a AY = 0,56, to jaka jest wartość AX?
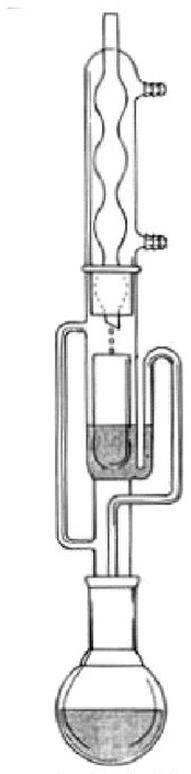
Przedstawiony na rysunku aparat służy do
Do technik rozdzielania należy
Na rysunku przedstawiono sprzęt stosowany do
Przeprowadzono orientacyjną ocenę jakości mikrobiologicznej mleka w tak zwanej próbie azotanowej, która zabarwiła się na kolor bladoróżowy, co znaczy, że jakość mleka wziętego do analizy była
| Zabarwienie próbki mleka | Ocena jakości próbki Mleko: |
|---|---|
| bez zmiany barwy | bardzo dobre i dobre |
| lekko lub wyraźnie różowa | średniej jakości |
| intensywnie różowa, czerwona lub brunatna | złej jakości |
Twardość ogólna badanej wody wynosi 2,5 mval/l. Wartość ta wyrażona w mg CaCO3/l wynosi
| Tabela. Jednostki twardości wody | |||||
| Jednostka twardości | mmol/l | mval/l | mg CaCO3/l | °f stopień francuski | °n stopień niemiecki |
|---|---|---|---|---|---|
| 1 mmol/l | 1 | 2 | 100 | 10 | 5,6 |
| 1 mval/l | 0,5 | 1 | 50 | 5,0 | 2,8 |
| 1 mg CaCO3/l | 0,01 | 0,02 | 1 | 0,1 | 0,056 |
| 1 stopień francuski (°f) | 0,1 | 0,2 | 10 | 1 | 0,56 |
| 1 stopień niemiecki (°n) | 0,178 | 0,357 | 17,8 | 1,78 | 1 |
Jak określane są enzymy, które katalizują przenoszenie różnych grup funkcyjnych?
Jak należy ogrzewać probówkę z roztworem w trakcie wykrywania kationów II grupy analitycznej, gdy powstaje H2S?
Formy przetrwalnikowe bakterii nie obejmują
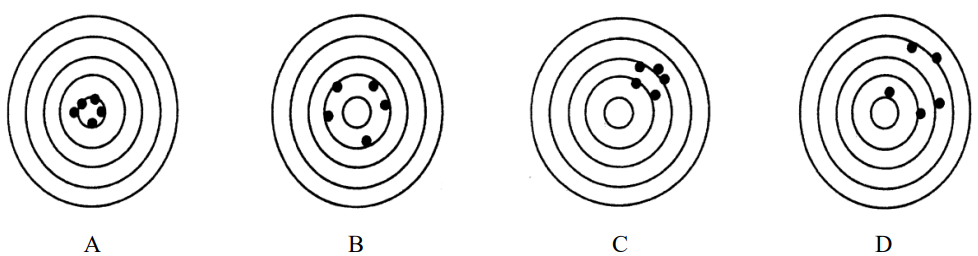
Na rysunkach przedstawiono serie pomiarów o różnej dokładności i precyzji (środek najmniejszego okręgu oznacza wartość prawdziwą). Serię pomiarów precyzyjnych, ale niedokładnych przedstawiono na rysunku
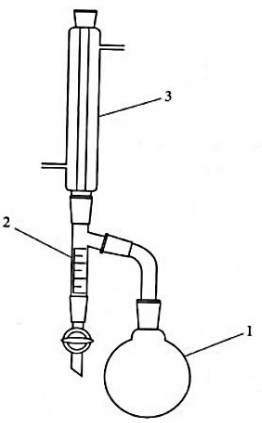
Zestaw przedstawiony na rysunku służy do oznaczania zawartości
Opis schematu:
1 - kolba okrągłodenna
2 - odbieralnik
3 - chłodnica zwrotna
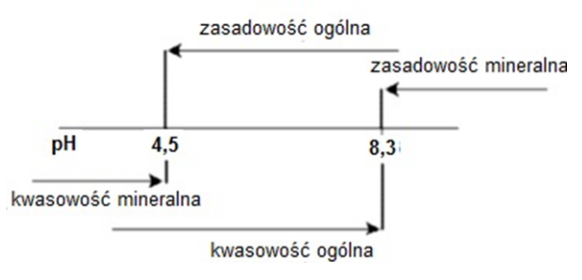
Na schemacie przedstawiono zakres występowania kwasowości i zasadowości w wodach naturalnych w zależności od pH. Dla wody o pH = 4,1 należy wykonać badanie
Eliminacja twardości wody w metodzie fizyko-chemicznej polega na użyciu
Jak należy przygotować próbkę wody do zamrożenia w naczyniu, które
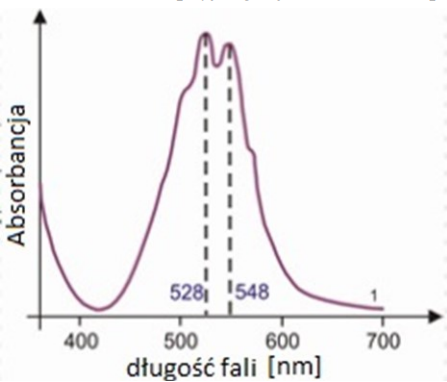
Która z przedstawionych na wykresie długości fali widma absorpcyjnego jonów MnO4- powinna być stosowana jako długość analityczna?
Zamieszczony w ramce opis określa liczbę
| Liczba gramów fluorowca, przeliczona na gramy jodu, który w określonych warunkach ulega reakcji addycji do atomów węgla związanych wiązaniem wielokrotnym, zawartych w 100 g badanego tłuszczu. Jest ona proporcjonalna do liczby wiązań wielokrotnych w tłuszczach. |
KOH w formie roztworu jest wykorzystywany jako titrant w analizie żywności do określenia
Które równanie przedstawia reakcję wytrącania osadu?
Oznaczanie wagowe substancji jest możliwe, kiedy analizowany związek jest
Metoda Mohra do oznaczania chlorków polega na
Wykonano identyfikację opisaną w schemacie:
BaCl2 + X — biały osadJaki wzór reprezentuje substrat X?
Przedstawiona na rysunku komora laminarna jest stosowana w laboratorium w celu bezpiecznego wykonywania prac
