Pytanie 1
Cholangiografia to badanie radiologiczne
Wynik: 38/40 punktów (95,0%)
Wymagane minimum: 20 punktów (50%)
Cholangiografia to badanie radiologiczne
Zgodnie ze standardami do wykonania zdjęcia bocznego czaszki, należy zastosować kasetę o wymiarze
Technikę bramkowania oddechowego stosuje się w badaniu MR
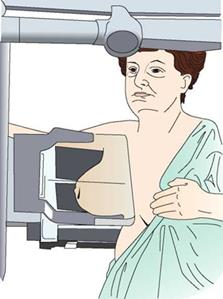
Na ilustracji przedstawiono pozycjonowanie pacjentki do badania mammograficznego w projekcji
Po podaniu kontrastu obraz zmian nowotworowych w badaniu MR najlepiej uwidacznia się w sekwencji
Jaki kolor ma warstwa korowa kości w badaniu MR na obrazie T1- zależnym?
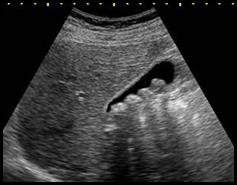
Którą strukturę anatomiczną uwidoczniono na zamieszczonym obrazie USG?
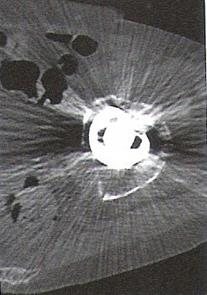
Zarejestrowany na obrazie TK artefakt jest spowodowany
Który system informatyczny służy do archiwizacji i transmisji obrazów radiologicznych?
Nieostrość geometryczna obrazu rentgenowskiego zależy od
Jak oznacza się w radioterapii obszar tkanek zawierający GTV i mikrorozsiewy w fazie niewykrywalnej klinicznie?
Skrótem HRCT (High Resolution Computed Tomography) określa się tomografię komputerową
W jakiej pozycji układa się pacjenta do standardowego badania MR kręgosłupa szyjnego?
Jaki rozmiar kasety należy zastosować, wykonując standardowe zdjęcie stawu kolanowego w projekcji bocznej?
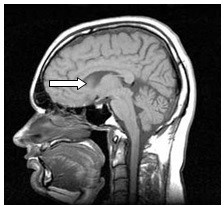
Zaznaczona strzałką struktura anatomiczna na obrazie rezonansu magnetycznego to
Przy ułożeniu do zdjęcia AP czaszki płaszczyzna
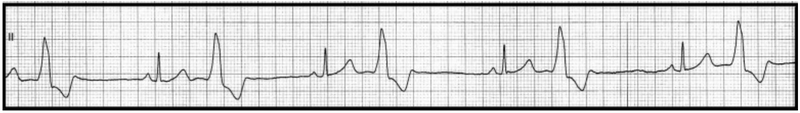
Który stan patologiczny został zarejestrowany podczas wykonywania badania EKG?
Cholangiografia to badanie radiologiczne
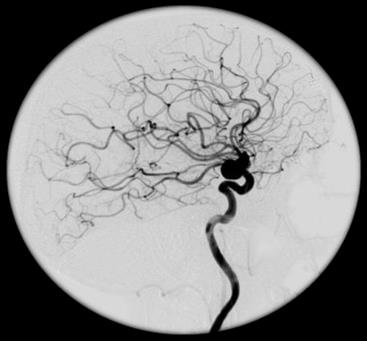
W przedstawionym na ilustracji obrazie badania angiograficznego uwidoczniono
Jakie źródła promieniowania stosowane są w brachyterapii?
DSA to cyfrowa
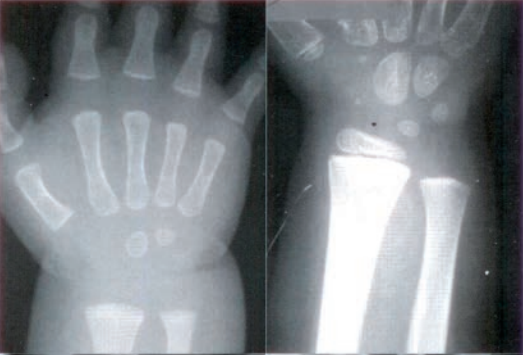
Zestaw rentgenogramów przedstawia
Gruboziarnista folia wzmacniająca wpływa na zwiększenie na obrazie rentgenowskim nieostrości
W systemie międzynarodowym ząb pierwszy przedtrzonowy po stronie lewej oznacza się symbolem
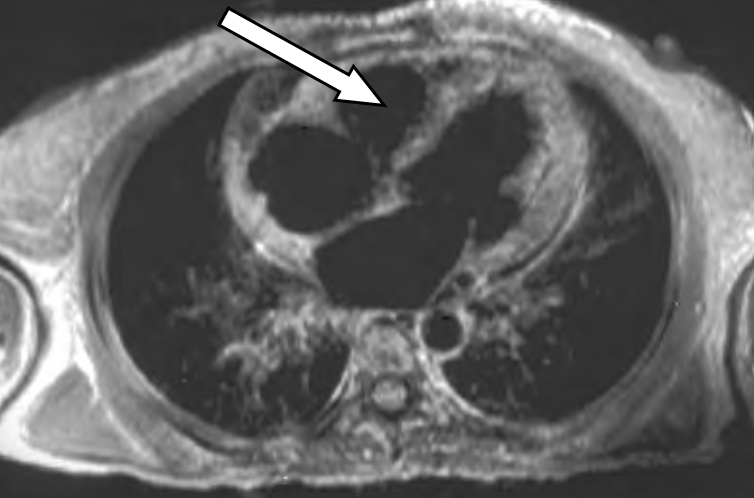
Na skanie rezonansu magnetycznego serca oznaczono
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem
Zadaniem technika elektroradiologa w pracowni naczyniowej jest
W których projekcjach podstawowych wykonuje się standardowe badanie mammograficzne?
Rutynowe badanie koronarografii prawej tętnicy wieńcowej wykonywane jest w rzucie skośnym przednim
W której technice brachyterapii stosuje się źródła promieniowania o mocy dawki 2-12 Gy/h?
W przypadku migotania komór w zapisie EKG występuje
W obrazowaniu MR wykorzystuje się moment magnetyczny
Które obszary napromieniowania powinien określić lekarz radioterapeuta u pacjenta z nowotworem stercza po wcześniejszej prostatektomii?
Która metoda diagnostyczna służy do określenia gęstości minerału kostnego w ujęciu objętościowym g/cm³?
Testy specjalistyczne aparatów rentgenowskich do zdjęć wewnątrzustnych są przeprowadzane
Podczas badania EEG w systemie „10-20” literą A oznacza się elektrody
W technice napromieniania SSD mierzona jest odległość źródła promieniowania
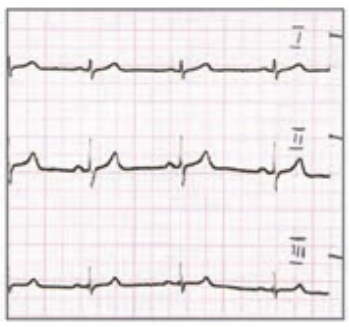
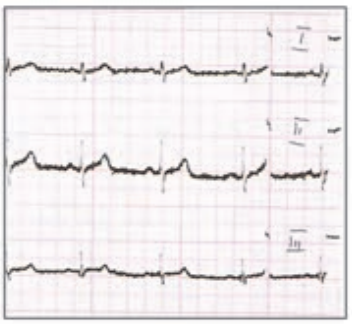
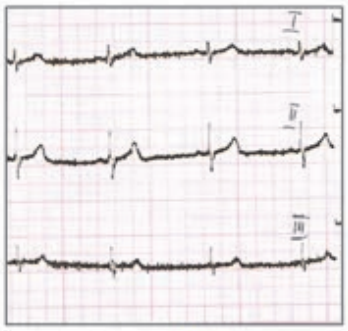
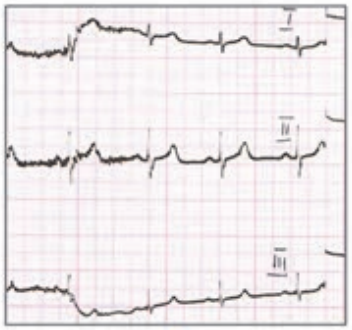
Który elektrokardiogram jest poprawny technicznie?
Do wykonania stomatologicznego zdjęcia rentgenowskiego techniką kąta prostego promień centralny należy ustawić prostopadle do
W której technice obrazowania zostają zarejestrowane jednocześnie dwa przeciwbieżne kwanty promieniowania gamma o równej energii 511 keV?