Pytanie 1
Przedstawiony obraz został zarejestrowany podczas wykonywania
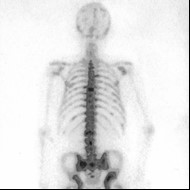
Wynik: 22/40 punktów (55,0%)
Wymagane minimum: 20 punktów (50%)
Przedstawiony obraz został zarejestrowany podczas wykonywania

Obiektywną metodą badania słuchu jest audiometria
Która struktura może być oknem akustycznym w badaniu ultrasonograficznym?
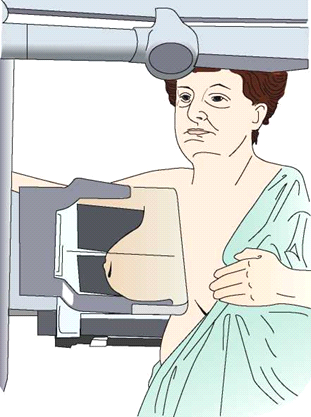
Ilustracja przedstawia pozycjonowanie pacjentki do badania mammograficznego w projekcji
Który radiofarmaceutyk należy podać pacjentowi w scyntygrafii perfuzyjnej mózgu?
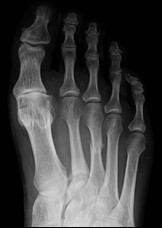
Na radiogramie stopy uwidocznione jest złamanie trzonu
Do zdjęcia lewobocznego kręgosłupa lędźwiowo-krzyżowego pacjenta należy ułożyć na boku
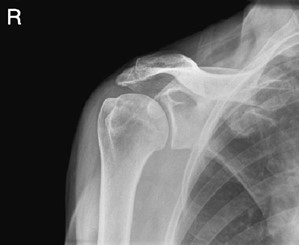
Na radiogramie uwidoczniono
Kryterium rozpoznawczym dla fali δ (delta) w badaniu EKG jest
Na zamieszczonej rycinie przedstawiono
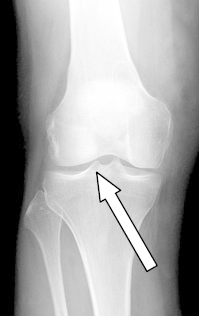
Którą strukturę anatomiczną oznaczono strzałką na radiogramie stawu kolanowego?
Podczas wykonywania badania EEG elektrodę P4 umieszcza się w okolicy
Do zdjęcia rentgenowskiego kręgosłupa piersiowego w projekcji AP pacjenta należy ułożyć
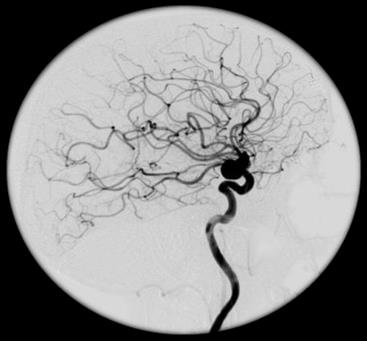
W przedstawionym na ilustracji obrazie badania angiograficznego uwidoczniono
Kolimator wielolistkowy w akceleratorze liniowym jest stosowany do
Hiperfrakcjonowanie dawki w radioterapii oznacza napromieniowywanie pacjenta
Brachyterapia wewnątrzjamowa jest wykorzystywana podczas leczenia nowotworu
Którą ochronę radiologiczną należy zastosować podczas wykonywania zdjęcia rentgenowskiego przeglądowego klatki piersiowej u pacjentki w okresie rozrodczym?
Który system informatyczny służy do archiwizacji i transmisji obrazów radiologicznych?
W jaki sposób należy ustawić promień centralny w stosunku do ramienia i przedramienia, by wykonać zdjęcie rentgenograficzne stawu łokciowego u pacjenta z przykurczem?
Technikę bramkowania oddechowego stosuje się w badaniu MR
W scyntygrafii dynamiczne badanie najczęściej rozpoczyna się
W pracowni radioterapii wyświetlenie na ekranie monitora aparatu komunikatu „ROTATION” oznacza prowadzoną terapię
Kto jest odpowiedzialny za wykonywanie testów podstawowych kontroli jakości gammakamery w Zakładzie Medycyny Nuklearnej?
Które obszary napromieniowania powinien określić lekarz radioterapeuta u pacjenta z nowotworem stercza po wcześniejszej prostatektomii?
Promieniowanie rentgenowskie jest
Który radiofarmaceutyk może zostać podany pacjentowi w scyntygrafii perfuzyjnej mózgu?
W którym okresie ciąży wykonanie u kobiety zdjęcia rentgenowskiego klatki piersiowej jest najbardziej szkodliwe dla płodu?
Planowany obszar napromieniania PTV obejmuje
W badaniu EKG elektrodę przedsercową V4 należy umocować
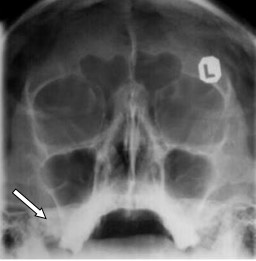
Na radiogramie czaszki strzałką zaznaczono
Testy specjalistyczne aparatów rentgenowskich do zdjęć wewnątrzustnych są przeprowadzane
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem
Który program wtórnej rekonstrukcji obrazów TK pozwala na odwzorowanie wnętrza jelita grubego, tchawicy i oskrzeli?
HRCT (high-resolution computed tomography) jest metodą obrazowania TK
W diagnostyce metodą rezonansu magnetycznego biorą udział
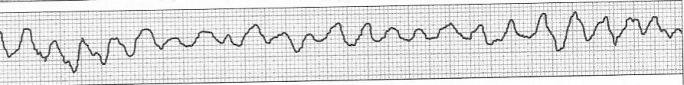
Zamieszczony elektrokardiogram przedstawia
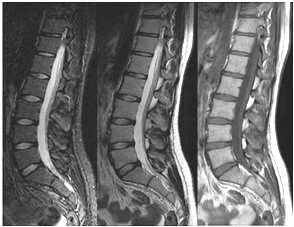
Które kolejne sekwencje badania kręgosłupa lędźwiowego uwidoczniono na przedstawionych obrazach?
Testy podstawowe z zakresu geometrii pola rentgenowskiego, przeznaczone do sprawdzenia zgodności pola wiązki promieniowania rentgenowskiego z symulacją świetlną, są wykonywane raz
Brachyterapia polegająca na wielokrotnym wsuwaniu i wysuwaniu źródła promieniowania do tego samego aplikatora nosi nazwę