Pytanie 1
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Wynik: 31/40 punktów (77,5%)
Wymagane minimum: 20 punktów (50%)
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
W przypadku migotania komór w zapisie EKG występuje
Na przedstawionym scyntygramie ukazano duży obszar
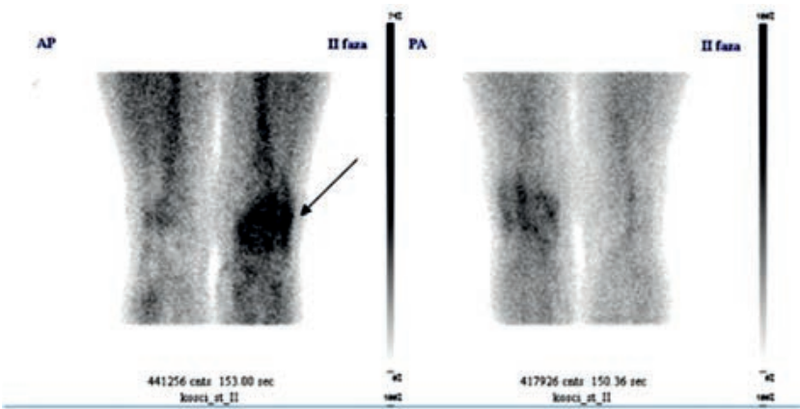
W badaniu EKG różnice potencjałów pomiędzy lewym podudziem a lewym przedramieniem rejestruje odprowadzenie
Podczas badania EEG otwarcie oczu powoduje
Na ilustracji przedstawiono pozycjonowanie pacjentki do badania mammograficznego w projekcji
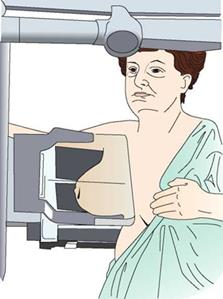
Na zamieszczonym przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano

W badaniu MR czas repetycji TR jest parametrem określającym odstęp czasu między
Jaki czas należy ustawić do wykonania zdjęcia rentgenowskiego dwójki górnej lewej?
| Tabela ekspozycji | |||
|---|---|---|---|
| wartości | czasu (s) | napięcia (kV) | natężenia (mA) |
| zęby przedtrzonowe i kły | 0,160 | 60 | 8 |
| siekacze | 0,120 | 60 | 8 |
| zęby trzonowe | 0,200 | 60 | 8 |
| ekspozycja zgryzowo-skrzydełkowa | 0,180 | 66 | 6 |
Którą strukturę anatomiczną oznaczono na zamieszczonym obrazie rezonansu magnetycznego?
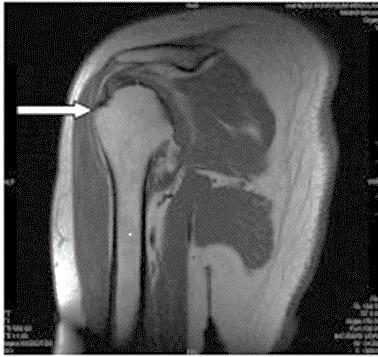
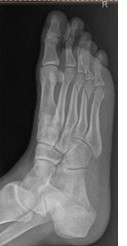
Na radiogramie stopy strzałką wskazano kość
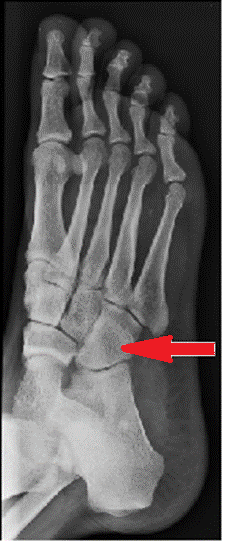
Centratory laserowe zamontowane w kabinie aparatu terapeutycznego służą do
W technice napromieniania SSD mierzona jest odległość źródła promieniowania od
Zgodnie z obowiązującą procedurą radiologiczną zdjęcie jamy brzusznej przy podejrzeniu zapalenia nerek zostanie wykonane w projekcji
W radiologii stomatologicznej ząb o numerze 23 to kieł
Do pomiaru dawek indywidualnych u osób narażonych zawodowo na promieniowanie rentgenowskie są stosowane
Rytm alfa i beta rejestruje się podczas badania
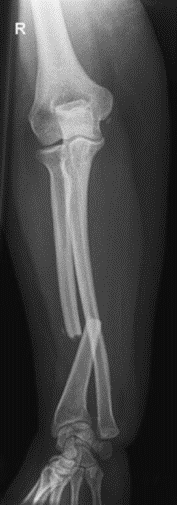
Na radiogramie uwidoczniono złamanie
Zgodnie z procedurą wzorcową w badaniu MR należy ułożyć pacjenta na brzuchu do diagnostyki
Które zdjęcia należy wykonać pacjentom z chorobą reumatoidalną stawów kolanowych?
Droga przewodnictwa powietrznego fali akustycznej przebiega przez
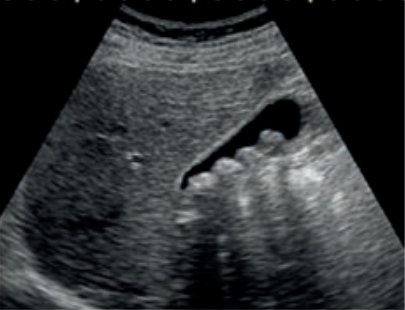
Jakie struktury anatomiczne uwidoczniono na obrazie USG?
W scyntygrafii wykorzystywane są głównie radioizotopy emitujące promieniowanie
Podczas wykonywania badania EKG czarną elektrodę kończynową należy umieścić na kończynie dolnej
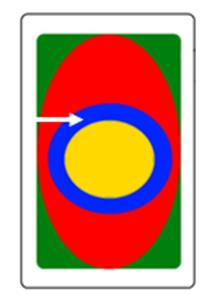
Który obszar napromieniania wskazano na ilustracji strzałką?
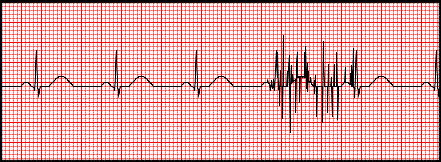
Artefakty zarejestrowane na elektrokardiogramie zostały wywołane przez
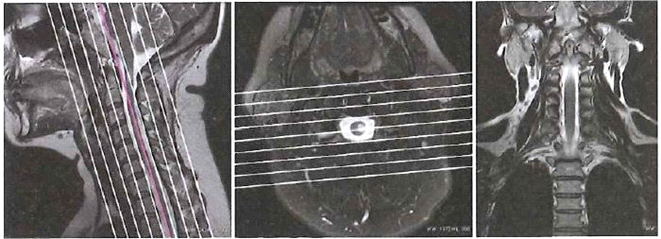
Obrazy MR kręgosłupa szyjnego przedstawiają etap planowania badania warstw
Który środek ochrony radiologicznej należy zastosować podczas badania czaszki 53-letniego pacjenta za pomocą tomografii komputerowej?
W badaniu PET stosuje się tylko radioizotopy emitujące
„Ognisko zimne” w obrazie scyntygraficznym oznacza
Diagnozowanie metodą PET oparte jest na zjawisku
W pozytonowej tomografii emisyjnej PET zostaje zarejestrowane promieniowanie powstające podczas
Które czynności wykonuje technik elektroradiolog w pracowni „gorącej”?
Skrótem HRCT (High Resolution Computed Tomography) określa się tomografię komputerową
Na rentgenogramie stopy uwidocznione jest złamanie
Pracownia radioterapii z przyspieszaczem liniowym jest obszarem
Fala głosowa rozchodzi się
Brachyterapia wewnątrzjamowa jest wykorzystywana podczas leczenia nowotworu
Czas połowicznego zaniku jest wykorzystywany
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego