Pytanie 1
W celu oceny wieku kostnego u dziecka praworęcznego, wykonuje się pojedyncze zdjęcie w projekcji
Wynik: 40/40 punktów (100,0%)
Wymagane minimum: 20 punktów (50%)
W celu oceny wieku kostnego u dziecka praworęcznego, wykonuje się pojedyncze zdjęcie w projekcji
Elementem systemu rejestracji obrazu, w którym fotony promieniowania X są bezpośrednio konwertowane na sygnał elektryczny, jest
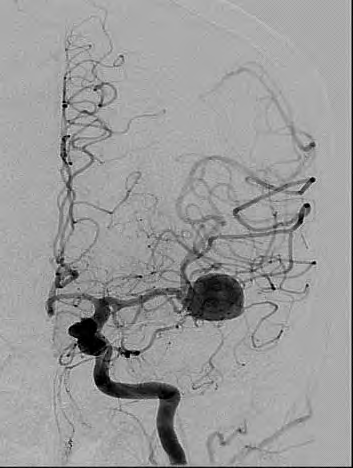
Którą patologię uwidoczniono w badaniu angiograficznym?
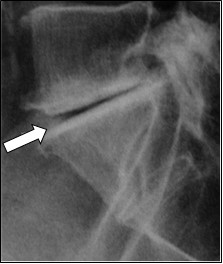
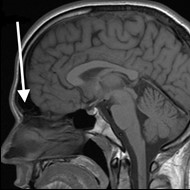
Na rentgenogramie strzałką zaznaczono
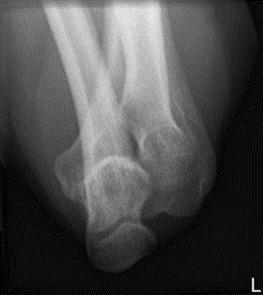
Którą strukturę anatomiczną i w jakiej projekcji uwidoczniono na radiogramie?
W zapisie EKG załamki P dodatnie w odprowadzeniu I i II, a ujemne w aVR oraz częstotliwość rytmu mniejsza niż 60/min wskazują na
W systemie międzynarodowym czwarty górny ząb mleczny po stronie prawej oznacza się symbolem
Zgodnie z obowiązującymi przepisami powierzchnia gabinetu rentgenowskiego, w którym jest zainstalowany zestaw rentgenowski do badań naczyniowych, powinna wynosić
Który system informatyczny służy do archiwizacji i transmisji obrazów radiologicznych?
W sekwencji echa spinowego obraz T2-zależny uzyskuje się przy czasie repetycji TR
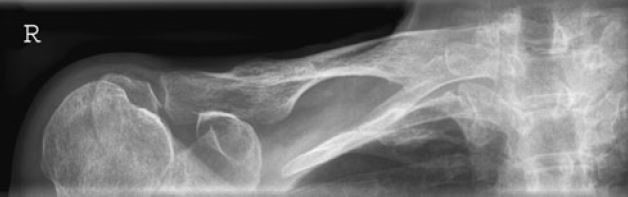
W jakiej projekcji i pod jakim kątem padania promienia centralnego został wykonany radiogram obojczyka?
Zgodnie z procedurą wzorcową w badaniu MR należy ułożyć pacjenta na brzuchu do diagnostyki
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
Brachyterapia wewnątrzjamowa jest wykorzystywana podczas leczenia nowotworu
Brachyterapia polegająca na wielokrotnym wsuwaniu i wysuwaniu źródła promieniowania do tego samego aplikatora nosi nazwę
Które ciało obce w obszarze badania nie stanowi przeciwwskazania do wykonania MR?
Do środków kontrastujących negatywnych należą
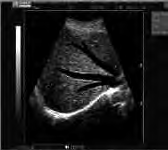
Na obrazie ultrasonograficznym jamy brzusznej uwidoczniono
Największa wartość energii promieniowania stosowanego w radioterapii jest generowana przy użyciu
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
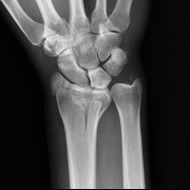
Na obrazie radiologicznym nadgarstka uwidoczniono złamanie nasady
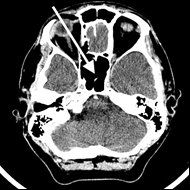
Na radiogramie TK głowy strzałką wskazano
W radiografii mianem SID określa się
Zwiększenie napięcia na lampie rentgenowskiej powoduje
Jaki kolor ma warstwa korowa kości w badaniu MR na obrazie T1- zależnym?
HRCT (high-resolution computed tomography) jest metodą obrazowania TK
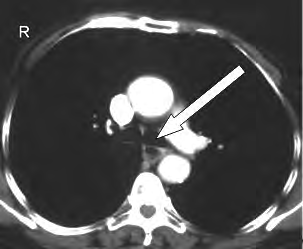
Na obrazie TK klatki piersiowej w przekroju poprzecznym strzałką oznaczono
Cholangiografia to badanie radiologiczne
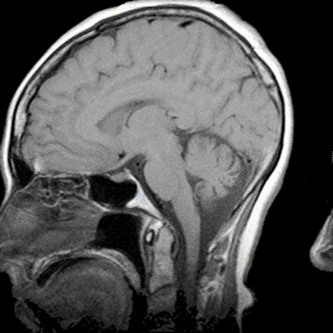
Który artefakt uwidoczniono na skanie RM głowy?
Do pomiaru dawek indywidualnych u osób narażonych zawodowo na promieniowanie rentgenowskie są stosowane
Wskazaniem do wykonania badania spirometrycznego jest
Na obrazie rezonansu magnetycznego głowy strzałką wskazano zatokę
Proces chemicznego wywoływania radiogramów polega na
Radioizotopowa terapia medycyny nuklearnej polega na wprowadzeniu do tkanek lub narządów radiofarmaceutyku
Wskazaniem do zastosowania brachyterapii w leczeniu radykalnym jest rak
Ligand stosuje się
W technice napromieniania SSD mierzona jest odległość źródła promieniowania
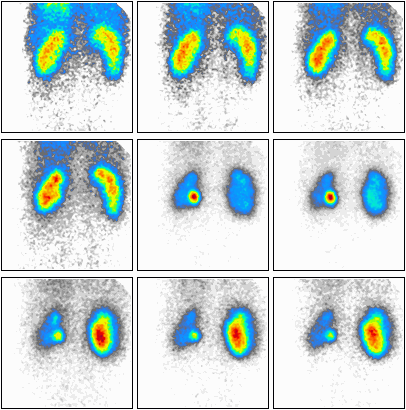
Podczas którego badania zostały zarejestrowane przedstawione obrazy?
Dobierz dla standardowego pacjenta projekcję, pozycję i sposób ułożenia kasety o wymiarach 30 cm x 40 cm do zdjęcia przeglądowego układu moczowego.
| Projekcja | Pozycja | Ułożenie kasety | |||
|---|---|---|---|---|---|
| 1. | AP | 3. | stojąca | 5. | poprzeczne |
| 2. | PA | 4. | leżąca | 6. | podłużne |
Obszary napromieniania w technice IMRT w trakcie wykonywania zabiegu radioterapeutycznego wyznacza