Pytanie 1
Do przechowywania zamrożonych próbek wody stosuje się naczynia wykonane
Wynik: 32/40 punktów (80,0%)
Wymagane minimum: 20 punktów (50%)
Do przechowywania zamrożonych próbek wody stosuje się naczynia wykonane
Aby uniknąć trwałego połączenia szlifowanych części sprzętu laboratoryjnego, co należy zrobić?
Proces oddzielania cieczy od osadu nazywa się
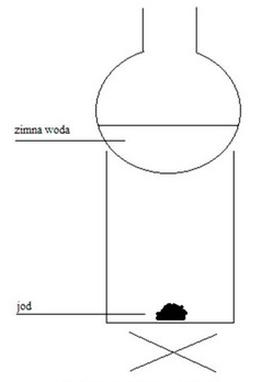
Na rysunku przedstawiono zestaw do oczyszczania jodu w procesie
Temperatura topnienia mocznika wynosi 133 °C. W celu określenia czystości preparatów tej substancji, przeprowadzono badania temperatury ich topnienia, uzyskując wyniki przedstawione w tabeli. Wskaż preparat o najmniejszym stopniu czystości.
| Preparat | A | B | C | D |
|---|---|---|---|---|
| Zakres temperatury topnienia [°C] | 132-133 | 130-133 | 125-133 | 128-133 |
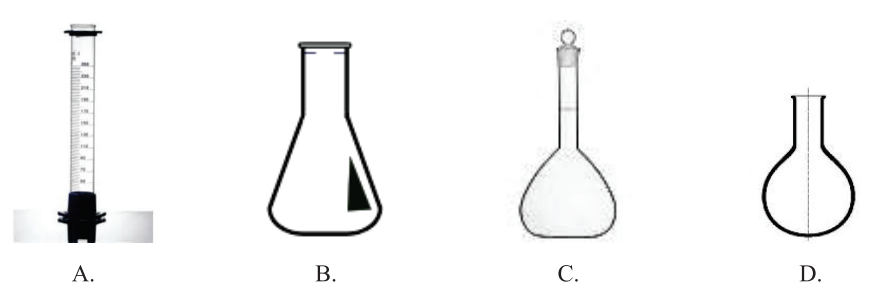
W celu przygotowania roztworu mianowanego należy użyć sprzętu przedstawionego na rysunku
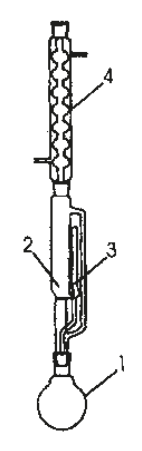
Aparat przedstawiony na rysunku służy do
Jakie metody można zastosować do rozdzielania i koncentracji składników próbki?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Najskuteczniejszą techniką separacji ketonu oraz kwasu karboksylowego obecnych w roztworze benzenowym jest
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Stosunek masowy miedzi do siarki w siarczku miedzi(I) wynosi
| 16S Siarka 32 | 29Cu Miedź 63,55 |
Na podstawie zamieszczonych w tabeli opisów metod rozdzielania mieszanin, dobierz odpowiadające im nazwy.
| Tabela. Metody rozdzielania mieszanin | |
|---|---|
| Lp. | Opis metody |
| I. | Zlewanie cieczy znad osadu. |
| II. | Przeprowadzenie ciekłego rozpuszczalnika w stan pary. |
| III. | Wyodrębnianie z mieszaniny ciał stałych lub cieczy składnika przy pomocy rozpuszczalnika tak dobranego, aby rozpuszczał żądany związek chemiczny. |
| IV. | Powolne opadanie cząstek substancji stałej w cieczy pod wpływem własnego ciężaru. |
Aby oszacować czystość MgCO3, poddano prażeniu próbkę o wadze 5 g tej soli aż do osiągnięcia stałej masy. W trakcie prażenia zachodzi reakcja:
MgCO3 → MgO + CO2 Całkowity ubytek masy wyniósł 2,38 g.
(Masy molowe reagentów to: MgCO3 – 84 g/mol, MgO – 40 g/mol, CO2 – 44 g/mol) Jaką czystość miała próbka węglanu magnezu?
W laboratoriach roztwór potasu dichromianu(VI) w stężonym kwasie siarkowym(VI) wykorzystuje się do
Jakie są zalecenia dotyczące postępowania z odpadowymi roztworami kwasów oraz zasad?
Laboratoryjny aparat szklany, który wykorzystuje kwasy do wytwarzania gazów w reakcji z metalem lub odpowiednią solą, to
Czy próbkę laboratoryjną przechowuje się w lodówce, gdy występuje w niej
Oblicz stężenie molowe 250 cm3 roztworu NaOH, w którym znajduje się 0,5 g substancji. Masa molowa NaOH wynosi 40 g/mol
Zdjęcie przedstawia palnik

Na podstawie danych w tabeli próbkę, w której będzie oznaczany BZT, należy przechowywać
| Oznaczany parametr | Rodzaj naczynia do przechowywania | Sposób utrwalania | Dopuszczalny czas przechowywania |
|---|---|---|---|
| barwa | szklane lub polietylenowe | - schłodzenie do temperatury 2-5°C | 24 h |
| fosforany ogólne | szklane lub polietylenowe | - zakwaszenie kwasem siarkowym(VI) - schłodzenie do temperatury 2-5°C | 4 h 48 h |
| BZT | szklane | - schłodzenie do temperatury 2-5°C - przechowywanie w ciemności | 24 h |
| azot azotanowy(V) | szklane lub polietylenowe | - schłodzenie do temperatury 2-5°C - dodanie 2 cm3 chloroformu do 1 dm3 próbki | 24 h 48 h |
Użycie płuczek jest konieczne w trakcie procesu
W przypadku odczynnika, w którym nawet najczulsze techniki analizy chemicznej nie są w stanie wykryć zanieczyszczeń, a jego badanie wymaga zastosowania metod opartych na zjawiskach fizycznych, zalicza się on do kategorii czystości
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Odczynnik chemiczny, w którym zawartość domieszek wynosi od 1 do 10%, jest nazywany odczynnikiem
Wskaż definicję fiksanali?
Metodą, która nie służy do utrwalania próbek wody, jest
Jaką próbkę stanowi woreczek gleby pobranej zgodnie z instrukcją?
| Instrukcja pobierania próbek glebowych | |
| Próbki pierwotne pobiera się laską glebową z wierzchniej warstwy gleby 0-20 cm, kolejno wykonując czynności: – w miejscu pobierania próbki pierwotnej (pojedynczej), rolę świeżo zaoraną przydeptać, – pionowo ustawić laskę do powierzchni gleby, – wcisnąć laskę do oporu (na wysokość poprzeczki ograniczającej), – wykonać pełny obrót i wyjąć laskę, – zawartość wgłębienia (zasobnika) przenieść do pojemnika skrobaczki. Po pobraniu próbek pojedynczych, całość wymieszać i napełnić kartonik lub woreczek. | |
Próbki pobrano z materiału o objętości \( 100 \, \text{m}^3 \), wysypanego z opakowania. Liczba miejsc poboru próbek pierwotnych z tego materiału wynosi:
$$ n = 0{,}5 \cdot \sqrt{V} $$ gdzie:
\( V \) – objętość jednostki badanej w \( \text{m}^3 \)
\( n \) – liczba miejsc poboru próbek
Odważka analityczna przygotowana w fabryce zawiera 0,1 mola EDTA. Posiadając taką jedną odważkę analityczną, jakie roztwory można przygotować?
Które z poniższych równań ilustruje reakcję, w której powstają produkty gazowe?
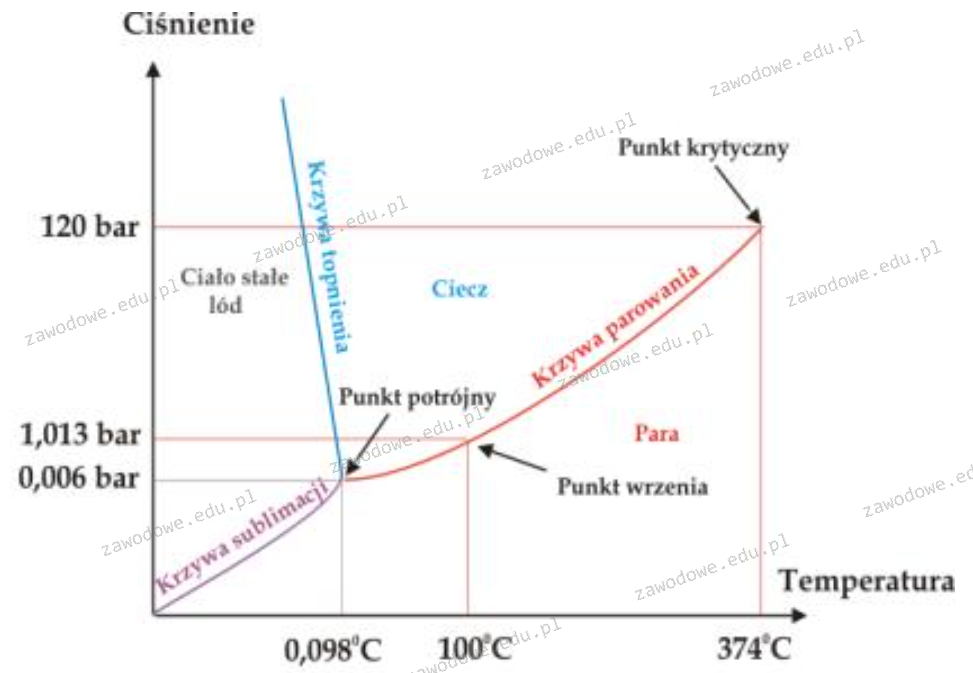
Korzystając z wykresu wskaż, w jakiej postaci występuje woda w temperaturze 10°C i pod ciśnieniem 100 barów.
Z etykiety wynika, że dany związek mógł być

Który z etapów przygotowania próbek do analizy opisano w ramce?
| Proces polegający na usuwaniu wody z zamrożonego materiału na drodze sublimacji lodu, tzn. bezpośredniego jego przejścia w stan pary z pominięciem stanu ciekłego. |
Podczas pobierania próby wody do oznaczania metali ciężkich zaleca się stosowanie butelek wykonanych z:
Próbkę wody przeznaczoną do oznaczenia zawartości metali poddaje się utrwalaniu za pomocą
| Sposoby utrwalania i przechowywania próbek wody przeznaczonych do badań fizykochemicznych. | |
|---|---|
| Oznaczenie | Sposób utrwalania i przechowywania |
| Barwa | Przechowywać w ciemności |
| Mętność | Przechowywać w ciemności |
| Twardość | pH = 3 z użyciem HNO₃ |
| OWO | 0,7 ml HCl/30 ml próbki |
| ChZT | pH 1-2 z użyciem H₂SO₄ |
| Fosfor | Przechowywać w temperaturze 1-5°C |
| Glin | pH 1-2 z użyciem HNO₃ |
| Żelazo | pH 1-2 z użyciem HNO₃ |
| Utlenialność | pH1-2 z użyciem H₂SO₄. Przechowywać w ciemności |