Pytanie 1
Jaką metodę wykorzystuje się w laboratorium do rozdzielenia osadu AgCl od cieczy macierzystej w probówkach?
Wynik: 22/40 punktów (55,0%)
Wymagane minimum: 20 punktów (50%)
Jaką metodę wykorzystuje się w laboratorium do rozdzielenia osadu AgCl od cieczy macierzystej w probówkach?
Jakim kolorem oznacza się instalację gazową w laboratorium analitycznym?
Z uwagi na higroskopijne właściwości tlenku fosforu(V) powinien on być przechowywany w warunkach bez dostępu
Podczas pipetowania menisk górny określa się dla roztworów
Na rysunku numerami rzymskimi oznaczono
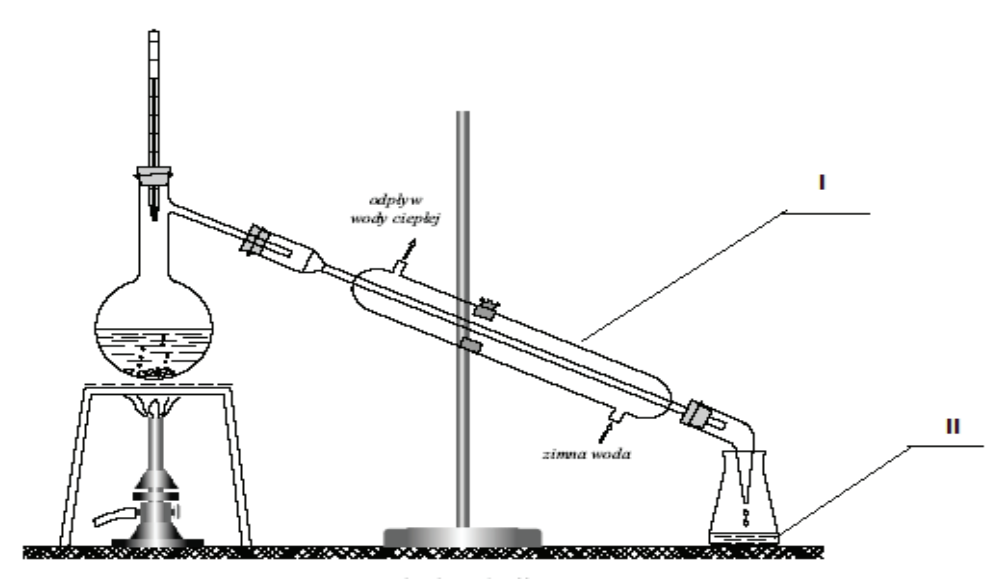
Jakie czynniki wpływają na zmiany jakościowe w składzie próbki?
Aby otrzymać roztwór AgNO3 (masa molowa AgNO3 to 169,8 g/mol) o stężeniu 0,1 mol/dm3, należy
Jakim narzędziem dokonuje się poboru próbki wody?
Użycie płuczek jest konieczne w trakcie procesu
W celu sprawdzenia stężenia kwasu siarkowego(VI) odważono 1 g badanego kwasu i przeprowadzono analizę miareczkową, w której zużyto 20,4 \( \text{cm}^3 \) roztworu NaOH.
Stężenie procentowe badanego kwasu, obliczone na podstawie wzoru wynosi
$$ C_p = \frac{0,02452 \cdot V_{NaOH}}{mp} \cdot 100\% $$gdzie:
\( C_p \) – stężenie procentowe badanego kwasu; \( \% \)
\( 0,02452 \) – współczynnik przeliczeniowy; \( \text{g/cm}^3 \)
\( V_{NaOH} \) – objętość roztworu NaOH, zużyta w miareczkowaniu; \( \text{cm}^3 \)
\( mp \) – odważka badanego kwasu; g
Aby uzyskać sole sodowe fenoli, należy stopić dany fenol z sodą (M = 106 g/mol), stosując 10% nadmiar w porównaniu do ilości stechiometrycznej, według równania:
2 ArOH + Na2CO3 → 2 ArONa + H2O + CO2 Ile sody jest wymagane do reakcji z 7,2 g 2-naftolu (M = 144 g/mol)?
Jakie urządzenie służy do pomiaru temperatury topnienia substancji chemicznych?
Przedstawiony sposób dotyczy pobierania próbki wody do przeprowadzenia badań
| Sposób pobierania próbki wody do przeprowadzenia badań: - próbki pobrać do sterylnych butelek; - przed przystąpieniem do pobierania wody zdjąć z kurka wszelkie urządzenia, zeskrobać zanieczyszczenia, następnie całkowicie otwierając i zamykając zawór, wielokrotnie płukać; - metalowy kurek wysterylizować płomieniem, a kurek z tworzywa sztucznego alkoholem etylowym; - kurek otworzyć do połowy przepływu i spuszczać wodę przez około 2-3 minuty do osiągnięcia stałej temperatury; - pobrać próbkę wody napełniając butelkę do około ¾ objętości i natychmiast zamknąć korkiem. |
Gdzie należy przechowywać cyjanek potasu KCN?
250 cm3 roztworu kwasu octowego o stężeniu 10% objętościowych zostało rozcieńczone pięciokrotnie. Jakie jest stężenie otrzymanego roztworu?
Zestaw przedstawiony na rysunku może służyć do
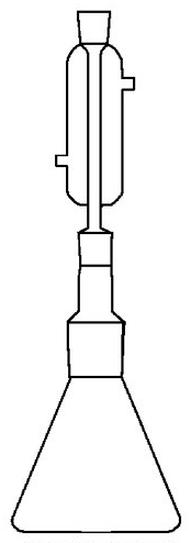
Podstawowa substancja w analizie miareczkowej charakteryzuje się następującymi właściwościami:
Który z procesów jest endotermiczny?
Preparaty zawierające KOH (tzw. żrący potaż), oznaczone są symbolem S 1/2. Na podstawie informacji zawartych w tabeli, określ zasady przechowywania tych preparatów.
| Numer zwrotu S | Warunki bezpiecznego stosowania | Numer zwrotu S | Warunki bezpiecznego stosowania |
|---|---|---|---|
| S1 | Przechowywać pod zamknięciem | S12 | Nie przechowywać pojemnika szczelnie zamkniętego |
| S2 | Chronić przed dziećmi | S13 | Nie przechowywać razem z żywnością, napojami i karmą dla zwierząt |
| S3 | Przechowywać w chłodnym miejscu | S15 | Przechowywać z dala od źródeł ciepła |
| S4 | Nie przechowywać w pomieszczeniach mieszkalnych | S16 | Nie przechowywać w pobliżu źródeł zapłonu – nie palić tytoniu |
W celu uzyskania czystej substancji próbkę zawierającą nitroanilinę poddano krystalizacji. Oblicz masę odważki nitroaniliny, pobranej do krystalizacji, jeśli uzyskano 1,5 g czystego związku, a wydajność krystalizacji wynosiła 75%.
W procesie oddzielania osadu od roztworu, po przeniesieniu osadu na sączek, najpierw należy go
Po rozpuszczeniu substancji w kolbie miarowej, należy odczekać przed dopełnieniem jej wodą "do kreski" miarowej. Taki sposób postępowania jest uzasadniony
Odczynnik, który nie został wykorzystany, należy zutylizować zgodnie z informacjami zawartymi na etykiecie
Przedstawiono wyciąg z karty charakterystyki substancji chemicznej. Na podstawie informacji zawartej w zamieszczonym fragmencie karty wskaż wzór chemiczny substancji, której można użyć jako materiału neutralizującego lodowaty kwas octowy.
Kwas octowy lodowaty 99,5% Materiały zapobiegające rozprzestrzenianiu się skażenia i służące do usuwania skażenia Jeżeli to możliwe i bezpieczne, zlikwidować lub ograniczyć wyciek (uszczelnić, zamknąć dopływ cieczy, uszkodzone opakowanie umieścić w opakowaniu awaryjnym). Ograniczyć rozprzestrzenianie się rozlewiska przez obwałowanie terenu; zebrane duże ilości cieczy odpompować. Małe ilości rozlanej cieczy przysypać niepalnym materiałem chłonnym (ziemia, piasek oraz materiałami neutralizującymi kwasy, np. węglanem wapnia lub sodu, zmielonym wapieniem, dolomitem), zebrać do zamykanego pojemnika i przekazać do zniszczenia. Zanieczyszczoną powierzchnię spłukać wodą. Popłuczyny zebrać i usunąć jako odpad niebezpieczny. |
Próbka, której celem jest ustalenie poziomu składników, dla których oznaczenia przygotowane przez różne laboratoria są niezgodne, to próbka
Na rysunku przedstawiono palnik Bunsena. Którym numerem oznaczono element do regulowania dopływu powietrza?

Rysunek przedstawia etapy zmniejszania próbki ogólnej. Jest to metoda
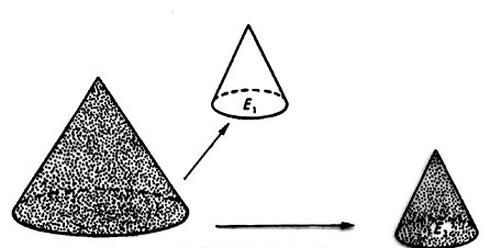
Aby oszacować czystość MgCO3, poddano prażeniu próbkę o wadze 5 g tej soli aż do osiągnięcia stałej masy. W trakcie prażenia zachodzi reakcja:
MgCO3 → MgO + CO2 Całkowity ubytek masy wyniósł 2,38 g.
(Masy molowe reagentów to: MgCO3 – 84 g/mol, MgO – 40 g/mol, CO2 – 44 g/mol) Jaką czystość miała próbka węglanu magnezu?
Aby obliczyć gęstość cieczy przy użyciu metody hydrostatycznej, należy zastosować
Zamieszczony fragment procedury opisuje sposób otrzymywania
| „W zlewce o pojemności 250 cm3 rozpuść w 50 cm3 wody destylowanej 5 g uwodnionego siarczanu(VI) miedzi(II). Do roztworu dodaj 16,7 cm3 roztworu NaOH o stężeniu 6 mol/dm3. Następnie dodaj 10 g glukozy w celu przeprowadzenia reakcji redukcji jonów miedzi(II) do miedzi(I). Ostrożnie ogrzewaj zlewkę z mieszaniną reakcyjną do otrzymania czerwonego osadu (...)Osad odsącz, przemyj alkoholem i susz na bibule na powietrzu." |
Próbki wody, które mają być badane pod kątem zawartości krzemu, powinny być przechowywane w pojemnikach
Jaką objętość powinna mieć kolba miarowa, aby przygotować mianowany roztwór NaOH o stężeniu 0,050 M z analitycznej odważki, która zawiera 0,1 mola NaOH?
Metodą, która nie umożliwia przeniesienia składników próbki do roztworu, jest
Reakcja miedzi metalicznej z stężonym kwasem azotowym(V) prowadzi do powstania azotanu(V) miedzi(II) oraz jakiego związku?
Aby przygotować 250 cm3 0,2-molowego roztworu wodorotlenku sodu, należy odważyć
| MNaOH = 40g / mol |
Którą substancję można bezpośrednio wyrzucić do odpadów komunalnych?
Na podstawie informacji zawartych w tabeli, wskaż liczbę próbek pierwotnych, które należy pobrać z partii materiału o objętości \( 100 \, \text{m}^3 \).
Wzór: \( n = 0{,}5 \cdot \sqrt{V} \)
\( V \) – objętość jednostki pobierania \( \text{m}^3 \)
\( n \) – liczba miejsc pobieranych próbek pierwotnych
Wartość \( n \) zaokrągla się do liczby całkowitej.
Minimalna liczba miejsc poboru \( n = 12 \), maksymalna \( n = 30 \)
Na rysunku pokazano przyrząd do poboru próbek
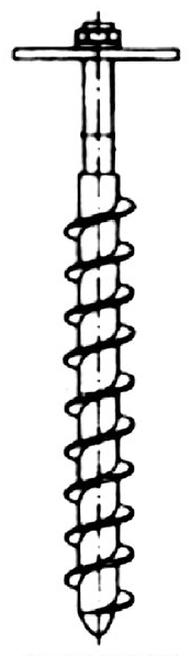
Aby wykonać czynności analityczne wskazane w ramce, należy użyć:
| Otrzymaną do badań próbkę badanego roztworu rozcieńczyć wodą destylowaną w kolbie miarowej o pojemności 100 cm3 do kreski i dokładnie wymieszać. Następnie przenieść pipetą 10 cm3 tego roztworu do kolby stożkowej, dodać ok. 50 cm3 wody destylowanej. |
Eliminacja substancji organicznych z próbki poprzez jej spalenie nazywa się