Pytanie 1
Kasety do pośredniej radiografii cyfrowej CR są wyposażone
Wynik: 33/40 punktów (82,5%)
Wymagane minimum: 20 punktów (50%)
Kasety do pośredniej radiografii cyfrowej CR są wyposażone
Wskaż roczną dawkę graniczną dla osób zatrudnionych w warunkach narażenia na promieniowanie jonizujące.
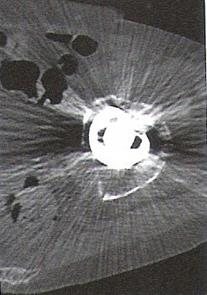
Zarejestrowany na obrazie TK artefakt jest spowodowany
Brachyterapia polegająca na wielokrotnym wsuwaniu i wysuwaniu źródła promieniowania do tego samego aplikatora nosi nazwę
Audiometria impedancyjna polega na pomiarze
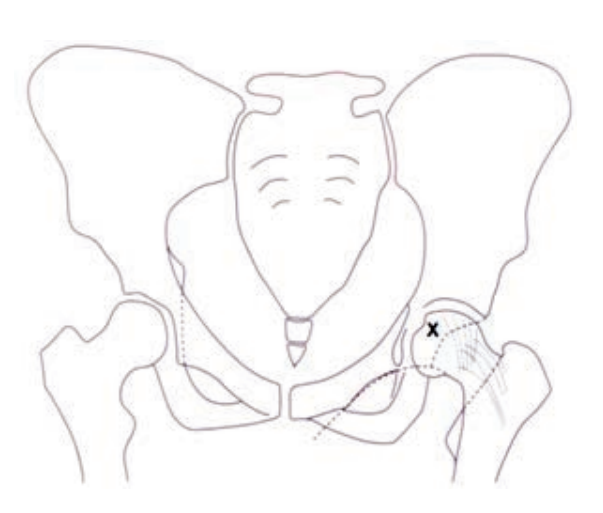
Na rycinie rentgenogramu w projekcji AP symbolem X oznaczono
Hiperfrakcjonowanie dawki w radioterapii oznacza napromienienie pacjenta
W pracowni ultrasonograficznej technik elektroradiolog nie korzysta z przepisów dotyczących
W radiografii mianem SID określa się
W celu wykonania badania scyntygraficznego układu kostnego radiofarmaceutyk należy podać pacjentowi
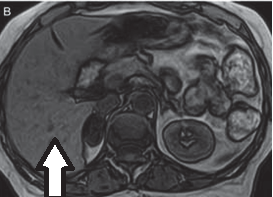
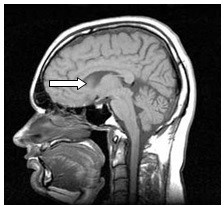
Na przekroju poprzecznym rezonansu magnetycznego strzałką oznaczono
Które obszary napromieniowania powinien określić lekarz radioterapeuta u pacjenta z nowotworem stercza po wcześniejszej prostatektomii?
Pielografia zstępująca umożliwia diagnostykę
Pomiar densytometryczny BMD metodą DXA z kręgosłupa powinien obejmować kręgi
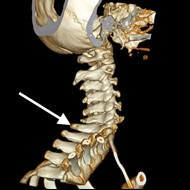
Na obrazie TK kręgosłupa strzałką wskazano wyrostek
Hałas podczas badania tomografii rezonansu magnetycznego jest efektem ubocznym pracy
Jak oznacza się w radioterapii obszar tkanek zawierający GTV i mikrorozsiewy w fazie niewykrywalnej klinicznie?
Testy podstawowe z zakresu geometrii pola rentgenowskiego, przeznaczone do sprawdzenia zgodności pola wiązki promieniowania rentgenowskiego z symulacją świetlną, są wykonywane raz
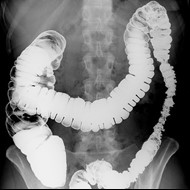
Przedstawiony obraz radiologiczny został zarejestrowany podczas badania jelita
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Źródłem promieniowania protonowego stosowanego w radioterapii jest
Który środek kontrastujący stosuje się w badaniu metodą rezonansu magnetycznego?
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
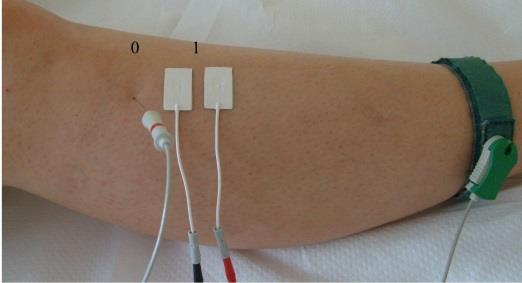
Jakie symbole mają odprowadzenia kończynowe dwubiegunowe w badaniu EKG?
Na ilustracji przedstawiono przygotowanie pacjenta do badania
Fotostymulacja wykonywana jest podczas badania
Do zdjęcia prawych otworów międzykręgowych kręgosłupa szyjnego pacjent stoi w skosie
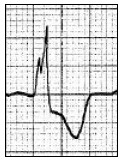
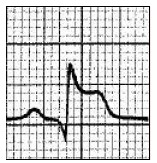
Który zapis EKG przedstawia falę Pardee'go?

Efekt „tea cup” widoczny jest na mammografach wykonanych w projekcji
Jakie wiązki promieniowania emituje medyczny akcelerator liniowy?
Badanie cewki moczowej polegające na wstecznym wprowadzeniu środka kontrastowego to
Która metoda leczenia onkologicznego zaliczana jest do leczenia systemowego?
Który załamek w zapisie EKG odpowiada zjawisku depolaryzacji przedsionków mięśnia sercowego?
Zaznaczona strzałką struktura anatomiczna na obrazie rezonansu magnetycznego to
Pomiaru impedancji akustycznej ucha środkowego dokonuje się podczas badania
Co jest przyczyną artefaktu widocznego na obrazie MR?
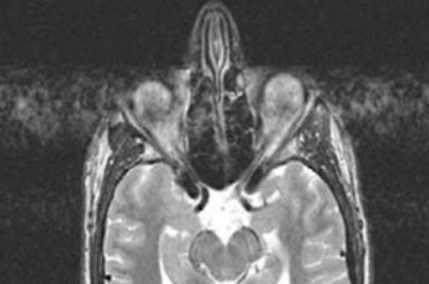
Który radioizotop jest stosowany w scyntygrafii perfuzyjnej mózgu?
Do badania mammograficznego w projekcji skośnej przyśrodkowo-bocznej kąt lampy powinien być ustawiony w zakresie
W zapisie EKG załamki P dodatnie w odprowadzeniu I i II, a ujemne w aVR oraz częstotliwość rytmu mniejsza niż 60/min wskazują na
Radioizotopowa terapia medycyny nuklearnej polega na wprowadzeniu do tkanek lub narządów radiofarmaceutyku