Pytanie 1
Centratory laserowe zamontowane w kabinie aparatu terapeutycznego służą do
Wynik: 38/40 punktów (95,0%)
Wymagane minimum: 20 punktów (50%)
Centratory laserowe zamontowane w kabinie aparatu terapeutycznego służą do
Kto jest odpowiedzialny za wykonywanie testów podstawowych kontroli jakości gammakamery w Zakładzie Medycyny Nuklearnej?
Gadolin jako dożylny środek kontrastowy stosowany w MR powoduje
Znak umieszczony w pracowni rezonansu magnetycznego zakazuje wstępu osobom

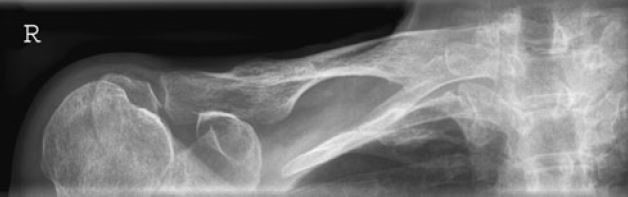
W jakiej projekcji i pod jakim kątem padania promienia centralnego został wykonany radiogram obojczyka?
Odprowadzenie EKG mierzące różnicę potencjałów między lewym podudziem a prawym przedramieniem oznacza się jako
Chorobą układu oddechowego typu obturacyjnego jest
W przypadku migotania komór w zapisie EKG występuje
Glukoza podawana pacjentowi w badaniu PET jest znakowana radioaktywnym
Wskaż osłonę radiologiczną, która jest stosowana w pracowniach radiodiagnostyki stomatologicznej.




Jaka jest odległość pomiędzy źródłem promieniowania a powierzchnią ciała pacjenta w technice izocentrycznej radioterapii?
Który system informatyczny służy do archiwizacji i transmisji obrazów radiologicznych?
Pozytywny środek cieniujący najczęściej stosowany w rentgenodiagnostyce powinien charakteryzować się
W którym okresie ciąży wykonanie u kobiety zdjęcia rentgenowskiego klatki piersiowej jest najbardziej szkodliwe dla płodu?
W celu wykonania badania scyntygraficznego układu kostnego radiofarmaceutyk należy podać pacjentowi
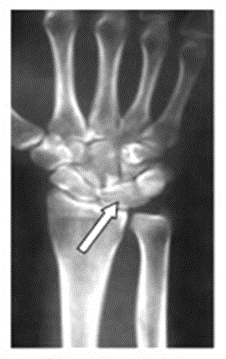
Na zamieszczonym obrazie radiologicznym nadgarstka strzałką wskazano kość
W radiografii mianem SID określa się
Który z nowotworów jest hormonozależny?
Standardowo do wykonania których zdjęć należy zastosować kratkę przeciwrozproszeniową?
Badanie przewodu pokarmowego metodą podwójnego kontrastu wiąże się z podaniem pacjentowi
Które zdjęcia należy wykonać pacjentom z chorobą reumatoidalną stawów kolanowych?
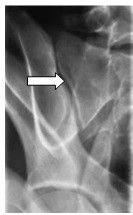
Którą strukturę anatomiczną zaznaczono strzałką na rentgenogramie?
Które odprowadzenie w badaniu EKG rejestruje różnice potencjałów pomiędzy lewym a prawym przedramieniem?
Obrazowanie portalowe w radioterapii służy do
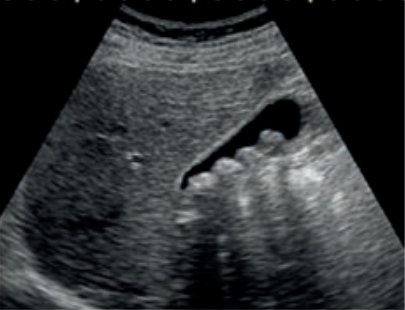
Jakie struktury anatomiczne uwidoczniono na obrazie USG?
Podczas badania EEG w systemie „10-20” literą A oznacza się elektrody
W badaniu audiometrycznym rezerwa ślimakowa to odległość między krzywą
Który typ głowicy ultrasonograficznej przedstawiono na ilustracji?

Na schemacie oznaczono
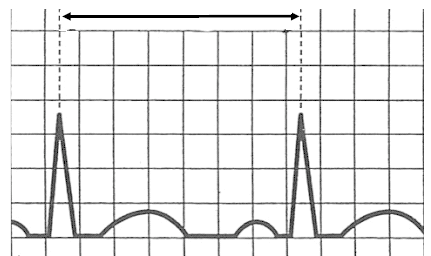
Które badanie zostało zarejestrowane na przedstawionym radiogramie?
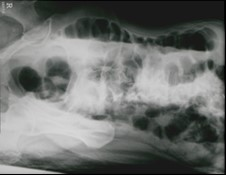
Dobierz dla standardowego pacjenta projekcję, pozycję i sposób ułożenia kasety o wymiarach 30 cm x 40 cm do zdjęcia przeglądowego układu moczowego.
| Projekcja | Pozycja | Ułożenie kasety | |||
|---|---|---|---|---|---|
| 1. | AP | 3. | stojąca | 5. | poprzeczne |
| 2. | PA | 4. | leżąca | 6. | podłużne |
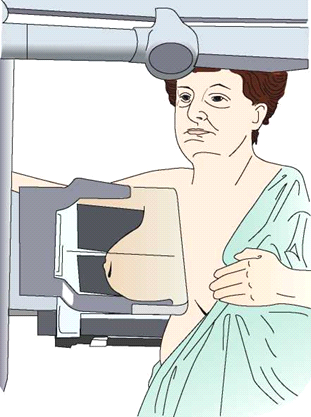
Ilustracja przedstawia pozycjonowanie pacjentki do badania mammograficznego w projekcji
Który detektor w radiografii wymaga laserowego czytnika obrazu?
Technika stereotaktyczna polega na napromienianiu nowotworu
Które obszary napromieniowania powinien określić lekarz radioterapeuta u pacjenta z nowotworem stercza po wcześniejszej prostatektomii?
W obrazowaniu MR do uwidocznienia naczyń krwionośnych jest stosowana sekwencja
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Nieostrość geometryczna obrazu rentgenowskiego zależy od
HRCT (high-resolution computed tomography) jest metodą obrazowania TK
Która metoda diagnostyczna służy do określenia gęstości minerału kostnego w ujęciu objętościowym g/cm³?