Pytanie 1
Którym skrótem w badaniu spirometrycznym oznaczana jest pojemność życiowa płuc?
Wynik: 27/40 punktów (67,5%)
Wymagane minimum: 20 punktów (50%)
Którym skrótem w badaniu spirometrycznym oznaczana jest pojemność życiowa płuc?
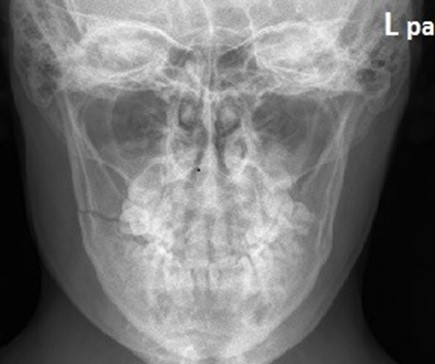
Na radiogramie żuchwy uwidoczniono złamanie w okolicy
Dobierz dla standardowego pacjenta projekcję, pozycję i sposób ułożenia kasety o wymiarach 30 cm x 40 cm do zdjęcia przeglądowego układu moczowego.
| Projekcja | Pozycja | Ułożenie kasety | |||
|---|---|---|---|---|---|
| 1. | AP | 3. | stojąca | 5. | poprzeczne |
| 2. | PA | 4. | leżąca | 6. | podłużne |
Parametrem krwi, który powinien zostać oznaczony u pacjenta przed wykonaniem badania MR z kontrastem, jest
Rak drobnokomórkowy i rak niedrobnokomórkowy to postacie organiczne nowotworów złośliwych
Który środek ochrony radiologicznej pacjenta należy zastosować podczas wykonywania zdjęcia bocznego kręgosłupa szyjnego?
Warstwa półchłonna (WP) służy do obliczania
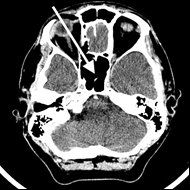
Na radiogramie TK głowy strzałką wskazano
W badaniu PET CT wykorzystuje się radioizotopy emitujące promieniowanie
W badaniu EKG różnice potencjałów pomiędzy lewym podudziem a lewym przedramieniem rejestruje odprowadzenie
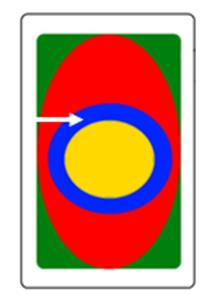
Który obszar napromieniania wskazano na ilustracji strzałką?
Do badania MR nadgarstka pacjenta należy ułożyć
Który parametr ekspozycji ma decydujący wpływ na kontrast obrazu rentgenowskiego?
Nieostrość geometryczna obrazu rentgenowskiego zależy od
Promieniowanie rentgenowskie powstaje w wyniku hamowania
Pomiaru impedancji akustycznej ucha środkowego dokonuje się podczas badania
Jak oznacza się w radioterapii obszar tkanek zawierający GTV i mikrorozsiewy w fazie niewykrywalnej klinicznie?
Glukoza podawana pacjentowi w badaniu PET jest znakowana radioaktywnym
W diagnostyce mammograficznej punktowy ucisk sutka stosuje się w projekcji
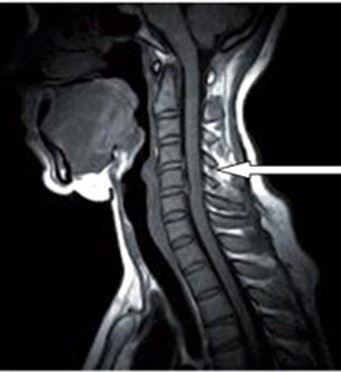
Na obrazie rezonansu magnetycznego strzałką oznaczono wyrostek kolczysty kręgu
Kiedy w procesie terapii wykonuje się badanie CBCT (cone beam computed tomography)?
Zdjęcie rentgenowskie nadgarstka w przywiedzeniu dołokciowym jest wykonywane w celu uwidocznienia kości
W radiografii mianem SID określa się
Bezwzględnym przeciwwskazaniem do badania spirometrycznego jest
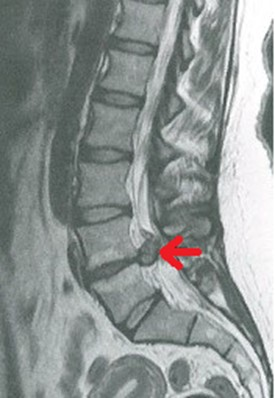
Na obrazie MR kręgosłupa lędźwiowego strzałką wskazano
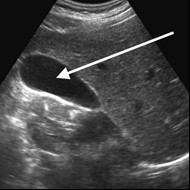
Na obrazie ultrasonograficznym jamy brzusznej strzałką wskazano
Chorobą układu oddechowego typu obturacyjnego jest
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
W trakcie obrazowania metodą rezonansu magnetycznego wykorzystywane jest zjawisko wysyłania sygnału emitowanego przez
Cholangiografia to badanie radiologiczne
Miejscem wykonania pomiaru densytometrycznego z kości przedramienia jest
Podstawowym elementem diagnostycznym aparatury izotopowej wykorzystującej emisyjne metody pomiaru jest
Badanie gęstości mineralnej kości metodą DXA należy wykonać
Skrótem CTV w radioterapii oznacza się
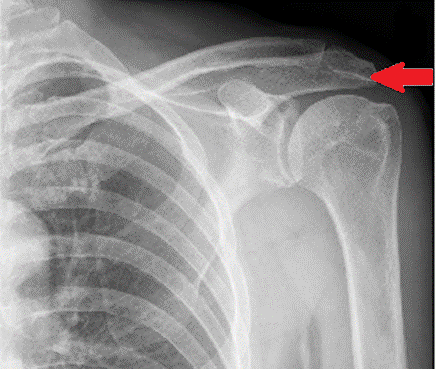
Na radiogramie stawu barkowego strzałką wskazano
Do planowego badania TK klatki piersiowej z użyciem środka cieniującego pacjent powinien zgłosić się
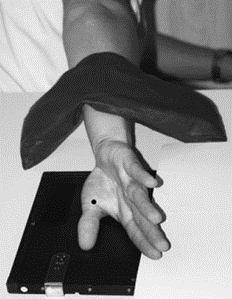
Na ilustracji przedstawiono ułożenie pacjenta do zdjęcia rentgenowskiego
Który system informatyczny służy do archiwizacji i transmisji obrazów radiologicznych?
Który załamek w zapisie EKG odpowiada zjawisku depolaryzacji przedsionków mięśnia sercowego?
Który radioizotop stosuje się do badania scyntygraficznego kości?