Pytanie 1
Fosfor biały, z uwagi na swoje właściwości, powinien być przechowywany
Wynik: 25/40 punktów (62,5%)
Wymagane minimum: 20 punktów (50%)
Fosfor biały, z uwagi na swoje właściwości, powinien być przechowywany
W wyniku analizy sitowej próbki stałej otrzymano frakcję o średnicy ziaren 12 – 30 mm. Jaką masę powinna mieć prawidłowo pobrana próbka pierwotna?
| Tabela. Wielkość próbki pierwotnej w zależności od wielkości ziarna | ||||
|---|---|---|---|---|
| Średnica ziaren lub kawałków [mm] | do 1 | 1 - 10 | 11 - 50 | ponad 50 |
| Pierwotna próbka (minimum) [g] | 100 | 200 | 1000 | 2500 |
Jaka minimalna pojemność powinna mieć miarka, aby jednorazowo zmierzyć 60,0 cm3 wody?
Przykładem piany stałej jest
| faza rozproszona | faza rozpraszająca | ||
|---|---|---|---|
| gaz | ciecz | ciało stałe | |
| gaz | - | piana | piana stała |
| ciecz | aerozol ciekły | emulsja | emulsja stała |
| ciało stałe | aerozol stały | zol | zol stały |
W probówce połączono roztwory CuSO4 oraz NaOH. Powstał niebieski osad, który po podgrzaniu zmienił kolor na czarny. Czarnym osadem jest
W laboratoriach roztwór potasu dichromianu(VI) w stężonym kwasie siarkowym(VI) wykorzystuje się do
Substancja oznakowana za pomocą przedstawionych na rysunku piktogramów jest

W standardowym układzie destylacyjnym, który ma ukośną chłodnicę, wykorzystuje się chłodnicę
Naczynia miarowe o kształcie rurek poszerzonych w środku, z wąskim i wydłużonym dolnym końcem, przeznaczone do pobierania i transportowania cieczy o ściśle określonej objętości, to
Aby oddzielić połączenia szlifów, należy w miejscu ich styku wprowadzić
Zastosowanie łaźni wodnej nie jest zalecane w trakcie prac, w których stosuje się
Reagenty o najwyższej czystości to reagenty
Roztwory o ściśle określonym stężeniu, używane w analizach miareczkowych, nazywamy
Wykorzystując pipetę gazową, pobrano próbkę azotu (Mn2 = 28 g/mol) o objętości 250 cm3 w standardowych warunkach. Jaką masę ma zmierzony azot?
W celu przygotowania 100 cm3 roztworu mianowanego, jaką kolbę należy zastosować?
Jakim przyrządem nie jest możliwe określenie gęstości cieczy?
Na podstawie danych zawartych w tabeli wskaż, które opakowania zawierają produkt zgodny ze specyfikacją.
| WŁAŚCIWOŚCI | NORMA KLASY A wg specyfikacji produktu | OPAKOWANIE | ||
|---|---|---|---|---|
| 1 | 2 | 3 | ||
| POSTAĆ | Bezbarwna ciecz, bez zanieczyszczeń. Dopuszcza się niebieskawе zabаrwienie i obecność skrystalizowanego osadu | Bezbarwna ciecz | ||
| Zawartość ługu sodowego (NaOH), min, % masy | 46,0 | 46,5 | 46,8 | 48,0 |
| Węglan sodu (Na₂CO₃), nie więcej niż, % masy | 0,4 | 0,3 | 0,3 | 0,2 |
| Chlorek sodu (NaCl), nie więcej niż, % masy | 0,020 | 0,015 | 0,014 | 0,011 |
| Chloran sodu (NaClO₃), nie więcej niż, % masy | 0,007 | 0,006 | 0,005 | 0,002 |
| Siarczan sodu (Na₂SO₄), nie więcej niż, % masy | 0,040 | 0,038 | 0,035 | 0,029 |
| Zawartość żelaza (Fe₂O₃), max, WT. PPM | 15 | 15 | 15 | 10 |
Ustalanie miana roztworu polega na
Poniżej jest równanie reakcji prażenia węglanu wapnia. 200 g węglanu wapnia zawierającego 10% zanieczyszczeń poddano prażeniu. Masa otrzymanego tlenku wapnia wyniosła
| CaCO3 → CaO + CO2 |
| (MCaCO3 = 100 g/mol, MCaO = 56 g/mol, MCO2 = 44 g/mol) |
Aby przygotować 150 g roztworu jodku potasu o stężeniu 10% (m/m), konieczne jest użycie
(zakładając, że gęstość wody wynosi 1 g/cm3)
Aby oszacować czystość MgCO3, poddano prażeniu próbkę o wadze 5 g tej soli aż do osiągnięcia stałej masy. W trakcie prażenia zachodzi reakcja:
MgCO3 → MgO + CO2 Całkowity ubytek masy wyniósł 2,38 g.
(Masy molowe reagentów to: MgCO3 – 84 g/mol, MgO – 40 g/mol, CO2 – 44 g/mol) Jaką czystość miała próbka węglanu magnezu?
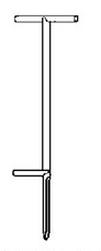
Przedstawiony na rysunku zagłębnik stosuje się do pobierania próbek
Co oznacza skrót AKT?
Woda używana w laboratorium chemicznym, uzyskana poprzez filtrację przez wymieniacz jonowy, jest określana mianem wody
Zawarty fragment instrukcji odnosi się do
Po dodaniu do kolby Kjeldahla próbki analizowanego materiału, kwasu siarkowego(VI) oraz katalizatora, należy delikatnie ogrzewać zawartość kolby za pomocą palnika gazowego. W początkowym etapie ogrzewania zawartość kolby wykazuje pienienie i zmienia kolor na ciemniejszy. W tym czasie należy przeprowadzać ogrzewanie bardzo ostrożnie, a nawet z przerwami, aby uniknąć "wydostania się" czarnobrunatnej masy do szyjki kolby.
Którego odczynnika należy użyć do przygotowania roztworu wzorcowego, zawierającego jony \( \text{Fe}^{3+} \)?
Średnia masa wody wypływająca z pipety o deklarowanej pojemności 25 cm3, w temperaturze 25°C wynosi 24,80 g. Korzystając z danych zamieszczonych w tabeli wskaż wartość poprawki kalibracyjnej dla tej pipety.
| Masa wody zajmującej objętość 1 dm3 w zależności od temperatury pomiaru | |
|---|---|
| Temperatura °C | Masa wody g |
| 20 | 997,17 |
| 21 | 997,00 |
| 22 | 996,80 |
| 23 | 996,59 |
| 24 | 996,38 |
| 25 | 996,16 |
| 26 | 995,93 |
| 27 | 995,69 |
| 28 | 995,45 |
| 29 | 995,18 |
| 30 | 994,92 |
Część partii pobrana w sposób jednorazowy z jednego źródła towaru zapakowanego lub z jednego opakowania jednostkowego określana jest mianem próbki
Piktogram nie jest konieczny dla
Na podstawie informacji zawartej na pipecie, została ona skalibrowana na
Aby przyspieszyć reakcję, należy zwiększyć stężenie substratów
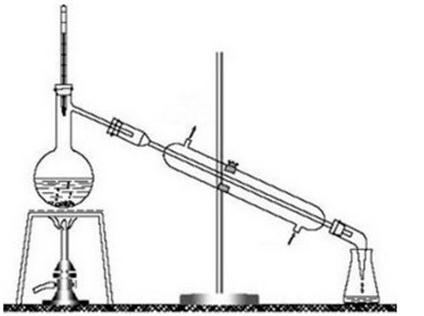
Na rysunku przedstawiono zestaw do
Ile gramów cukru trzeba dodać do 200 gramów wody o temperaturze 20°C, aby uzyskać roztwór nasycony?
Zamieszczony piktogram przedstawia substancję o klasie i kategorii zagrożenia:

Komora przeszklona w formie dużej szafy, wyposażona w wentylator, która zapobiega wydostawaniu się szkodliwych substancji do atmosfery laboratorium oraz chroni przed pożarami i eksplozjami, to
Chemikalia, dla których upłynął okres przydatności,
Roztwór amoniaku o stężeniu 25% nie powinien być trzymany
Sączenie na gorąco powinno być użyte, aby
Jakim kolorem zazwyczaj oznacza się przewody w instalacji gazowej w laboratorium?
Podczas oznaczania kwasu siarkowego zachodzi reakcja:
H2SO4 + 2NaOH → Na2SO4 + 2H2OZgodnie z zamieszczoną instrukcją, roztwór poreakcyjny należy
| Fragmenty instrukcji zbierania, utylizacji i eliminacji odpadów chemicznych | |
|---|---|
| Lista substancji, które mogą być usunięte z odpadami komunalnymi w postaci stałej, lub wprowadzone do systemu kanalizacyjnego w postaci rozcieńczonych roztworów wodnych, o ile ich ilość nie przekracza jednorazowo 100 g. | |
| Związki nieorganiczne Siarczany sodu, potasu, magnezu, wapnia, amonu | |
| Kwasy nieorganiczne Stężone kwasy ostrożnie rozcieńczyć przez wkroplenie z równoczesnym mieszaniem do wody z lodem, a następnie zneutralizować roztworem wodorotlenku sodowego. Po neutralizacji doprowadzić pH roztworu do zakresu 6-8 przelać do pojemnika S. Małe ilości kwasów takich jak siarkowy, solny, azotowy czy fosforowy (nie więcej niż 10 g) po rozcieńczeniu wodą i neutralizacji roztworem wodorotlenku sodowego oraz doprowadzeniu pH takiego roztworu do zakresu 6-8 można wylać do zlewu i obficie spłukać wodą. | |
| Sole nieorganiczne Stałe sole nieorganiczne – pojemnik N. Obojętne roztwory soli nieorganicznych pojemnik S. Sole metali ciężkich, sole o właściwościach toksycznych – pojemnik TN. |