Pytanie 1
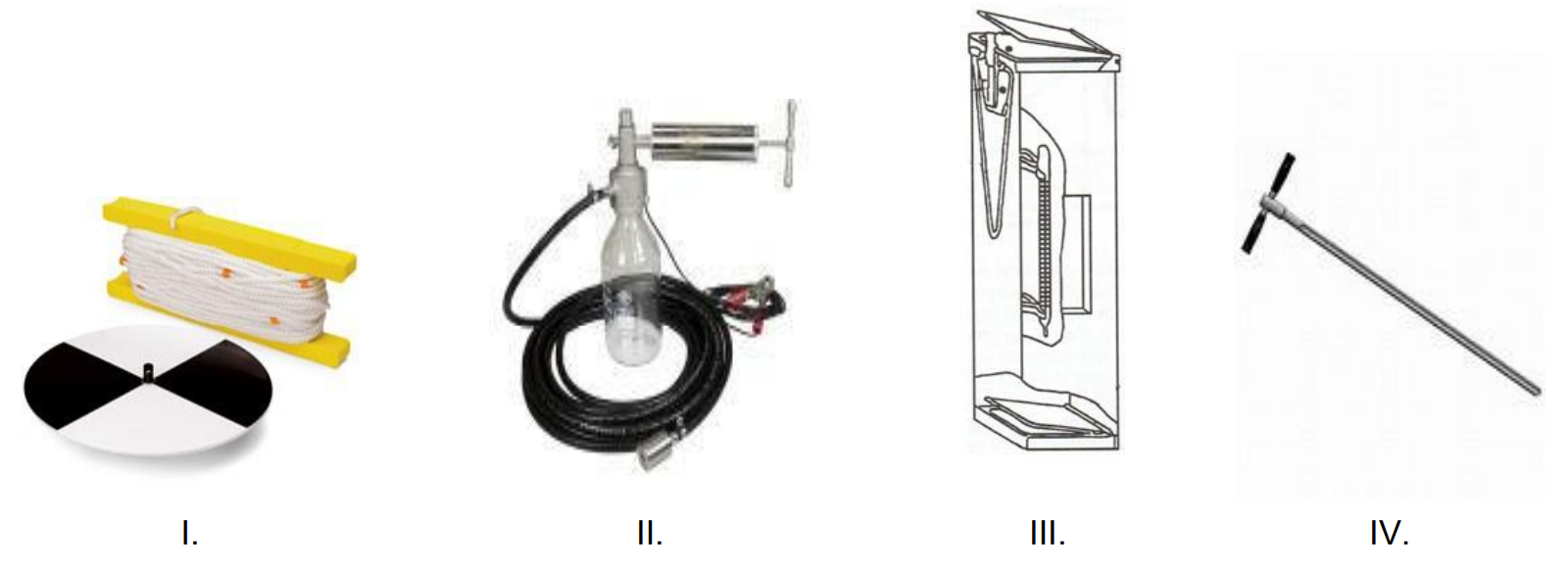
Na którym rysunku przedstawiono sprzęt stosowany do pomiaru mętności wody?
Wynik: 16/40 punktów (40,0%)
Wymagane minimum: 20 punktów (50%)
Na którym rysunku przedstawiono sprzęt stosowany do pomiaru mętności wody?

Na etykiecie odczynnika chemicznego zawarte są następujące informacje:
Z informacji wynika, że odczynnik ten może być zastosowany do sporządzenia roztworu o stężeniu około 0,1 mol/dm3 z dokładnością do
| NH4SCN amonu tiocyjanian | 0,1 mol/l |
| Stężenie po rozcieńczeniu do 1000 ml w 20°C | 0,1 mol/l ± 0,2 % |
Jaką metodę kontroli stanu mikrobiologicznego powietrza opisano w zamieszczonej informacji?
| Otwarte płytki Petriego z podłożem stałym pozostawiono na 30 minut na wysokości 1 metra od podłogi, a następnie inkubowano przez 48 godzin w temperaturze 37°C. Po tym czasie wyhodowane kolonie zliczono i zidentyfikowano ich szczepy. |
W zamieszczonej informacji przedstawiono równania reakcji zachodzące podczas oznaczania chlorków metodą
| Ag+ + Cl- → AgCl ↓ Ag+ + SCN- → AgSCN ↓ Fe3+ + SCN- → Fe(SCN)2+ |
Próbkę tłuszczu poddano reakcji z wodą bromową. Nie zaobserwowano zmian. Wskaż wzór tłuszczu, który mógł znajdować się w tej próbce.
Ogólna twardość próbki wody stosowanej w technologiach wynosi 16,5°n, a twardość węglanowa osiąga 7,2°n. Jaką wartość ma twardość stała?
Rolę wskaźnika w oznaczeniu opisanym w ramce pełni
| Do kolby miarowej o pojemności 250 cm3 odpipetować 25 cm3 3% wody utlenionej i dopełnić wodą do kreski. Do kolby stożkowej o pojemności 250 cm3 odpipetować 20 cm3 próbki rozcieńczonej wody utlenionej, dodać 25 cm3 kwasu siarkowego(VI) (1+4) i miareczkować roztworem manganianu(VII) potasu o stężeniu 0,02 mol/dm3 do pojawienia się trwałego różowego zabarwienia. |
Zjawisko dzielenia się składników mieszaniny pomiędzy fazę stacjonarną a ruchomą w układzie to proces widoczny w
Oznaczanie wagowe substancji jest możliwe, kiedy analizowany związek jest
Czym charakteryzuje się barwa roztworu zawierającego jony Cr2O72-?
Substancją służącą do wykrywania chlorków w analizach jakościowych jest
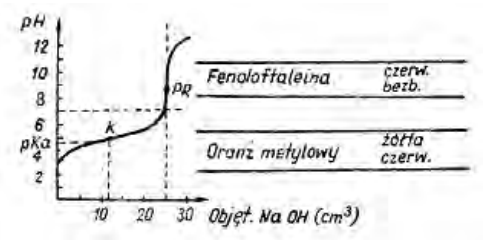
Zamieszczony wykres przedstawia krzywą miareczkowania
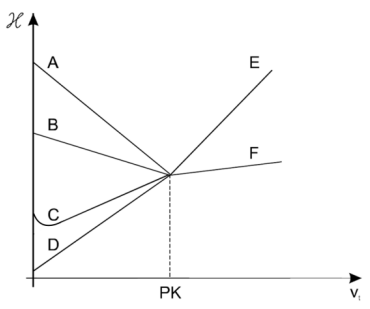
Zawartość kwasu octowego oznaczano alkacymetrycznie, mierząc zmiany przewodnictwa właściwego mieszaniny reakcyjnej w wyniku dodawania roztworu NaOH. Przebieg miareczkowania przedstawiają linie
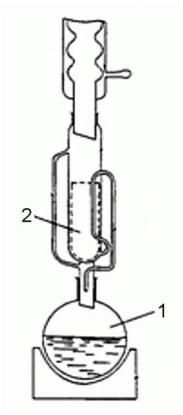
W celu przeprowadzenia oznaczenia za pomocą aparatu przedstawionego na ilustracji surowiec roślinny umieszcza się w
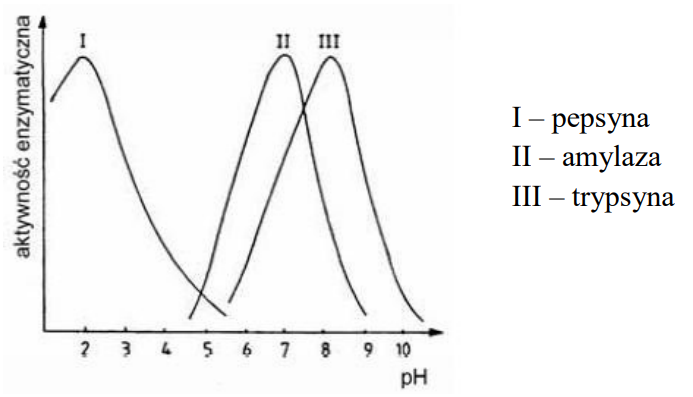
Na wykresie przedstawiono zależność aktywności enzymów od pH. Optimum aktywności amylazy występuje przy pH
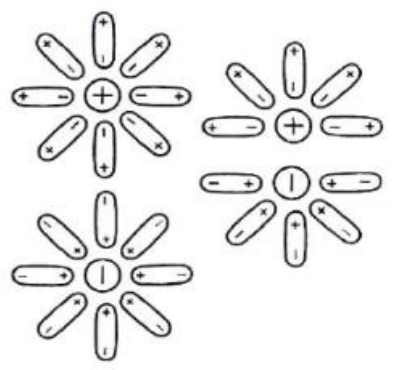
Na rysunku przedstawiono schemat procesu
W kulturze bakterii i grzybów nie należy używać jako pożywki
Jakiego rodzaju proces uzdatniania wody ilustrują podane równania reakcji chemicznych?
CO2 + Ca(OH)2 → CaCO3 + H2O Ca(HCO3)2 + Ca(OH)2 → 2CaCO3 + 2H2O
Maksymalne dopuszczalne poziomy dozwolonych substancji dodatkowych stosowanych w wybranych środkach spożywczych. W próbkach dżemów A, B, C, D oznaczono zawartość substancji dodatkowych. Na podstawie wyników przeprowadzonej analizy, wskaż próbkę dżemu, która nie spełnia podanych wymagań.
| Numer wg systemu oznaczeń Unii Europejskiej | Nazwa | Środek spożywczy | Maksymalny poziom mg/kg |
|---|---|---|---|
| E 210 E 211 | Kwas benzoesowy Benzoesan sodu | Niskocukrowe dżemy, galaretki, marmolady i podobne produkty niskokaloryczne lub bez dodatku cukru i inne produkty smarowne na bazie owoców. | 500 |
| E 220 | Dwutlenek siarki | Dżemy, galaretki, marmolady i podobne produkty smarowne łącznie z produktami niskokalorycznymi. | 50 |
| E 104 | Żółcień chinolinowa | 100 | |
| E 961 | Neotam | Dżemy, galaretki owocowe i marmolady. | 32 |
| Wyniki przeprowadzonej analizy | ||||
|---|---|---|---|---|
| Numer wg systemu oznaczeń Unii Europejskiej | Oznaczona ilość mg/kg | |||
| A. | B. | C. | D. | |
| E 104 | 65,2 | 58,5 | 74,8 | 57,5 |
| E 210 | 458,5 | 498,7 | 487,0 | 423,8 |
| E 220 | 38,0 | 47,8 | 52,0 | 25,0 |
| E 961 | 3,5 | 25,9 | 32,7 | 16,9 |
Na rysunku przedstawiono sprzęt stosowany do
Na podstawie informacji zamieszczonych w tabeli wskaż wzór związku, który wytrąci się w postaci osadu.
| Badany kation | Odczynnik grupowy | NaOH | Barwienie płomienia |
|---|---|---|---|
| Mg2+ | brak | biały osad | |
| K+ | brak | fiołkowy | |
| Na+ | brak | żółty |
Na podstawie zamieszczonego fragmentu opisu wykonania ćwiczenia ustal, który wskaźnik jakości wody jest określany.
| Oznaczenie polega na określeniu ilości tlenu zużywanej do utleniania substancji organicznych w badanej próbce w ciągu n dób inkubacji w temperaturze 20°C. Ilość tę, w przeliczeniu na 1 dm³ wody, oblicza się jako różnicę zawartości tlenu przed i po inkubacji próbki. |
Do metod instrumentalnych w analizach jakościowych nie zaliczają się techniki
Iloczyn rozpuszczalności trudno rozpuszczalnego związku Ca3(PO4)2 wyrażony jest równaniem:
| A. | KSO = [Ca2+] · [PO43-] |
| B. | KSO = [Ca3+]2 · [PO42-]3 |
| C. | KSO = [Ca2+]3 · [PO43-]2 |
| D. | KSO = 3[Ca2+] · 2[PO43-] |
Równanie przedstawia reakcję zachodzącą podczas oznaczania żelaza metodą miareczkowania
| 5Fe2+ + MnO4- + 8H+ ⇆ 5Fe3+ + Mn2+ + 4H2O |
Do optycznych metod instrumentalnych wykorzystywanych w chemicznej analizie zalicza się
Numerem 6 na rysunku oznaczono
Zamieszczona instrukcja dotyczy wykonania preparatu mikroskopowego
| 1. Materiał nanieść na szkiełko podstawowe. 2. Po wyschnięciu, preparat utrwalić przez przeciągnięcie szkiełka podstawowego nad płomieniem palnika spirytusowego. 3. Następnie nanieść na szkiełko roztwór błękitu metylenowego i pozostawić do wyschnięcia. 4. Spłukać wodą destylowaną, pozostawić preparat do wyschnięcia. |
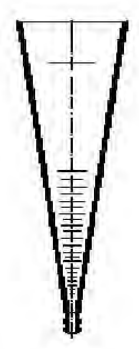
Jedna z analizowanych cech jakości wody ma wartość 0,8 NTU. Cechą tą jest
Na którym rysunku przedstawiono schemat metody dokładnej i nieprecyzyjnej?
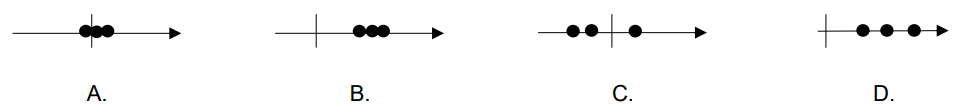
Na rysunku przedstawiono kolbę
Roztwór zawierający aniony I grupy analitycznej poddano identyfikacji metodą chromatografii cienkowarstwowej. Na chromatogramie uwidoczniono dwie plamki w odległości 5,6 cm i 3,5 cm od linii startu. Odległość czoła eluenta od linii startu wyniosła 10,1 cm, a wartości wskaźników Rf wzorców anionów wynoszą jak w tabeli. Które z anionów zawierała badana próbka?
| Anion | Cl- | Br- | I- | SCN- |
|---|---|---|---|---|
| Wskaźnik Rf | 0,243 | 0,352 | 0,554 | 0,648 |
Lepkość oleju napędowego w temperaturze 40°C wynosi 3 mm2/s. Jaką lepkość to określa?
Twardość całkowita wody
Na schemacie przedstawiającym sposób pobierania hodowli do badań ze skosu agarowego literą D oznaczono
Znając zasadę działania polarymetru i wzór - można oznaczyć stężenie
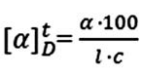
Przedstawione reakcje zachodzą w produktach żywnościowych podczas fermentacji
| C12H22O11 + H2O → C6H12O6 + C6H12O6 |
| C6H12O6 → 2 CH3 −CH(OH) −COOH |
Białka, których cząsteczki mają wiązania peptydowe, w reakcji z jonami miedzi(II) w środowisku zasadowym tworzą kompleks o barwie fioletowej. Stopień intensywności barwy jest proporcjonalny do liczby wiązań peptydowych. Tę zależność można wykorzystać do oznaczeń
W celu identyfikacji cukru sporządzono jego roztwór i przelano do trzech probówek. Następnie przeprowadzono doświadczenia, których wyniki zapisano w tabeli:
Badanym cukrem była
| Badany roztwór | Dodany odczynnik | Obserwacje |
|---|---|---|
| Probówka 1. | Cu(OH)2 | Zawiesina Cu(OH)2 rozpuściła się, a roztwór przyjął szafirową barwę |
| Cu(OH)2 | Po ogrzaniu probówki pojawił się ceglasto-czerwony osad | |
| Probówka 2. | [Ag(NH3)2]+ | Po ogrzaniu na ściankach probówki pojawiło się srebro metaliczne |
| Probówka 3. | Br2(aq) + roztwór NaHCO3 | Woda bromowa uległa odbarwieniu |
W ramce przedstawiono równania reakcji zachodzące podczas pośredniego jodometrycznego oznaczania
| 2Cu2+ + 4I- →2CuI + I2 I2 + S2O32- → 2I- + S4O62- |