Pytanie 1
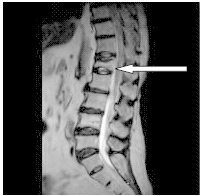
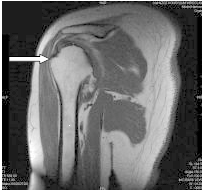
Na obrazie rezonansu magnetycznego strzałką oznaczono patologiczny kręg
Wynik: 31/40 punktów (77,5%)
Wymagane minimum: 20 punktów (50%)
Na obrazie rezonansu magnetycznego strzałką oznaczono patologiczny kręg

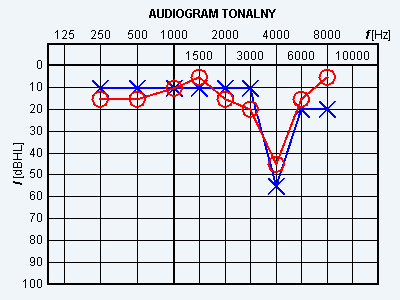
Wynik badania słuchu metodą audiometrii tonalnej wskazuje na
W radioterapii konwencjonalnej pacjent jest leczony promieniowaniem pochodzącym
Jednym z kryteriów poprawnie wykonanego badania spirometrycznego jest czas trwania natężonego wydechu, który powinien wynosić u osób powyżej 10 roku życia co najmniej
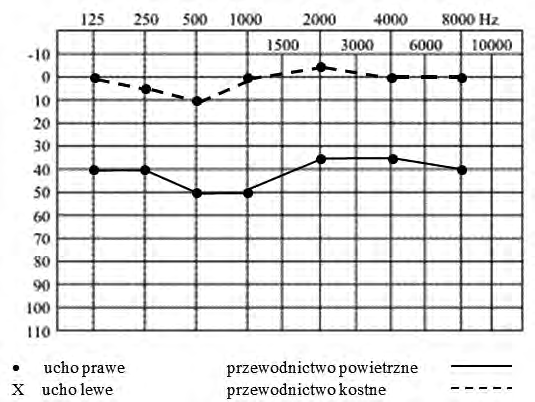
Na podstawie zapisu badania audiometrycznego rozpoznano u pacjenta uszkodzenie słuchu
W radiologii analogowej lampy rentgenowskiej z tubusem używa się do wykonania zdjęcia
W brachyterapii MDR stosowane są dawki promieniowania
Odprowadzenie II rejestruje różnicę potencjałów między
Podczas badania EEG w systemie „10-20” literą A oznacza się elektrody
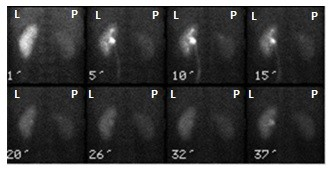
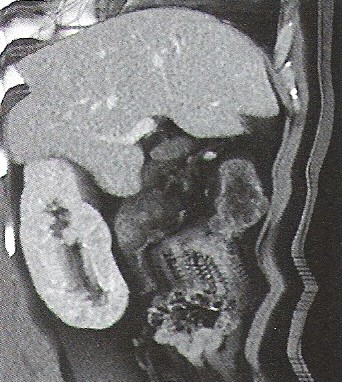
Na zarejestrowanych obrazach badania renoscyntygraficznego widać, że prawa nerka pacjenta
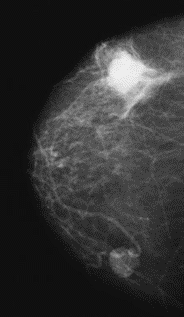
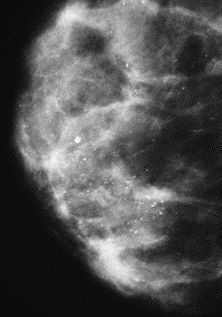
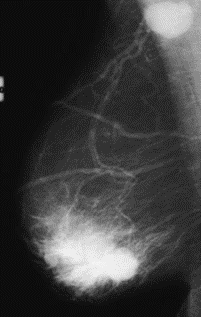
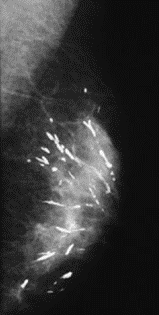
Na którym obrazie rentgenowskim sutka uwidoczniono zmianę patologiczną w obrębie węzłów chłonnych?
Folia wzmacniająca umieszczona w kasecie rentgenowskiej emituje pod wpływem promieniowania X światło
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem
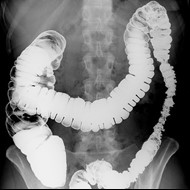
Przedstawiony obraz radiologiczny został zarejestrowany podczas badania jelita
Jaki rozmiar kasety należy zastosować, wykonując standardowe zdjęcie stawu kolanowego w projekcji bocznej?
W której projekcji należy wykonać badanie radiologiczne kręgosłupa lędźwiowego, by na otrzymanym zdjęciu wyrostki kręgów lędźwiowych układały się w charakterystyczny kształt piesków (teriera szkockiego)?
Zdjęcie zatok przynosowych wykonuje się w pozycji
Źródłem promieniowania protonowego stosowanego w radioterapii jest
Wskazaniem do wykonania badania spirometrycznego jest
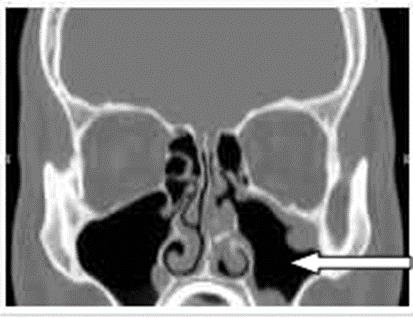
Na zamieszczonym obrazie TK strzałką zaznaczono zatokę
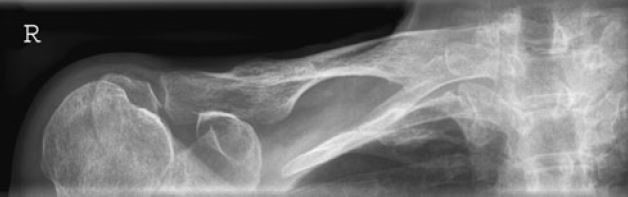
W jakiej projekcji i pod jakim kątem padania promienia centralnego został wykonany radiogram obojczyka?
Odprowadzenie EKG mierzące różnicę potencjałów między lewym podudziem a prawym przedramieniem oznacza się jako
Gadolin jako dożylny środek kontrastowy stosowany w MR powoduje
Podczas wykonywania badania EKG czarną elektrodę kończynową należy umieścić na kończynie dolnej
Warstwa półchłonna (WP) służy do obliczania
Którym skrótem oznacza się tomografię komputerową wysokiej rozdzielczości?
Droga przewodnictwa powietrznego fali akustycznej przebiega przez
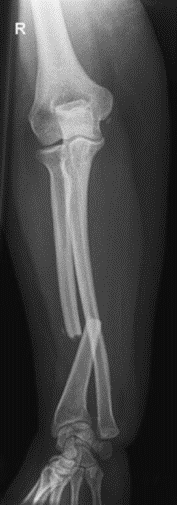
Na radiogramie uwidoczniono złamanie
Którą strukturę anatomiczną oznaczono na obrazie rezonansu magnetycznego?
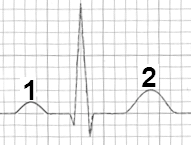
Na schemacie oznaczono
Który radiofarmaceutyk może zostać podany pacjentowi w scyntygrafii perfuzyjnej mózgu?
Pracownia radioterapii z przyspieszaczem liniowym jest obszarem
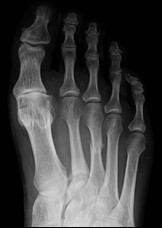
Na radiogramie stopy uwidocznione jest złamanie trzonu
Którą ochronę radiologiczną należy zastosować podczas wykonywania zdjęcia rentgenowskiego przeglądowego klatki piersiowej u pacjentki w okresie rozrodczym?
W pozytonowej tomografii emisyjnej PET zostaje zarejestrowane promieniowanie powstające podczas
Parametrem krwi, który powinien zostać oznaczony u pacjenta przed wykonaniem badania MR z kontrastem, jest
W jaki sposób należy oprzeć stroik w audiometrycznym badaniu przewodnictwa kostnego?
Wskazaniem do zastosowania brachyterapii w leczeniu radykalnym jest rak
Na którym obrazie TK uwidoczniony jest artefakt spowodowany ruchami oddechowymi pacjenta?
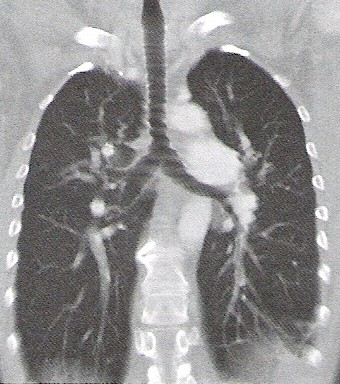

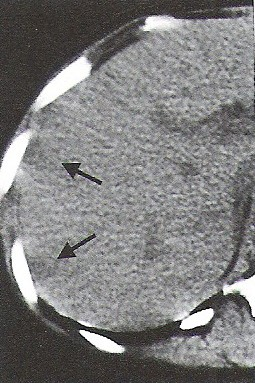
Hiperfrakcjonowanie dawki w radioterapii oznacza napromienienie pacjenta