Pytanie 1
Jakie struktury anatomiczne uwidoczniono na obrazie USG?
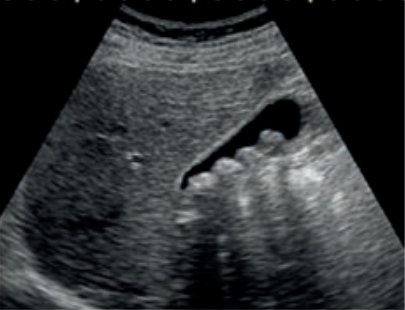
Wynik: 40/40 punktów (100,0%)
Wymagane minimum: 20 punktów (50%)
Jakie struktury anatomiczne uwidoczniono na obrazie USG?

Na obrazie radiologicznym nadgarstka uwidoczniono złamanie nasady
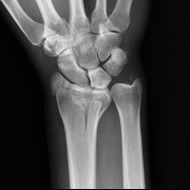
Na radiogramie stopy strzałką wskazano kość
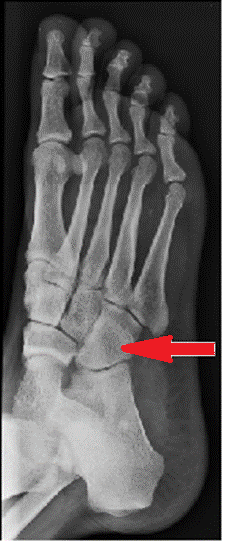
W trakcie obrazowania metodą rezonansu magnetycznego wykorzystywane jest zjawisko wysyłania sygnału emitowanego przez
Przyczyną zaniku kostnego jest
Bezwzględnym przeciwwskazaniem do wykonania badania rezonansem magnetycznym jest
Na zamieszczonym przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano

W badaniu EEG elektrody referencyjne przymocowane do płatka ucha to
Pomiaru impedancji akustycznej ucha środkowego dokonuje się podczas badania
Na obrazie radiologicznym uwidoczniono złamanie kości
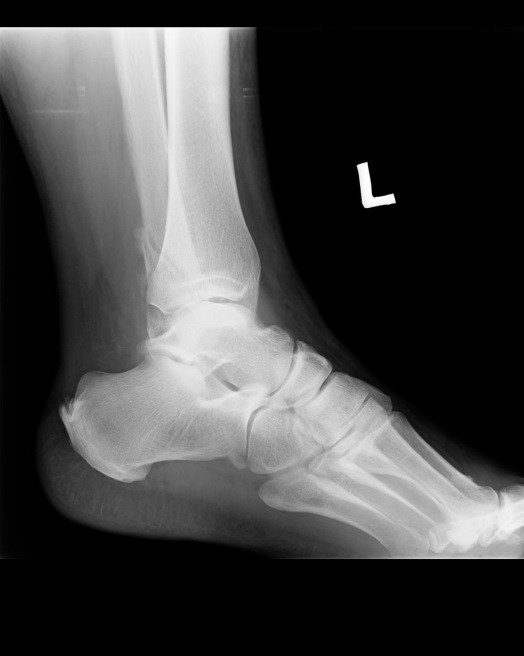
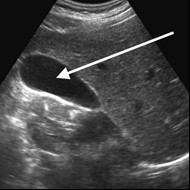
Na obrazie ultrasonograficznym jamy brzusznej strzałką wskazano
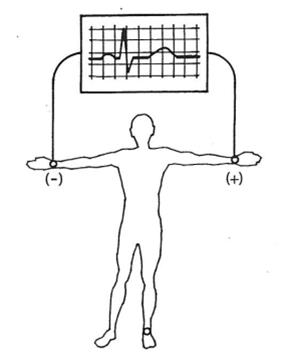
Które odprowadzenie elektrokardiograficzne przedstawiono na ilustracji?
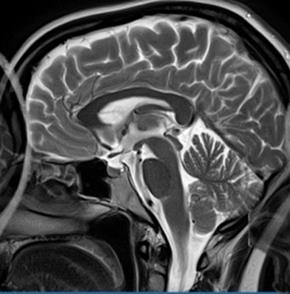
Którym skrótem oznacza się tomografię komputerową wysokiej rozdzielczości?
Wskaż przyczynę powstania artefaktu widocznego na obrazie MR.
Jaki jest cel stosowania bolusa w radioterapii?
Zamieszczony elektrokardiogram przedstawia
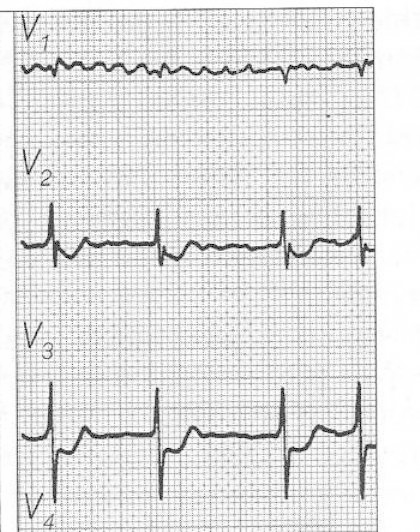
Który załamek w zapisie EKG odpowiada zjawisku depolaryzacji przedsionków mięśnia sercowego?
Źródłem promieniowania protonowego stosowanego w radioterapii jest
Na którym obrazie TK uwidoczniony jest artefakt spowodowany ruchami oddechowymi pacjenta?
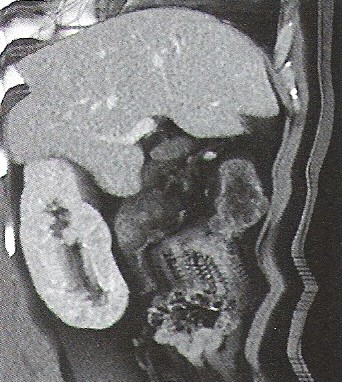

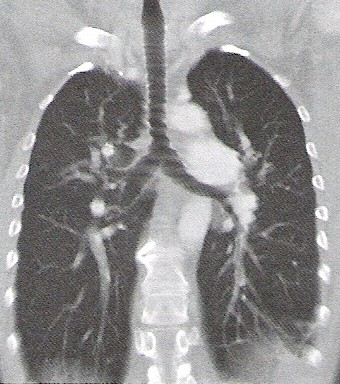
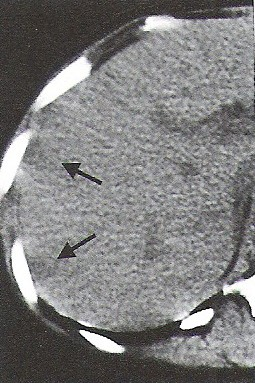
Do prób aktywacyjnych stosowanych w badaniu EEG zalicza się
Jednostką indukcji magnetycznej jest
Zdjęcie rentgenowskie nadgarstka w przywiedzeniu dołokciowym jest wykonywane w celu uwidocznienia kości
Technik elektroradiolog do badania MR kręgosłupa lędźwiowego powinien ułożyć pacjenta:
W zapisie EKG linia izoelektryczna obrazuje
Fala głosowa rozchodzi się
W radioterapii hadronowej leczenie odbywa się przy użyciu
Na przedstawionym scyntygramie ukazano duży obszar
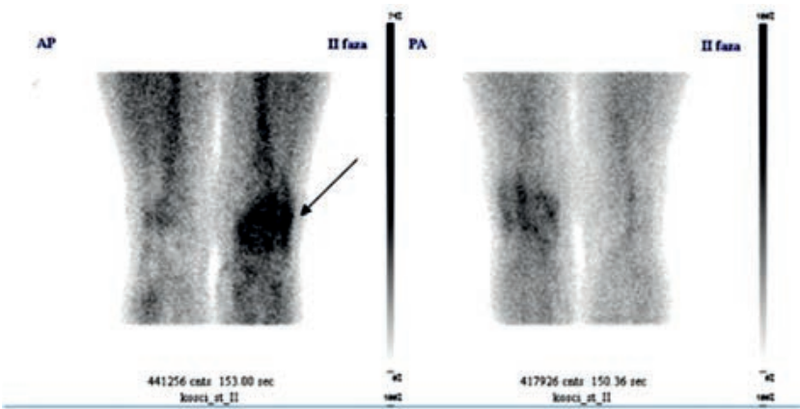
Jednym z kryteriów poprawnie wykonanego badania spirometrycznego jest czas trwania natężonego wydechu, który powinien wynosić u osób powyżej 10 roku życia co najmniej
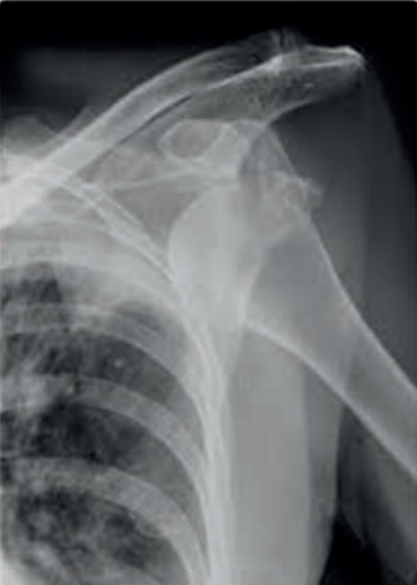
Którą patologię uwidoczniono na zamieszczonym rentgenogramie?
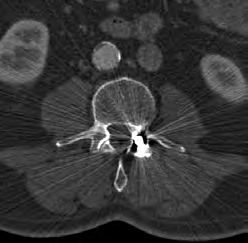
Który artefakt jest widoczny na skanie tomografii komputerowej?
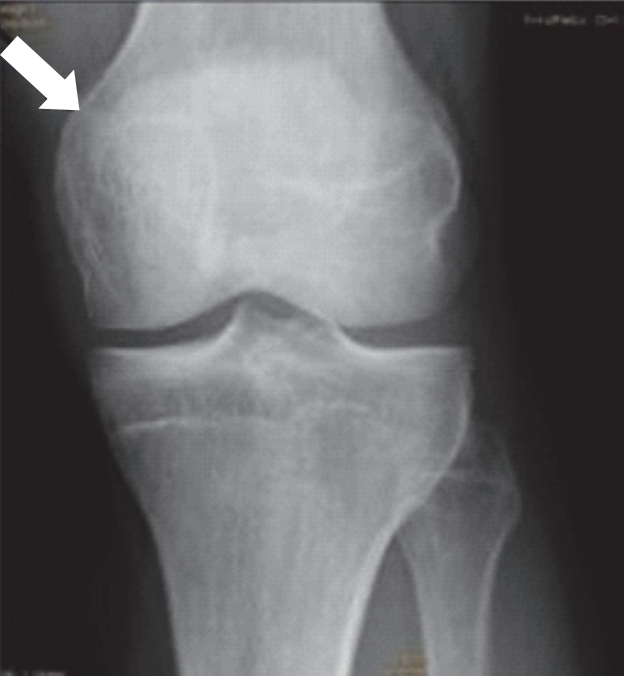
Którą strukturę anatomiczną zaznaczono na radiogramie stawu kolanowego?
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Technik elektroadiolog do badania MR kręgosłupa lędźwiowego powinien ułożyć pacjenta
Po wykonanej radioterapii do dokumentacji pacjenta należy wpisać dawkę promieniowania w jednostce
Objawem późnego odczynu popromiennego po teleradioterapii jest
Gruboziarnista folia wzmacniająca wpływa na zwiększenie na obrazie rentgenowskim nieostrości
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
Zadaniem technika elektroradiologa w pracowni naczyniowej jest
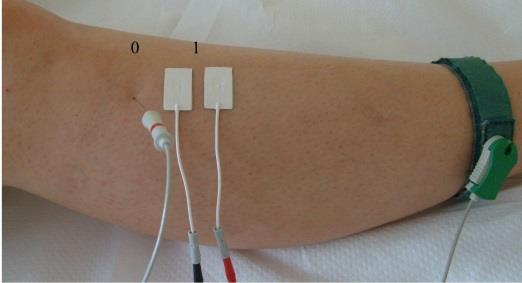
Na ilustracji przedstawiono przygotowanie pacjenta do badania
Wyniosłość międzykłykciowa znajduje się na nasadzie