Pytanie 1
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Wynik: 26/40 punktów (65,0%)
Wymagane minimum: 20 punktów (50%)
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Na zamieszczonej rycinie przedstawiono
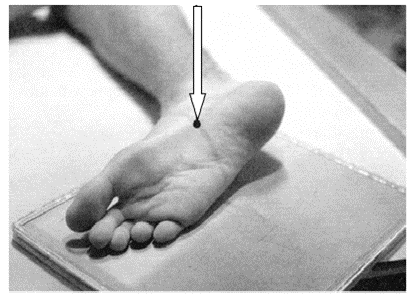
Którą kość zaznaczono strzałką na radiogramie stopy?
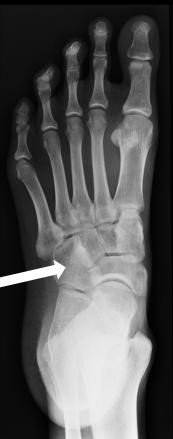
Wskazaniem do wykonania badania spirometrycznego jest
W scyntygrafii dynamiczne badanie najczęściej rozpoczyna się
Które odprowadzenie w badaniu EKG rejestruje różnice potencjałów pomiędzy lewym a prawym przedramieniem?
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Zamieszczony rentgenogram został zarejestrowany podczas wykonania
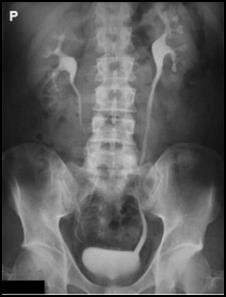
Zwiększenie napięcia na lampie rentgenowskiej powoduje
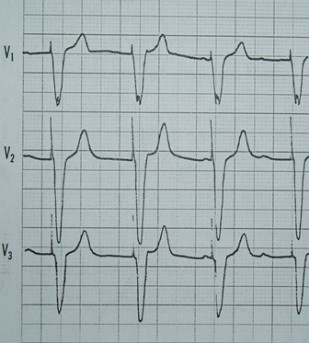
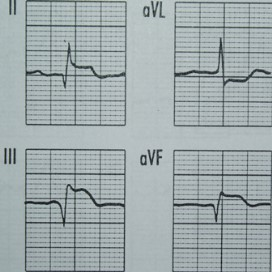
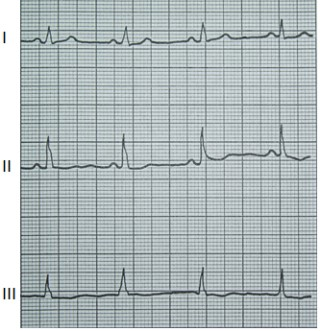
Na którym z zapisów EKG została uwidoczniona fala Pardee'go?
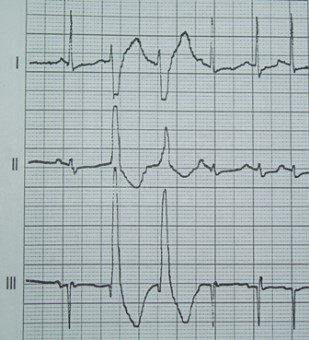
Który obszar napromieniania w radioterapii oznacza się skrótem PTV?
Technik elektroadiolog do badania MR kręgosłupa lędźwiowego powinien ułożyć pacjenta
W scyntygrafii serca metoda bramkowanej akwizycji SPECT umożliwia między innymi ocenę frakcji wyrzutowej
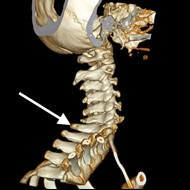
Na obrazie TK kręgosłupa strzałką wskazano wyrostek
Bezwzględnym przeciwwskazaniem do wykonania badania rezonansem magnetycznym jest
Który radioizotop jest stosowany w diagnostyce i terapii raka tarczycy?
Zwiększenie napięcia na lampie rentgenowskiej powoduje
Technika stereotaktyczna polega na napromienianiu nowotworu
W diagnostyce metodą rezonansu magnetycznego biorą udział
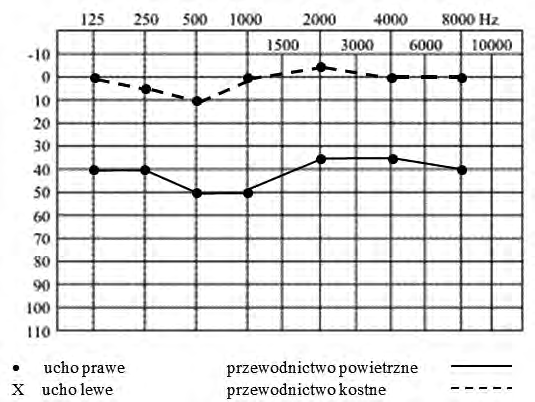
W badaniu audiometrycznym rezerwa ślimakowa to odległość między krzywą
Na zamieszczonej ilustracji przedstawiono ułożenie pacjenta do wykonania zdjęcia rentgenowskiego
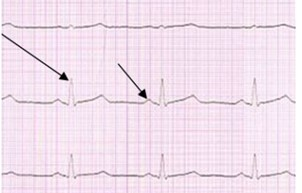
Na elektrokardiogramie strzałki wskazują załamki
Na podstawie zapisu badania audiometrycznego rozpoznano u pacjenta uszkodzenie słuchu
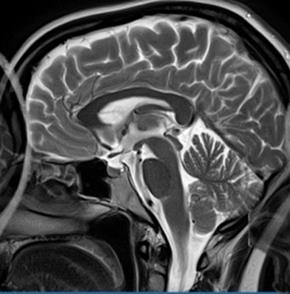
Wskaż przyczynę powstania artefaktu widocznego na obrazie MR.
Zgodnie z obowiązującą procedurą radiologiczną zdjęcie jamy brzusznej przy podejrzeniu zapalenia nerek zostanie wykonane w projekcji
Na rycinie rentgenogramu w projekcji AP symbolem X oznaczono
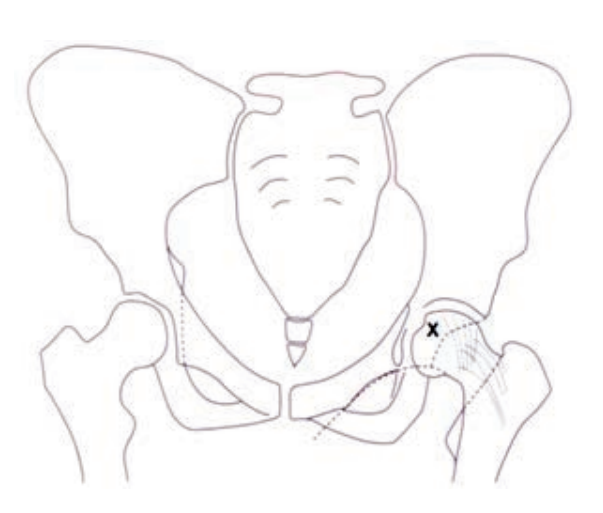
Na schemacie oznaczono
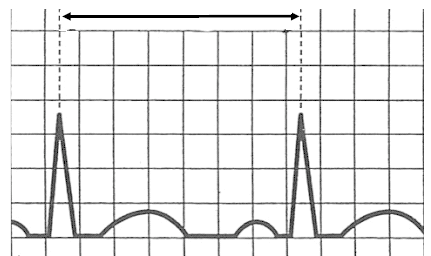
Który detektor w radiografii wymaga laserowego czytnika obrazu?
Na obrazie uwidoczniono
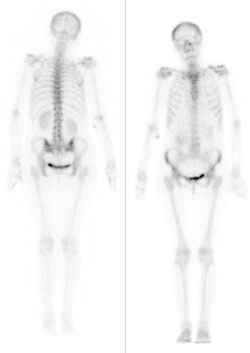
W celu maksymalnego ograniczenia dawki promieniowania badanie rentgenowskie u dzieci należy wykonać
Jaka jest odległość pomiędzy źródłem promieniowania a powierzchnią ciała pacjenta w technice izocentrycznej radioterapii?
W metodzie RM (rezonansu magnetycznego) po umieszczeniu pacjenta w silnym, stałym polu magnetycznym dochodzi do oddziaływania
W badaniu EKG różnice potencjałów pomiędzy lewym podudziem a lewym przedramieniem rejestruje odprowadzenie
Która właściwość promieniowania X pozwala na skierowanie promienia centralnego na wybrany punkt topograficzny podczas wykonywania badania radiologicznego?
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
Pomiar densytometryczny BMD metodą DXA z kręgosłupa powinien obejmować kręgi
Jednym z kryteriów poprawnie wykonanego badania spirometrycznego jest czas trwania natężonego wydechu, który powinien wynosić u osób powyżej 10 roku życia co najmniej
Objawem późnego odczynu popromiennego po teleradioterapii jest
W badaniu EKG punktem przyłożenia odprowadzenia przedsercowego C2 jest
Jak oznacza się w systemie międzynarodowym czwarty górny ząb mleczny po stronie prawej?