Pytanie 1
Oddzielanie płynnej mieszanki poprzez jej odparowanie, a potem skroplenie poszczególnych składników to
Wynik: 25/40 punktów (62,5%)
Wymagane minimum: 20 punktów (50%)
Oddzielanie płynnej mieszanki poprzez jej odparowanie, a potem skroplenie poszczególnych składników to
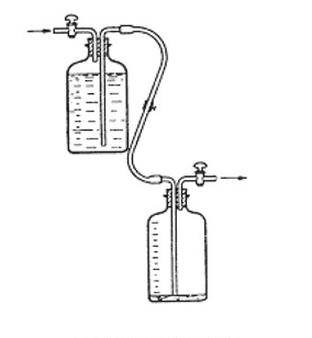
Na rysunku przedstawiono
Osoba pracująca z lotnym rozpuszczalnikiem straciła przytomność. Jakie działania należy podjąć, aby udzielić pierwszej pomocy?
Odczynnik chemiczny, w którym zawartość domieszek wynosi od 1 do 10%, jest nazywany odczynnikiem
Oddzielanie płynnej mieszaniny wieloskładnikowej poprzez odparowanie, a następnie skraplanie jej komponentów, to proces
Procedura oznaczenia kwasowości mleka. Do wykonania analizy, zgodnie z powyższą procedurą, potrzebne są
| Do kolby stożkowej o pojemności 300 cm3 pobrać dokładnie 25 cm3 badanego mleka i rozcieńczyć wodą destylowaną do objętości 50 cm3. Dodać 2-3 krople fenoloftaleiny i miareczkować mianowanym roztworem wodorotlenku sodu do uzyskania lekko różowego zabarwienia. |
Sporządzono 250 cm3 roztworu glicerolu o gęstości 1,05 g/cm3 w temperaturze 20°C. Korzystając z danych zamieszczonych w tabeli, określ stężenie procentowe sporządzonego roztworu glicerolu.
| Glicerolu [%] | 10% | 20% | 30% | 50% |
|---|---|---|---|---|
| d20 [g/dm3] | 1023,70 | 1048,40 | 1073,95 | 1127,20 |
W jakiej standardowej temperaturze są kalibrowane szklane naczynia pomiarowe?
W jakim celu używa się kamyczków wrzenne w trakcie długotrwałego podgrzewania cieczy?
W celu uzyskania 500 g mieszaniny oziębiającej o temperaturze -18oC należy zmieszać
| Tabela. Mieszaniny oziębiające | ||
|---|---|---|
| Temperatura mieszaniny [°C] | Skład mieszaniny | Stosunek masowy |
| -2 | Woda + chlorek amonu | 10 : 3 |
| -15 | Woda + rodanek amonu | 10 : 13 |
| -18 | Lód + chlorek amonu | 10 : 3 |
| -21 | Lód + chlorek sodu | 3 : 1 |
| -22 | Lód + chlorek amonu + azotan(V) amonu | 25 : 5 : 11 |
| -25 | Lód + azotan(V) amonu | 1 : 1 |
Instalacja, do której należy podłączyć palnik, powinna być pokryta farbą w kolorze
Metoda oczyszczania substancji, która opiera się na różnicy w rozpuszczalności substancji docelowej oraz zanieczyszczeń w zastosowanym rozpuszczalniku, nosi nazwę
Zapis "20°C" umieszczony na pipecie oznacza, że

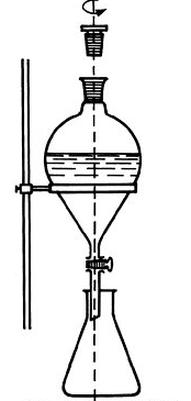
Na ilustracji zobrazowano urządzenie do
Kalibracja pH-metru nie jest potrzebna po
Na rysunku przedstawiono proces
Do grupy reagentów o szczególnym zastosowaniu nie wlicza się
Różnica pomiędzy średnim wynikiem pomiaru a wartością rzeczywistą stanowi błąd
Metodą, która nie umożliwia przeniesienia składników próbki do roztworu, jest
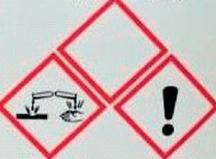
Według zasady pierwszeństwa, znajdując na opakowaniu zbiorczym odczynnika piktogramy pokazane na rysunku, należy zwrócić szczególną uwagę na to, że substancja jest
Substancje, które wykorzystuje się do ustalania miana roztworu, to
Naczynia z roztworem kwasu siarkowego(VI) o dużym stężeniu nie powinny być pozostawiane otwarte nie tylko za względów bezpieczeństwa, ale także dlatego, że kwas
W którym wierszu tabeli podano ilości substancji i wody, potrzebne do sporządzenia 350 g roztworu o stężeniu 7%?
| Masa substancji | Masa wody | |
|---|---|---|
| A. | 24,5 g | 350 g |
| B. | 24,5 g | 325,5 g |
| C. | 7 g | 343 g |
| D. | 7 g | 350 g |
Jakie jest pH 0,001-molowego roztworu NaOH?
Wskaż zbiór substancji, które po rozpuszczeniu w wodzie stają się elektrolitami?
Aspirator jest urządzeniem wykorzystywanym do pobierania próbek
Symbol "In" znajduje się na
Aby wykonać chromatografię cienkowarstwową, należy przygotować eluent składający się z toluenu, acetonu oraz kwasu mrówkowego w proporcjach objętościowych 10:4:1. Jakie ilości poszczególnych składników powinny być wykorzystane do uzyskania 300 cm3 eluentu?
Zgodnie z danymi zawartymi w tabeli wskaźników roztwór obojętny będzie miał barwę
| Wskaźnik | Zakres zmiany barwy (w jednostkach pH) | Barwa w środowisku | |
|---|---|---|---|
| kwaśnym | zasadowym | ||
| błękit tymolowy | 1,2 – 2,8 | czerwona | żółta |
| oranż metylowy | 3,1 – 4,4 | czerwona | żółta |
| czerwień metylowa | 4,8 – 6,0 | czerwona | żółta |
| czerwień chlorofenolowa | 5,2 – 6,8 | żółta | czerwona |
| błękit bromotymolowy | 6,0 – 7,6 | żółta | niebieska |
| czerwień fenolowa | 6,6 – 8,0 | żółta | czerwona |
| błękit tymolowy | 8,0 – 9,6 | żółta | niebieska |
| fenoloftaleina | 8,2 – 10,0 | bezbarwna | czerwona |
| żółcień alizarynowa | 10,1 – 12,0 | żółta | zielona |
Po rozpuszczeniu substancji w kolbie miarowej, należy odczekać przed dopełnieniem jej wodą "do kreski" miarowej. Taki sposób postępowania jest uzasadniony
Do wykrywania pierwiastków w niskich stężeniach w badaniach spektrograficznych należy używać reagentów
W trakcie określania miana roztworu NaOH, do zmiareczkowania 25,0 cm3 tego roztworu, użyto 30,0 cm3 roztworu HCl o stężeniu 0,1000 mol/dm3. Jakie miało miano zasady?
Proces, w którym woda jest usuwana z zamrożonego materiału poprzez sublimację lodu
(czyli bezpośrednie przejście do stanu pary z pominięciem stanu ciekłego) nazywa się
W chemicznym laboratorium apteczka pierwszej pomocy powinna zawierać
Ilustracja przedstawia fragment szklanej pipety wielomiarowej

Co oznacza zapis cz.d.a. na etykiecie opakowania odczynnika chemicznego?
W celu wydania świadectwa kontroli jakości odczynnika chemicznego - jodku potasu cz.d.a. przeprowadzono jego analizę. Wymagania oraz wyniki badań zapisano w tabeli:
Z analizy danych zawartych w tabeli wynika, że jodek potasu cz.d.a.
| Wymagania | Wynik badania | |
|---|---|---|
| Zawartość KI | min. 99,5% | 99,65% |
| Wilgoć | max. 0,1% | 0,075% |
| Substancje nierozpuszczalne w wodzie | max. 0,005% | 0,002% |
| pH (5%, H2O) | 6 ÷ 8 | 6,8 |
| Azot ogólny (N) | max. 0,001% | 0,0007% |
| Chlorki i bromki (j. Cl) | max. 0,01% | 0,004% |
| Fosforany (PO4) | max. 0,001% | 0,0006% |
| Jodany (IO3) | max. 0,0003% | 0,0001% |
| Siarczany (SO4) | max. 0,001% | 0,0004% |
| Metale ciężkie (j. Pb) | max. 0,0005% | 0,00025% |
| Arsen (As) | max. 0,00001% | 0,000006% |
| Magnez (Mg) | max. 0,001% | 0,0004% |
| Sód (Na) | max. 0,05% | 0,015% |
| Wapń (Ca) | max. 0,001% | 0,0006% |
| Żelazo (Fe) | max. 0,0003% | 0,0003% |
W przypadku zanieczyszczeń szklanych naczyń osadami o charakterze nieorganicznym, takimi jak wodorotlenki, tlenki oraz węglany, do ich oczyszczania używa się
Które z poniższych działań należy wykonać przed rozpoczęciem pracy z nowym szkłem laboratoryjnym?
W przypadku rozlania żrącego odczynnika chemicznego na skórę pierwszym poprawnym działaniem jest: