Pytanie 1
W którym okresie ciąży wykonanie u kobiety zdjęcia rentgenowskiego klatki piersiowej jest najbardziej szkodliwe dla płodu?
Wynik: 20/40 punktów (50,0%)
Wymagane minimum: 20 punktów (50%)
W którym okresie ciąży wykonanie u kobiety zdjęcia rentgenowskiego klatki piersiowej jest najbardziej szkodliwe dla płodu?
Do czego służy do symulator rentgenowski wykorzystywany w procesie radioterapii?
Fistulografia to badanie kontrastowe
Który radioizotop jest stosowany w diagnostyce i terapii raka tarczycy?
Świeżo wynaczyniona krew na obrazach TK głowy bez podania środka kontrastowego ukazuje się jako obszar
Która struktura może być oknem akustycznym w badaniu ultrasonograficznym?
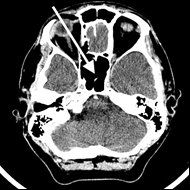
Na radiogramie TK głowy strzałką wskazano
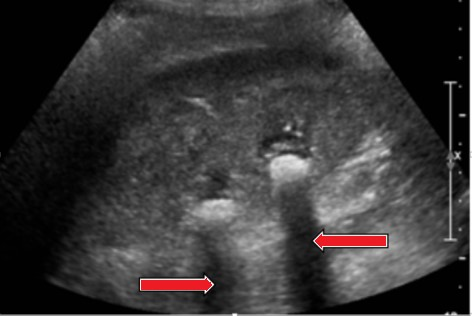
Który artefakt wskazano strzałkami na obrazie USG nerki?
Efekt „tea cup” widoczny jest na mammografach wykonanych w projekcji
Zwiększenie napięcia na lampie rentgenowskiej powoduje
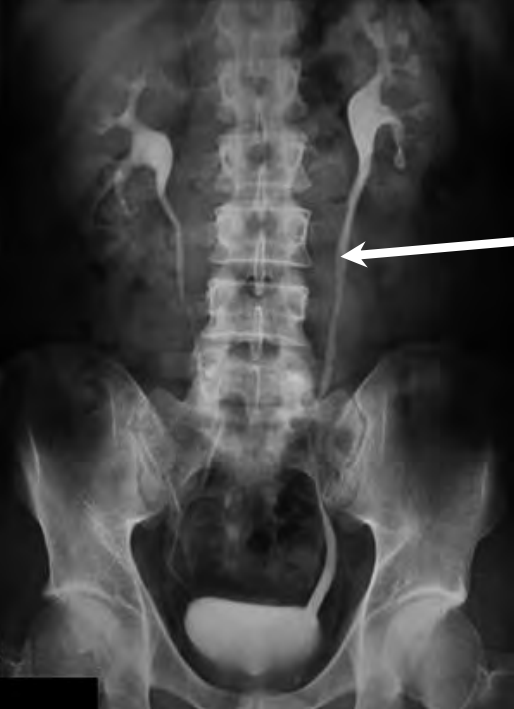
Na prawidłowo przedstawionym radiogramie badania kontrastowego strzałką zaznaczono
Testy podstawowe z zakresu geometrii pola rentgenowskiego, przeznaczone do sprawdzenia zgodności pola wiązki promieniowania rentgenowskiego z symulacją świetlną, są wykonywane raz
Którą kasetę należy wykorzystać do wykonania rentgenogramu klatki piersiowej w projekcji bocznej u 35-letniej pacjentki o wzroście 165 cm i wadze 54 kg?
Miejscem wykonania pomiaru densytometrycznego z kości przedramienia jest
Brachyterapia polegająca na wielokrotnym wsuwaniu i wysuwaniu źródła promieniowania do tego samego aplikatora nosi nazwę
Obiektywną metodą badania słuchu jest audiometria
Ultrasonograficzne środki kontrastowe to
W technice napromieniania SSD mierzona jest odległość źródła promieniowania
W zapisie EKG linia izoelektryczna obrazuje
Na zamieszczonym radiogramie strzałką oznaczono kość
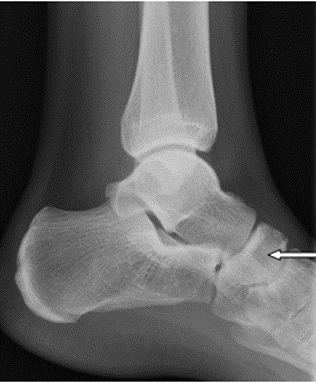
Podczas wykonywania zdjęcia rentgenowskiego lewobocznego czaszki promień centralny powinien przebiegać
W celu wykonania badania scyntygraficznego układu kostnego radiofarmaceutyk należy podać pacjentowi
Wynik badania słuchu metodą audiometrii tonalnej wskazuje na
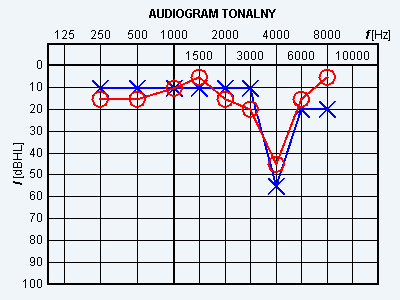
Ligand stosuje się
Które czynności wykonuje technik elektroradiolog w pracowni „gorącej”?
Podczas teleradioterapii piersi lewej narządem krytycznym jest
Na rentgenogramie przedstawione jest złamanie Saltera-Harrisa typu
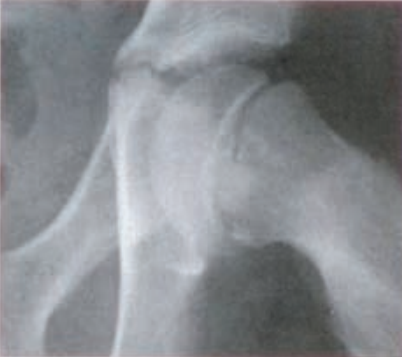
Wskazaniem do zastosowania brachyterapii w leczeniu radykalnym jest rak
Zdjęcie którego zęba górnego zlecił na skierowaniu lekarz stomatolog?
W radioterapii hadronowej leczenie odbywa się przy użyciu
Hałas podczas badania tomografii rezonansu magnetycznego jest efektem ubocznym pracy
Zamieszczony rentgenogram został zarejestrowany podczas wykonania
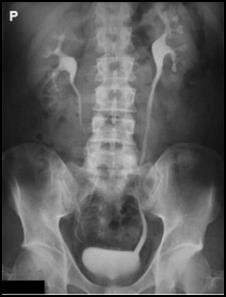
W jaki sposób należy ustawić promień centralny w stosunku do ramienia i przedramienia, by wykonać zdjęcie rentgenograficzne stawu łokciowego u pacjenta z przykurczem?
W jaki sposób należy ustawić promień centralny w stosunku do ramienia i przedramienia, by wykonać zdjęcie rentgenograficzne stawu łokciowego u pacjenta z przykurczem?
W scyntygrafii wykorzystywane są głównie radioizotopy emitujące promieniowanie
Zgodnie ze standardami do wykonania zdjęcia bocznego czaszki, należy zastosować kasetę o wymiarze
Technik elektroadiolog do badania MR kręgosłupa lędźwiowego powinien ułożyć pacjenta
Który wynik badania tympanometrycznego potwierdza, że słuch badanego pacjenta jest w granicach normy?
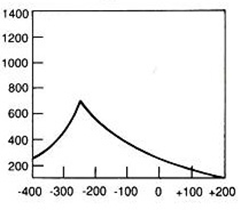
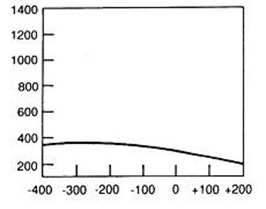
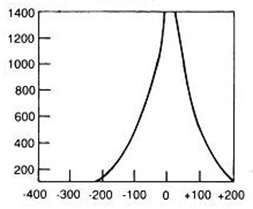
Brachyterapia polega na napromieniowaniu pacjenta promieniowaniem
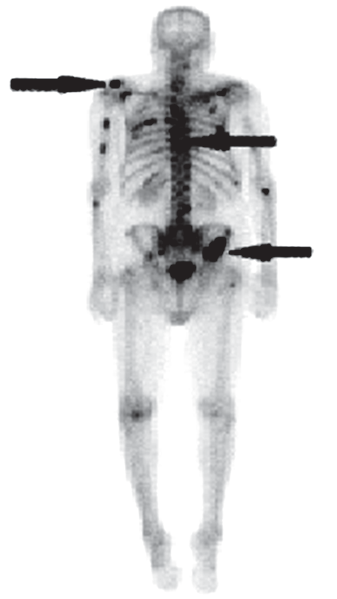
Na scyntygramie kości strzałkami oznaczono ogniska