Pytanie 1
Dostanie się do środowiska pałeczek Salmonella, hodowanych na podłożach mikrobiologicznych, skutkuje
Wynik: 29/40 punktów (72,5%)
Wymagane minimum: 20 punktów (50%)
Dostanie się do środowiska pałeczek Salmonella, hodowanych na podłożach mikrobiologicznych, skutkuje
W wyniku badań mikrobiologicznych wody przeznaczonej do produkcji soków, po 3 dniach inkubacji stwierdzono w 1 ml próbki 100 j.t.k. bakterii, w tym 2 j.t.k Escherichia coli.
Ustal jakość wody na podstawie informacji zamieszczonych w tabeli.
| Wymagania mikrobiologiczne, jakim powinna odpowiadać woda | ||
|---|---|---|
| Lp. | Parametr | Najwyższa dopuszczalna wartość liczby jednostek tworzących kolonię [j.t.k] |
| 1 | Escherichia coli | 0 |
| 2 | Enterokoki | 0 |
| 3 | Pseudomonas aeruginosa | 0 |
| 4 | Ogólna liczba mikroorganizmów w (36±2) °C po 48h | 20 |
| 5 | Ogólna liczba mikroorganizmów w (22±2) °C po 72h | 100 |
Który z reagentów można wykorzystać do wykrywania skrobi?
W opisie przeprowadzonego eksperymentu
(...) obecność węgla wykrywa się poprzez spalenie próbki i określenie ilości CO2 przy użyciu roztworu wody barytowej. Azot w trakcie spalania próbki z sodem metalicznym generuje cyjanek, który może być wykryty po dodaniu FeSO4 jako błękit pruski (...) Jakiego rodzaju analizę zastosowano w opisywanym doświadczeniu?
Analiza obecności pałeczek Salmonella w żywności zalicza się do badań
Do analizy pobrano próbkę o masie 200 mg. Na podstawie informacji zamieszczonych w tabeli określ, w której skali będzie wykonana ta analiza.
| Wielkość próbki | Skala analizy |
|---|---|
| > 0,1 g | makro |
| 0,01 – 0,1 g | semimikro |
| 0,0001 – 0,01 g | mikro |
| < 10-4 g | ultramikro |
Skróconym badaniom poddano próbki wody z 4 ujęć. Wyniki zapisano w tabeli. Na podstawie analizy danych zawartych w tabelach wskaż zestaw próbek spełniających wymagania jakościowe.
| Wyniki badań próbek wody z 4 ujęć | ||||
|---|---|---|---|---|
| Wskaźnik organoleptyczny | Próbka 1 | Próbka 2 | Próbka 3 | Próbka 4 |
| Barwa (Pt) | 10 | 20 | 15 | 20 |
| Odczyn (pH) | 7,5 | 6,5 | 6,8 | 8,8 |
| Mętność | 5 | 4 | 3 | 5 |
| Zapach | 3 – naturalny, nieuciążliwy | 3 – naturalny, nieuciążliwy | 3 – nieuciążliwy, wyczuwalny zapach chloru | 3 – naturalny, nieuciążliwy |
| Zawiesiny, plamy oleju, itp. | Niewidoczne w szklanych naczyniach | Niewidoczne w szklanych naczyniach | Niewidoczne w szklanych naczyniach | Niewidoczne w szklanych naczyniach |
| Warunki organoleptyczne, jakim powinna odpowiadać woda do picia i na potrzeby gospodarcze | ||||
| Lp. | Wskaźniki organoleptyczne, Nazwa substancji | Jednostka miary | Najwyższa dopuszczalna dawka lub przedział | |
| 1 | Barwa (Pt) | mg · dm-3 | 20 | |
| 2 | Odczyn (pH) | ---- | 6,5 – 8,5 | |
| 3 | Mętność | mg · dm-3 | 5 | |
| 4 | Zapach | ---- | 3 – naturalny, nieuciążliwy, dopuszczalny zapach chloru przy dezynfekcji chlorem | |
| 5 | Zawiesiny, plamy oleju itp. | ---- | Niewidoczne w szklanych naczyniach | |
W trakcie ilościowego oznaczania chlorków w próbce wody, zachodzą przemiany zgodnie z równaniami reakcji. Który typ reakcji reprezentują?
| Ag⁺ + Cl⁻ → AgCl 2 Ag⁺ + CrO₄²⁻ → Ag₂CrO₄ |
Przeprowadzano analizę jakościową próbki według schematu:
Badana próbka zawierała kation
| badany roztwór zawierający jony X2+ | |
| + roztwór HCl | |
| XCl2↓ biały osad | |
| + H2O: ogrzać | |
| roztwór X2+: podzielić na 2 części | |
| + roztwór KI | oziębić |
| XI2 żółty osad | XCl2↓ biały osad |
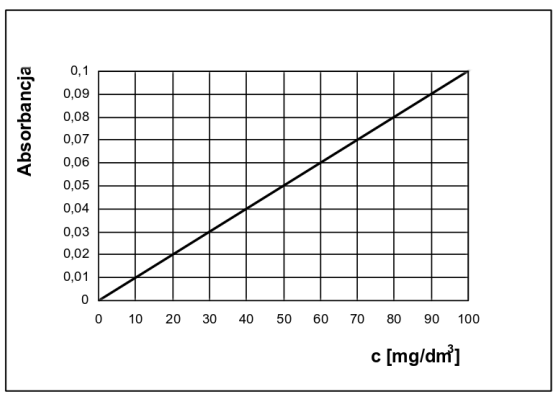
Korzystając z zamieszczonej na rysunku krzywej wzorcowej spektrofotometrycznego oznaczania kwasu salicylowego określ, ile miligramów tego kwasu znajduje się w 1 dm3 roztworu, jeżeli absorbancja badanej próbki wynosi 0,06.
W procesie oddzielania osadu od cieczy podczas realizacji analiz jakościowych metodą półmikro, używa się
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Jakie aspekty nie są objęte badaniami organoleptycznymi olejów rafinowanych?
Zespół enzymów, obecny zarówno w organizmach roślinnych, jak i zwierzęcych, który katalizuje proces hydrolizy wiązań peptydowych w białkach oraz peptydach, to
Na zmiareczkowanie 10 cm3 roztworu KOH zużyto 10 cm3 0,1000-molowego roztworu H2SO4. Oblicz ilość KOH w badanej próbce w g/100 cm3.
| MK = 39 g/mol, MO = 16 g/mol, MH = 1 g/mol, MS = 32 g/mol |
Jaką temperaturę powinny mieć próbki wody lub ścieków w czasie transportu?
Jakie urządzenie wykorzystuje się do pomiaru lepkości względnej?
Wykonano jodometryczne oznaczenie zawartości kwasu askorbinowego dla 4 próbek tabletek witaminy C, uzyskując wyniki. Na podstawie informacji zawartych w opisie i wyników analizy można stwierdzić, że zawartość witaminy C
| Opis Na opakowaniach tabletek witaminy C producenci deklarują zawartość 200 mg kwasu askorbinowego. Zgodnie z normą odchylenia od deklarowanej zawartości substancji leczniczej nie mogą przekraczać ±10% dla tabletek o zawartości poniżej 100 mg i ±5% dla tabletek o deklarowanej zawartości 100 mg i więcej. | ||||
| Próbka | 1 | 2 | 3 | 4 |
| Zawartość kwasu askorbinowego | 198,5 mg | 211 mg | 201 mg | 205 mg |
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
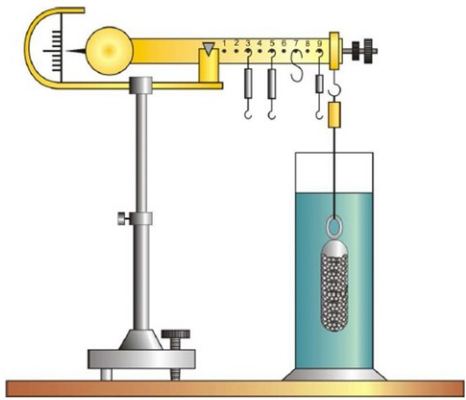
Przedstawiona na rysunku waga Westphala-Mohra służy do badania
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
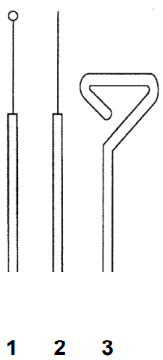
Wskaż nazwy sprzętów laboratoryjnych przedstawionych na rysunku.
W treści metody analitycznej napisano:
Różnica w wynikach dwóch pomiarów przeprowadzonych jednocześnie lub w krótkim odstępie czasowym na tej samej próbce, przez tego samego analityka, w identycznych warunkach, nie powinna być większa niż 1,5 g na 100 g analizowanej próbki.
Jaki parametr metody analitycznej został opisany?
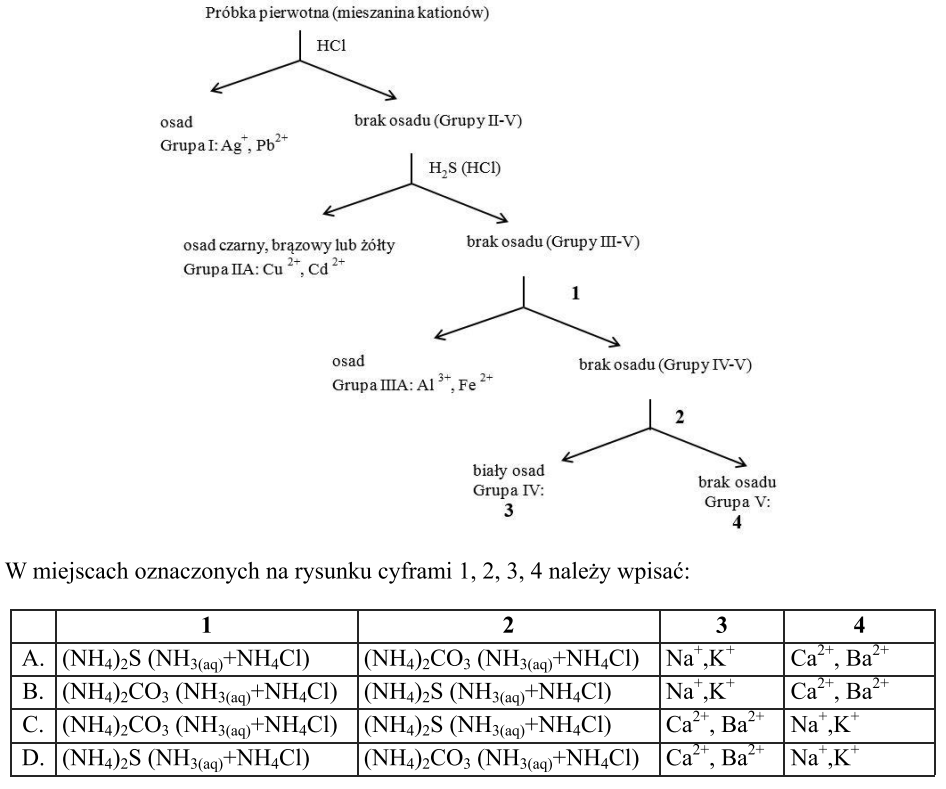
Schemat obrazuje proces rozdzielenia mieszaniny kationów.
Próbka pierwotna (mieszanina kationów)
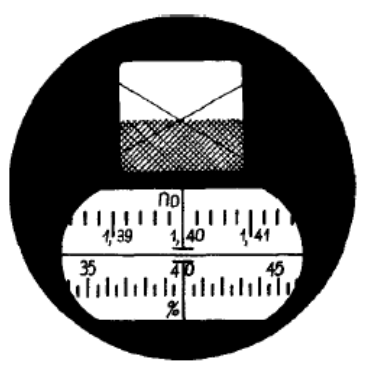
Na rysunku przedstawione jest pole widzenia
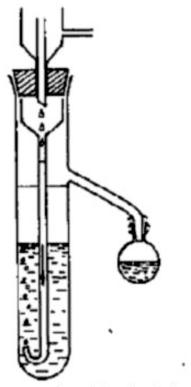
Ekstraktor przedstawiony na rysunku stosuje się do rozpuszczalników
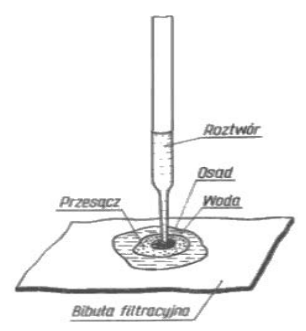
Na rysunku przedstawiono wykonanie analizy metodą
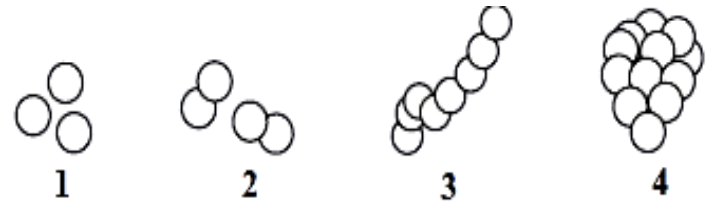
Na rysunku przedstawiającym formy kolonii bakterii cyfrą 4 oznaczono
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Szkło wodne sodowe jest roztworem krzemianów sodu o wzorze Na2O • nSiO2 Zawartość tlenków sodu i krzemu wpływa na tzw. moduł molowy M
| M = B/A·1,032 | A - zawartość tlenku sodu, [%] B - zawartość krzemionki, [%] 1,032 - współczynnik przeliczeniowy z jednostek wagowych na mole |
| Wymagania | Rodzaj R | |||
|---|---|---|---|---|
| R - 150-1.7 | R - 150S | R - 150-2.3 | R - 149 | |
| Moduł molowy SiO2/Na2O | 1,65 ÷ 1,85 | 2,2 ÷ 2,4 | 2,3 ÷ 2,4 | 2,8 ÷ 3,0 |
W analizie najczęściej oznacza się parametry CHZT i BZT
Aby wykonać roztwór mosiądzu (stop miedzi), jaki kwas należy zastosować?
Wartości iloczynów rozpuszczalności związków srebra wynoszą odpowiednio: Osad której soli srebra wytrąci się jako pierwszy podczas dodawania jonów Ag+ do roztworu zawierającego jony I-, Br-, Cl- oraz CN-?
| Związek chemiczny | Iloczyn rozpuszczalności |
|---|---|
| AgCl | 1,8·10-10 |
| AgBr | 5,3·10-13 |
| AgCN | 1,4·10-16 |
| AgI | 8,3·10-17 |
Analiza, która opiera się na kontrolowanym wprowadzaniu roztworu o znanym stężeniu do badanego roztworu, to metoda oznaczeń ilościowych zwana
Aby określić całkowitą zawartość żelaza w próbce wody, konieczne jest zredukowanie żelaza(III) do żelaza(II), a następnie wykorzystanie metody analitycznej, która nazywa się
Jak nazywa się część białkowa enzymu?
Reakcja: MnO4- + 8H+ + 5e- → Mn2+ + 4H2O jest wykorzystywana w metodzie analizy jakościowej, określanej jako
Analiza wody basenowej w celu wykrycia bakterii polega na podgrzewaniu próbki w inkubatorze przez 48 godzin w temperaturze 36±2°C. Jaki proces jest opisany?
Jakiego koloru płomień uzyskuje się dzięki sole miedzi?
Badanie szczegółowej struktury komórek roślinnych oraz zwierzęcych, jak również rozmieszczenia atomów w kryształach metali i minerałów, jest możliwe dzięki wykorzystaniu mikroskopu