Pytanie 1
Który narząd na obrazie scyntygrafii znakowanej erytrocytami zaznaczono cyfrą 2?
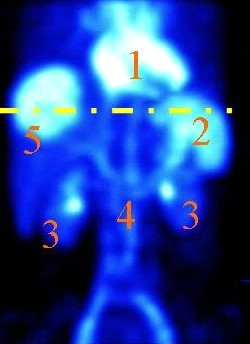
Wynik: 36/40 punktów (90,0%)
Wymagane minimum: 20 punktów (50%)
Który narząd na obrazie scyntygrafii znakowanej erytrocytami zaznaczono cyfrą 2?

Zgodnie z obowiązującymi przepisami powierzchnia gabinetu rentgenowskiego, w którym jest zainstalowany zestaw rentgenowski do badań naczyniowych, powinna wynosić
W przedstawionym na ilustracji obrazie badania angiograficznego uwidoczniono
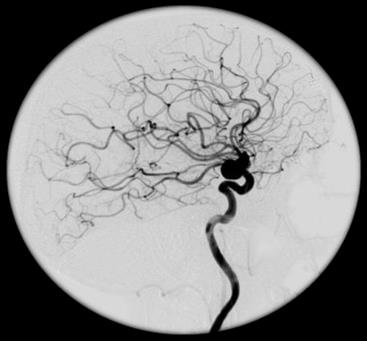
Zwiększenie napięcia na lampie rentgenowskiej powoduje
Zamieszczone obrazy związane są z badaniem
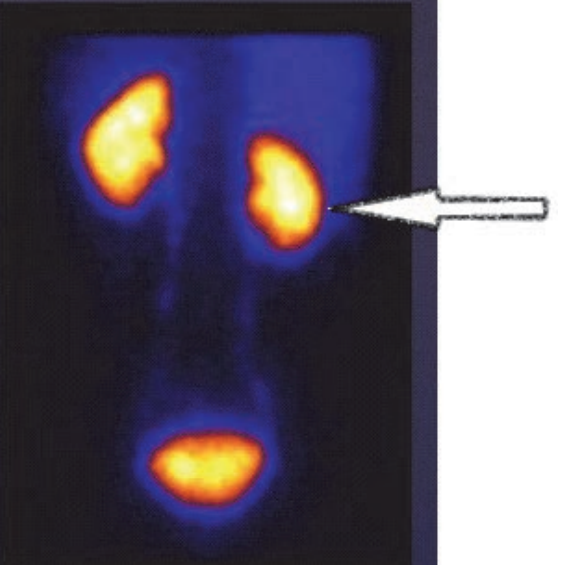
Na scyntygramie strzałką oznaczono
Testy podstawowe z zakresu geometrii pola rentgenowskiego, przeznaczone do sprawdzenia zgodności pola wiązki promieniowania rentgenowskiego z symulacją świetlną, są wykonywane raz
Który system informatyczny służy do archiwizacji i transmisji obrazów radiologicznych?
Na zamieszczonym obrazie radiologicznym nadgarstka strzałką wskazano kość
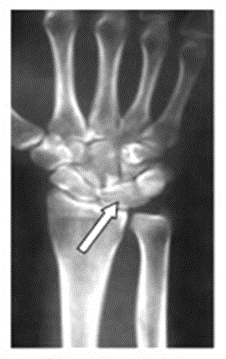
Na radiogramie strzałką oznaczono
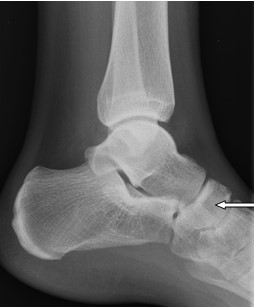
Która właściwość promieniowania X pozwala na skierowanie promienia centralnego na wybrany punkt topograficzny podczas wykonywania badania radiologicznego?
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
Fistulografia to badanie kontrastowe
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
Promieniowanie rentgenowskie jest
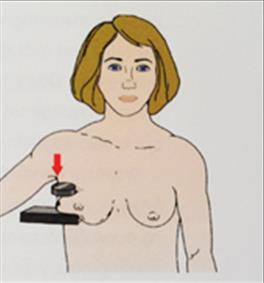
Ilustracja przedstawia pozycjonowanie pacjentki do badania mammograficznego w projekcji
Cholangiografia to badanie radiologiczne
Do zdjęcia lewobocznego kręgosłupa lędźwiowo-krzyżowego pacjenta należy ułożyć na boku
Wskaż osłonę radiologiczną, która jest stosowana w pracowniach radiodiagnostyki stomatologicznej.




Promieniowanie jonizujące pośrednio to
Podstawowym elementem diagnostycznym aparatury izotopowej wykorzystującej emisyjne metody pomiaru jest
Podczas wykonywania zdjęcia rentgenowskiego klatki piersiowej w celu ochrony radiologicznej pacjenta należy zastosować
Które badanie zostało zarejestrowane na przedstawionym radiogramie?
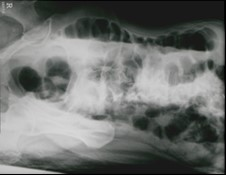
Zadaniem technika elektroradiologii w pracowni badań naczyniowych jest
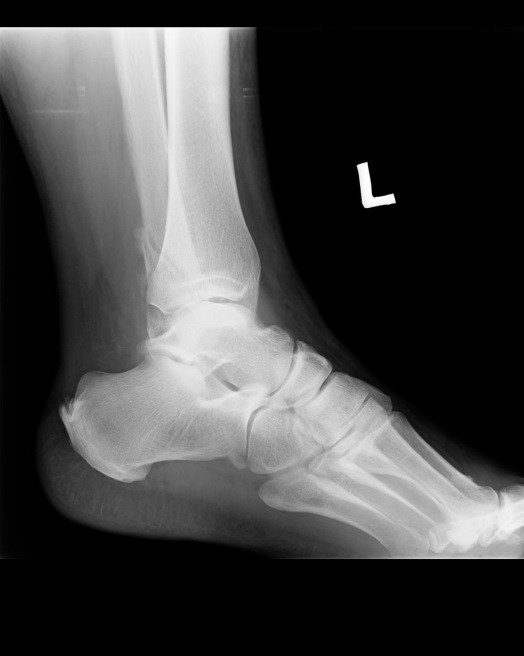
Na radiogramie uwidoczniono złamanie
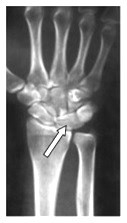
Na obrazie radiologicznym nadgarstka strzałką zaznaczona jest kość
Która sekwencja w obrazowaniu MR jest stosowana do uwidocznienia naczyń krwionośnych?
W diagnostyce metodą rezonansu magnetycznego biorą udział
Zgodnie ze standardami do wykonania zdjęcia bocznego czaszki, należy zastosować kasetę o wymiarze
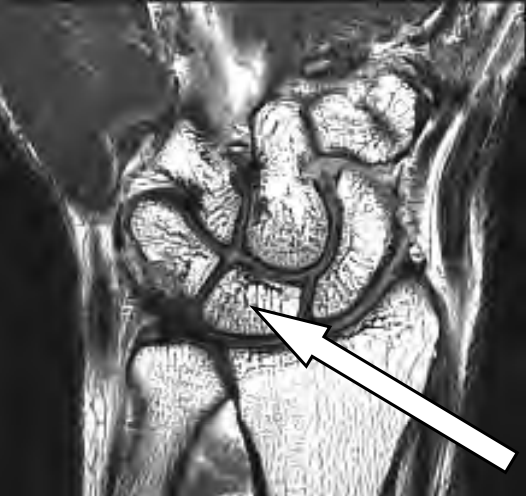
Na obrazie RM nadgarstka lewego strzałką oznaczono kość
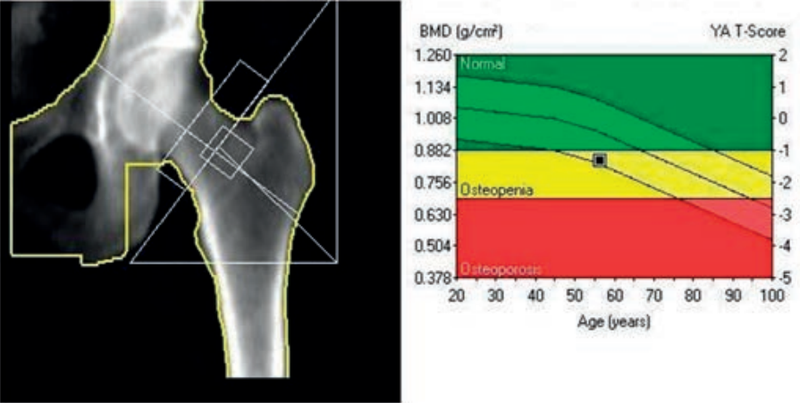
Wskazaniem do wykonania przesiewowego badania densytometrycznego jest
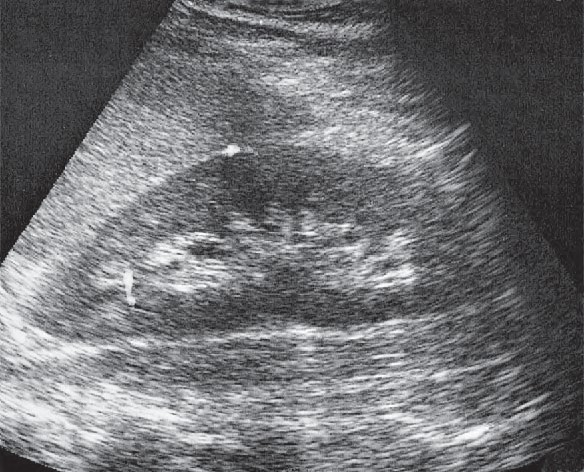
Który narząd widoczny jest na wydruku badania ultrasonograficznego?
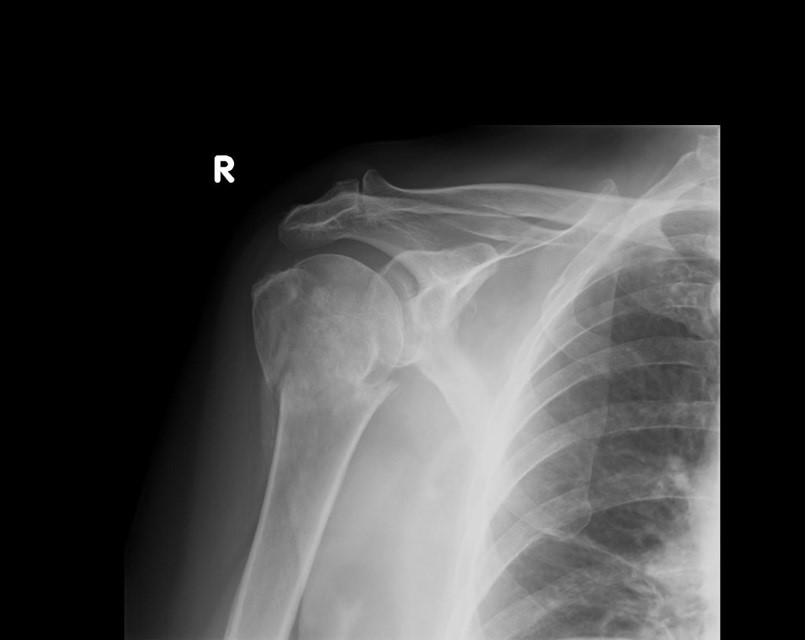
Na obrazie radiologicznym uwidoczniono złamanie kości
Jak określa się rekonstrukcję obrazów TK, której wynikiem są obrazy dwuwymiarowe tworzone w dowolnej płaszczyźnie przez wtórną obróbkę zestawionych ze sobą wielu przekrojów poprzecznych?
Parametrem krwi, który powinien zostać oznaczony u pacjenta przed wykonaniem badania MR z kontrastem jest
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Kto jest odpowiedzialny za wykonywanie testów podstawowych kontroli jakości gammakamery w Zakładzie Medycyny Nuklearnej?
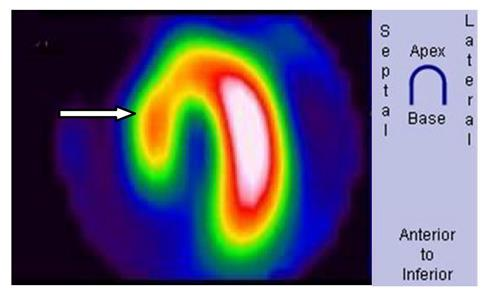
Na obrazie scyntygrafii perfuzyjnej serca strzałką wskazano ścianę
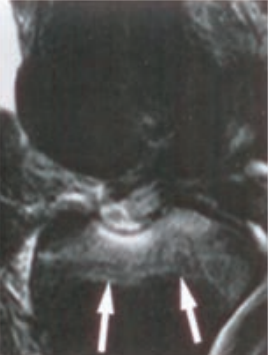
Obraz stawu kolanowego otrzymano metodą
Scyntygrafia kości „whole body” jest wskazana podczas diagnostyki