Pytanie 1
Nieostrość geometryczna obrazu rentgenowskiego zależy od
Wynik: 32/40 punktów (80,0%)
Wymagane minimum: 20 punktów (50%)
Nieostrość geometryczna obrazu rentgenowskiego zależy od
Na ilustracji przedstawiono zjawisko
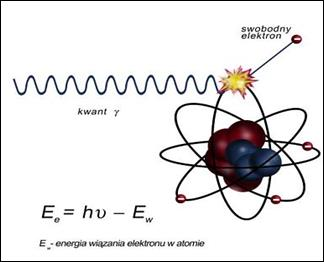
Celiakografia jest badaniem kontrastowym
W jaki sposób należy oprzeć stroik w audiometrycznym badaniu przewodnictwa kostnego?
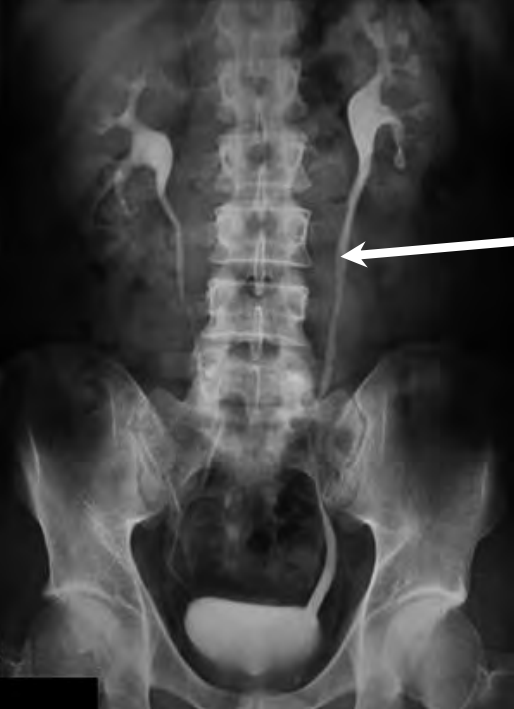
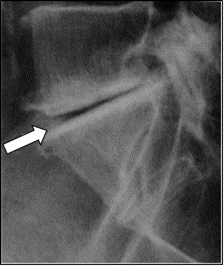
Na prawidłowo przedstawionym radiogramie badania kontrastowego strzałką zaznaczono
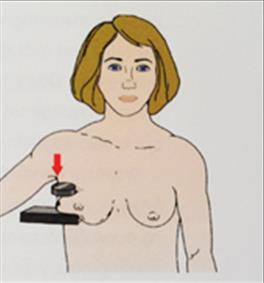
Ilustracja przedstawia pozycjonowanie pacjentki do badania mammograficznego w projekcji
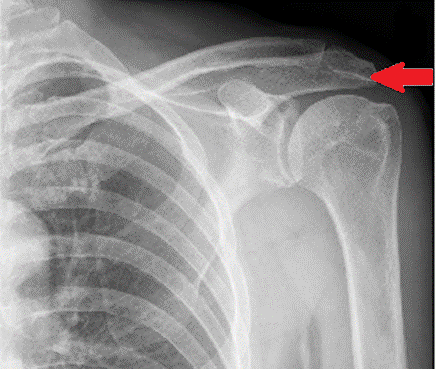
Na radiogramie stawu barkowego strzałką wskazano
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem
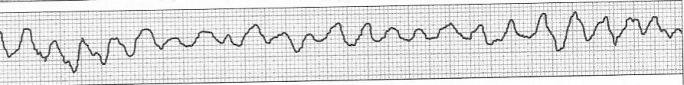
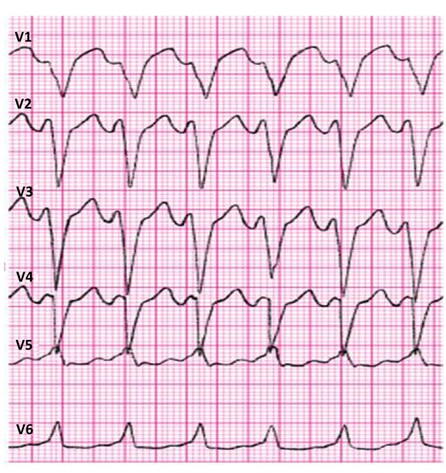
Zamieszczony elektrokardiogram przedstawia
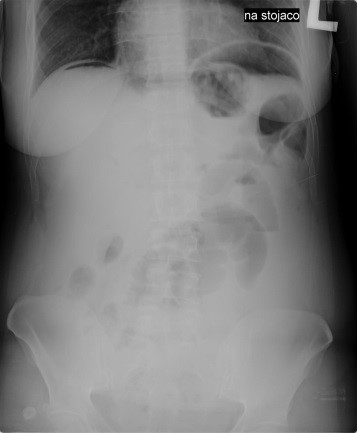
Radiogram jamy brzusznej uwidacznia
Z kratką przeciwrozproszeniową należy wykonać zdjęcie
Który obszar napromieniania w radioterapii oznacza się skrótem PTV?
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
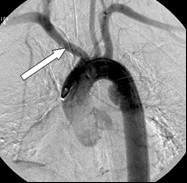
Na obrazie cyfrowej angiografii subtrakcyjnej strzałką zaznaczono
Jaka jest standardowa odległość OF do wykonania rentgenowskich zdjęć kości i stawów kończyny górnej?
Który załamek w zapisie EKG odpowiada zjawisku depolaryzacji przedsionków mięśnia sercowego?
Na zamieszczonym rentgenogramie strzałką zaznaczono
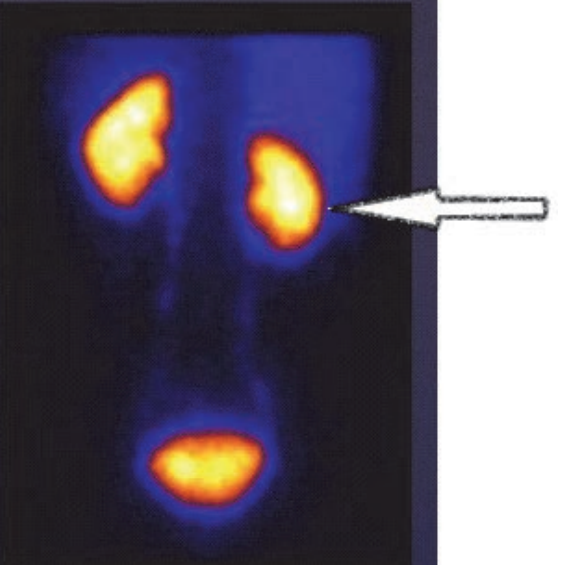
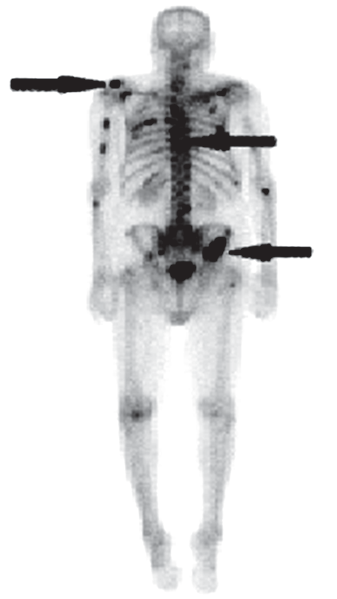
Na scyntygramie strzałką oznaczono
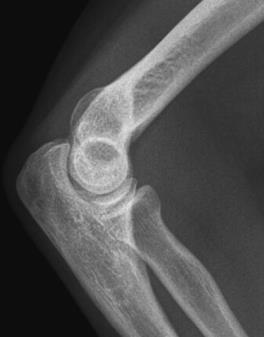
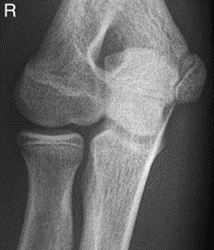
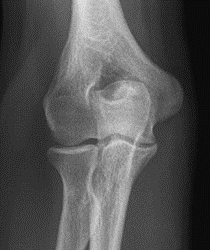
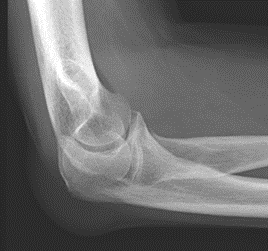
Które zdjęcie RTG stawu łokciowego zostało wykonane w projekcji skośnej w rotacji zewnętrznej?
W radiologii stomatologicznej ząb o numerze 23 to kieł
Folia wzmacniająca umieszczona w kasecie rentgenowskiej emituje pod wpływem promieniowania X światło
Na scyntygramie kości strzałkami oznaczono ogniska
Znak umieszczony w pracowni rezonansu magnetycznego zakazuje wstępu osobom

W celu maksymalnego ograniczenia dawki promieniowania badanie rentgenowskie u dzieci należy wykonać
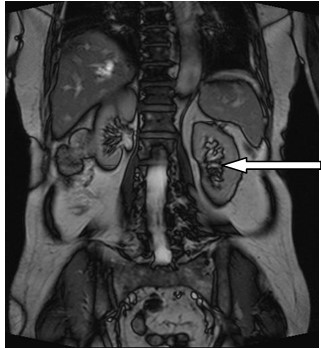
Który narząd został oznaczony strzałką na obrazie rezonansu magnetycznego?
Badanie gęstości mineralnej kości metodą DXA należy wykonać
Pojawienie się w zapisie EKG patologicznego załamka Q lub QS może wskazywać na
W badaniu PET stosuje się tylko radioizotopy emitujące
Efekt „tea cup” widoczny jest na mammografach wykonanych w projekcji
Na schemacie oznaczono
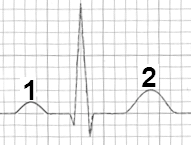
Które zaburzenie rytmu serca zarejestrowano na elektrokardiogramie?
Na schemacie oznaczono
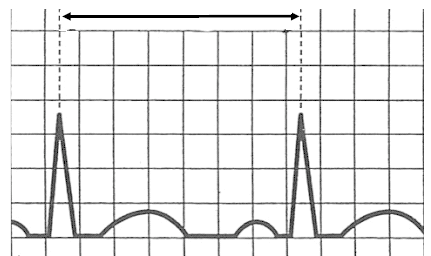
W badaniu EKG elektrodę przedsercową V4 należy umocować
W badaniu PETCT radioizotop ulega
Zgodnie z obowiązującymi przepisami powierzchnia gabinetu rentgenowskiego, w którym jest zainstalowany zestaw rentgenowski do badań naczyniowych, powinna wynosić
Źródłem promieniowania protonowego stosowanego w radioterapii jest
Brachyterapia polegająca na wielokrotnym wsuwaniu i wysuwaniu źródła promieniowania do tego samego aplikatora nosi nazwę
Podczas wykonywania badania EEG elektrodę P4 umieszcza się w okolicy
Przemiana promieniotwórcza radu w ren opisana wzorem \( {}_{88}^{226}\text{Ra} \to {}_{86}^{222}\text{Rn} + {}_{2}^{4}\text{He} \) jest rozpadem