Pytanie 1
Jak oznacza się w radioterapii obszar tkanek zawierający GTV i mikrorozsiewy w fazie niewykrywalnej klinicznie?
Wynik: 26/40 punktów (65,0%)
Wymagane minimum: 20 punktów (50%)
Jak oznacza się w radioterapii obszar tkanek zawierający GTV i mikrorozsiewy w fazie niewykrywalnej klinicznie?
Proces chemicznego wywoływania radiogramów polega na
W badaniu EEG w systemie „10-20” elektrody w okolicy skroniowej oznaczone są literą
Który radioizotop jest emiterem promieniowania alfa?
W której próbie stroikowej przystawia się stroik do czoła (u podstawy nosa) lub na szczycie głowy i porównuje się przewodnictwo kostne ucha prawego i lewego?
Który wynik badania tympanometrycznego potwierdza, że słuch badanego pacjenta jest w granicach normy?
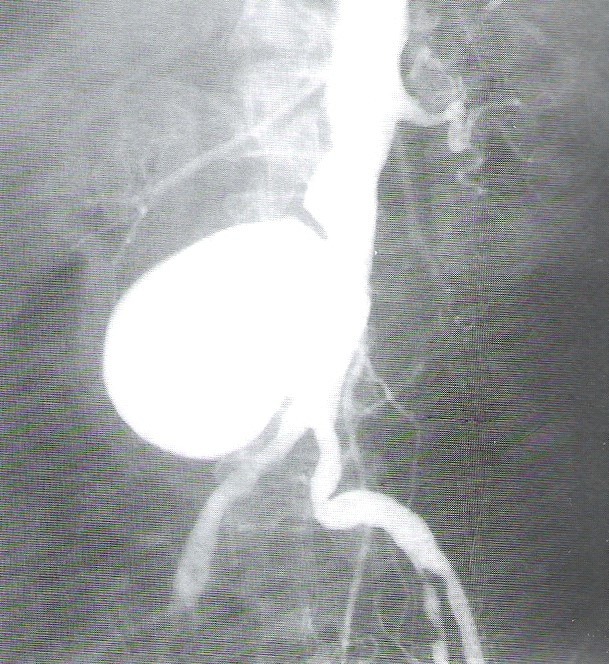
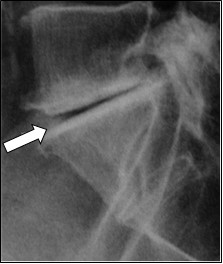
Na obrazie rentgenowskim strzałką zaznaczono
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem
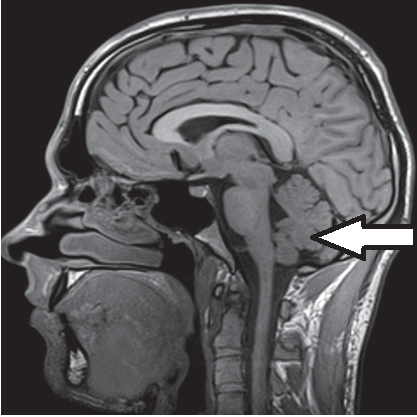
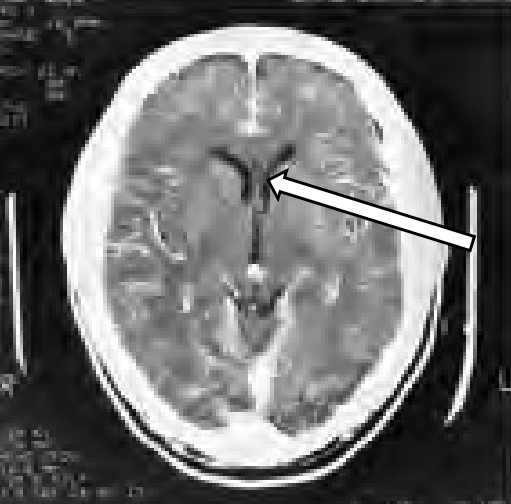
Którą strukturę anatomiczną oznaczono strzałką na obrazie rezonansu magnetycznego?
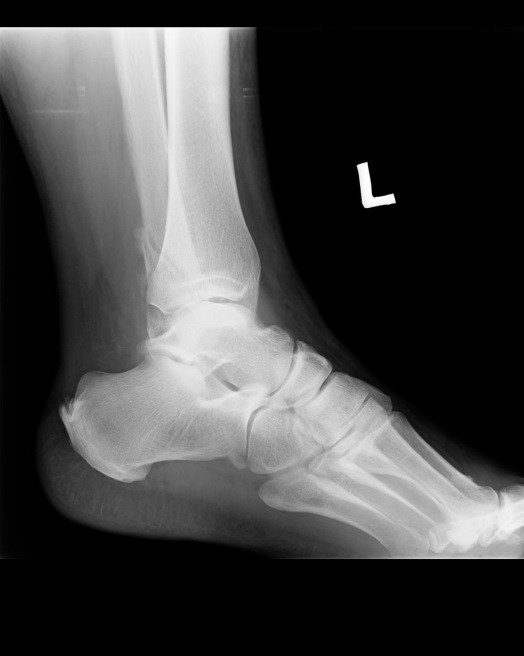
Na obrazie radiologicznym uwidoczniono złamanie kości
Ile razy i jak zmieni się wartość natężenia promieniowania X przy zwiększeniu odległości OF ze 100 cm do 200 cm?
Które ciało obce w obszarze badania nie stanowi przeciwwskazania do wykonania MR?
Który radiofarmaceutyk należy podać pacjentowi w scyntygrafii perfuzyjnej mózgu?
Parametr SNR w obrazowaniu MR oznacza
Rozpoczęcie badania TK nerek po 20-30 sekundach od początku podania środka kontrastowego umożliwia diagnostykę
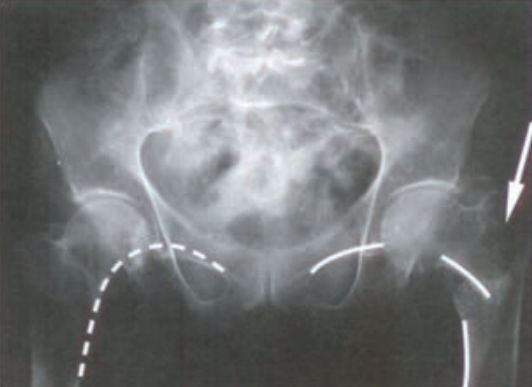
Radiogram przedstawia
Który system informatyczny służy do archiwizacji i transmisji obrazów radiologicznych?
W badaniu MR czas repetycji TR jest parametrem określającym odstęp czasu między
Na rentgenogramie strzałką zaznaczono
Do zdjęcia rentgenowskiego żeber w projekcji skośnej tylnej pacjenta należy ustawić
Czas repetycji w obrazowaniu metodą rezonansu magnetycznego to
Ligand stosuje się
W diagnostyce metodą rezonansu magnetycznego biorą udział
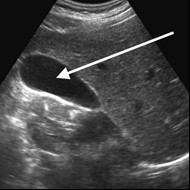
Na obrazie ultrasonograficznym jamy brzusznej strzałką wskazano
Jaki rozmiar kasety należy zastosować, wykonując standardowe zdjęcie stawu kolanowego w projekcji bocznej?
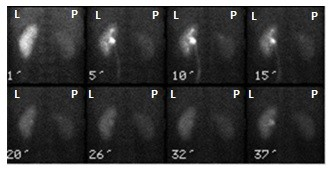
Na zarejestrowanych obrazach badania renoscyntygraficznego widać, że prawa nerka pacjenta
Promieniowanie rentgenowskie powstaje w wyniku hamowania
W radiografii mianem SID określa się
Fala głosowa rozchodzi się
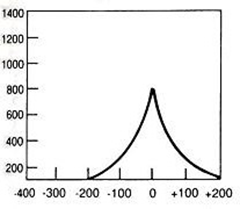
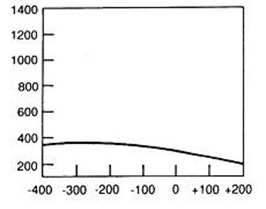
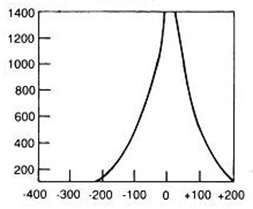
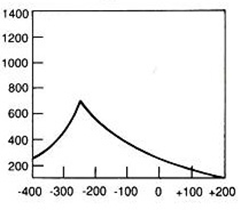
Zamieszczone na ilustracji obrazy dotyczą badania
Na którym z zapisów EKG została uwidoczniona fala Pardee'go?
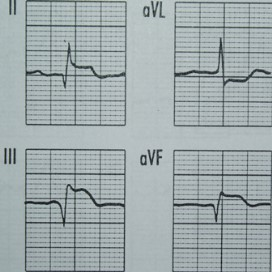
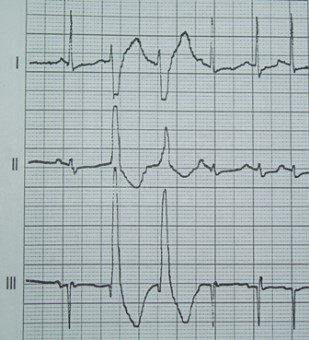
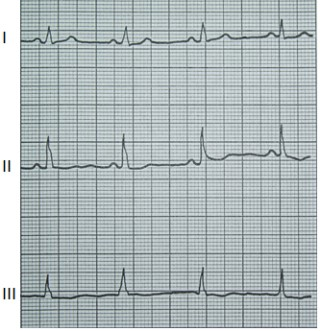
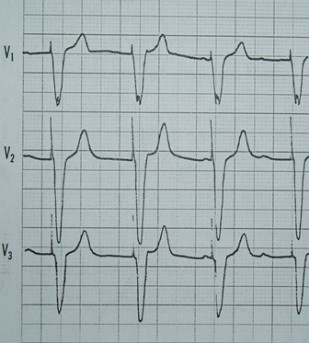
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
Przy podejrzeniu ciała obcego w oczodole należy wykonać
W których projekcjach podstawowych wykonuje się standardowe badanie mammograficzne?
Standardowo do wykonania których zdjęć należy zastosować kratkę przeciwrozproszeniową?
W zapisie EKG prawidłowego rytmu zatokowego wszystkie załamki P są
W obrazowaniu MR wykorzystuje się moment magnetyczny
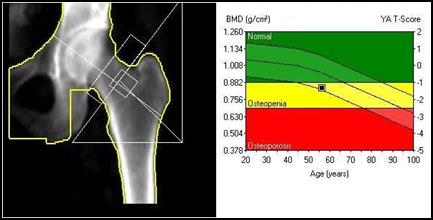
Którą strukturę anatomiczną oznaczono na skanie TK głowy?
Jaki czas należy ustawić do wykonania zdjęcia rentgenowskiego dwójki górnej lewej?
| Tabela ekspozycji | |||
|---|---|---|---|
| wartości | czasu (s) | napięcia (kV) | natężenia (mA) |
| zęby przedtrzonowe i kły | 0,160 | 60 | 8 |
| siekacze | 0,120 | 60 | 8 |
| zęby trzonowe | 0,200 | 60 | 8 |
| ekspozycja zgryzowo-skrzydełkowa | 0,180 | 66 | 6 |
Do prób aktywacyjnych stosowanych w badaniu EEG zalicza się