Pytanie 1
Techniką polegającą na mierzeniu siły elektromotorycznej ogniwa składającego się z dwóch elektrod umieszczonych w analizowanym roztworze jest
Wynik: 22/40 punktów (55,0%)
Wymagane minimum: 20 punktów (50%)
Techniką polegającą na mierzeniu siły elektromotorycznej ogniwa składającego się z dwóch elektrod umieszczonych w analizowanym roztworze jest
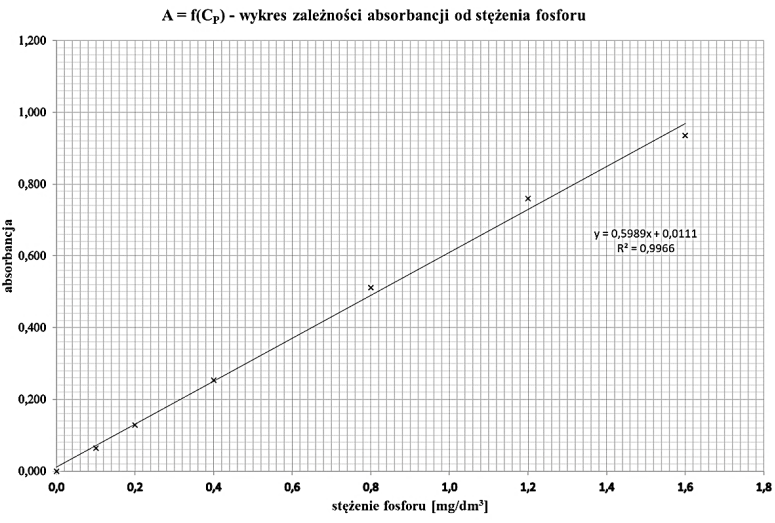
Na rysunku przedstawiono wykres zależności absorbancji od stężenia fosforu. Ile wynosi stężenie fosforu w próbce, jeśli absorbancja dla badanej próbki wynosi A = 0,628?
W procesie oddzielania osadu od cieczy podczas realizacji analiz jakościowych metodą półmikro, używa się
Analiza wody basenowej w celu wykrycia bakterii polega na podgrzewaniu próbki w inkubatorze przez 48 godzin w temperaturze 36±2°C. Jaki proces jest opisany?
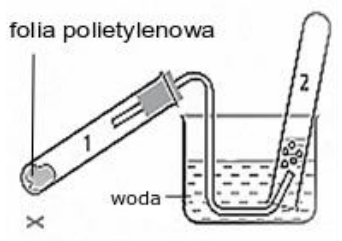
W wyniku przeprowadzenia doświadczenia zgodnie ze schematem, w probówce 2 otrzymano
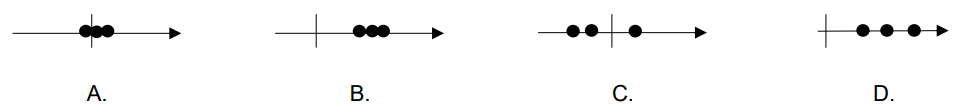
Na którym rysunku przedstawiono schemat metody dokładnej i nieprecyzyjnej?
Parametr jakości wody, który wskazuje minimalną objętość w cm3, w której może znajdować się jedna komórka bakterii Escherichia coli lub innych pokrewnych bakterii żyjących w jelitach człowieka, określa się mianem
Zjawisko opisane w ramce to
| Jeżeli w wodzie zostanie rozpuszczona α-D-glukopiranoza, to roztwór tuż po rozpuszczeniu wykazuje skręcalność właściwą [α]D= +112,2°, lecz w miarę upływu czasu skręcalność ta stopniowo spada do wartości charakterystycznej w stanie równowagi, mianowicie [α]D= +52,7° |
Na podstawie informacji zamieszczonych w tabeli wskaż, do którego rodzaju nawozów azotowych należy saletra potasowa.
| Podział nawozów azotowych | Średnia zawartość azotu [%] | MN = 14 g/mol MO = 16 g/mol MK = 39 g/mol | |
|---|---|---|---|
| I. | saletrzane | 15 | |
| II. | amonowe | 25 | |
| III. | saletrzano-amonowe | 34 | |
| IV. | amidowe | 46 |
W jakich dziedzinach wykorzystuje się wskaźniki metalochromowe?
W jakich oznaczeniach analitycznych wykorzystuje się fenoloftaleinę jako wskaźnik?
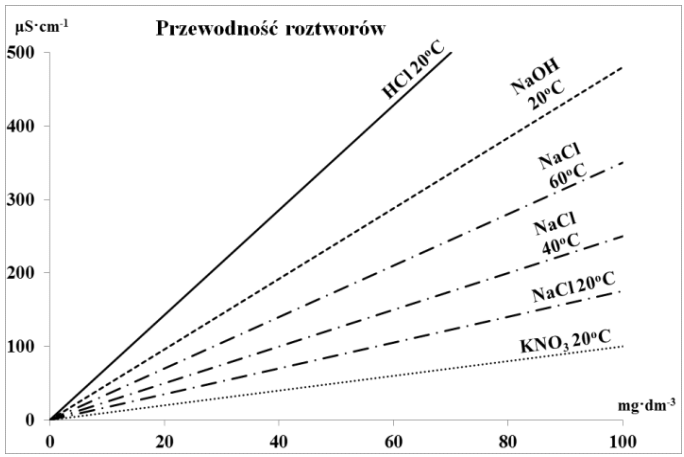
Wykres przedstawia przewodność roztworów kwasów, zasad i soli. Z analizy wykresu wynika, że konduktywność elektrolityczna roztworu
Lepkość oleju napędowego w temperaturze 40°C wynosi 3 mm2/s. Jaką lepkość to określa?
Na podstawie informacji zamieszczonych w tabeli wskaż nazwę badanego związku.
| Dodany odczynnik | Obserwacje |
|---|---|
| Cu(OH)₂ | Zawiesina Cu(OH)₂ rozpuściła się, a roztwór przyjął szafirową barwę |
| Cu(OH)₂ | Po ogrzaniu probówki pojawił się ceglastoczerwony osad |
| [Ag(NH₃)₂]⁺ | Na ściankach probówki pojawiło się srebro metaliczne |
Schemat obrazuje proces rozdzielenia mieszaniny kationów.
Próbka pierwotna (mieszanina kationów)
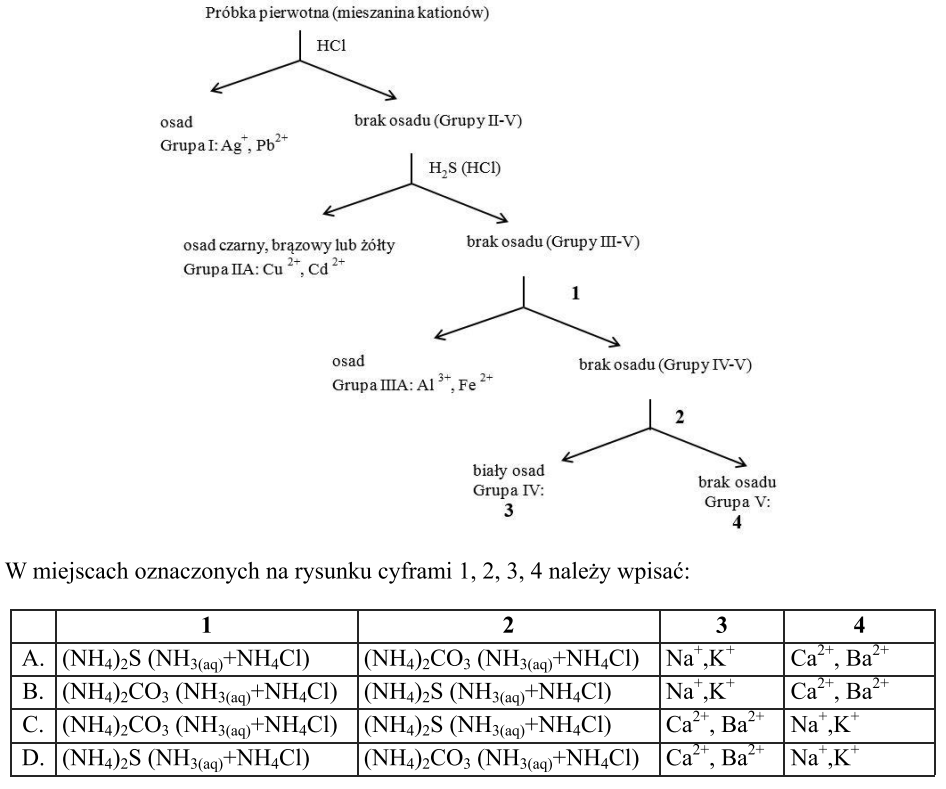
Na schemacie przedstawiono bieg promieni światła w
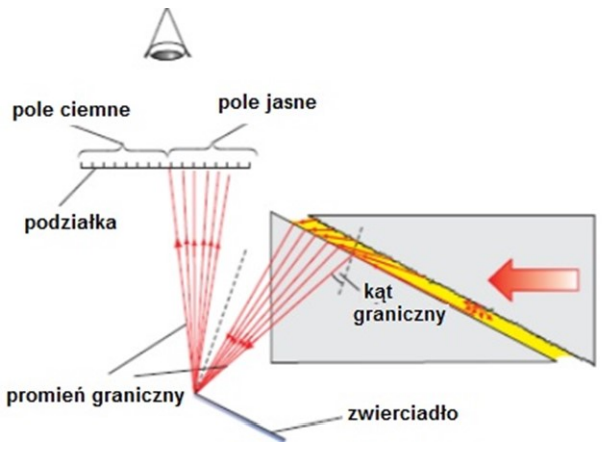
Którą właściwość fizyczną substancji można wyznaczyć za pomocą przyrządu przedstawionego na rysunku?
Proces, w wyniku którego formy wegetatywne mikroorganizmów ulegają zniszczeniu (pozostają jedynie bakterie w postaci spor oraz tzw. wolne wirusy), nazywany jest
Jaką substancję stanowi płyn Lugola, używaną w mikrobiologii do barwienia preparatów według metody Grama?
Na ilustracji przedstawiono

W obecności anionów siarczanowych SO42- w roztworze wodnym, ich obecność można zweryfikować, dodając roztwór
W trakcie analizy przeprowadzonej metodą fotometrii płomieniowej próbkę nawozu o wadze 0,1000 g rozpuszczono w 250 cm3 wody destylowanej. Po wykonaniu badań uzyskano zawartość potasu równą 0,0830 mg/cm3. Jaką wartość procentową K2O ma badany nawóz i czy mieści się ona w normie, jeśli współczynnik przeliczeniowy K na K2O wynosi 1,205, a zawartość procentowa K2O w nawozie powinna być w zakresie 40-50%?
Woda obecna w cząsteczce Ca(OH)2 określana jest jako woda
Jakie cechy powinien mieć preparat mikroskopowy?
Ile miligramów wapnia (MCa = 40,0 g/mol) znajdowało się w analizowanym roztworze, jeśli do zmiareczkowania próbki wykorzystano 20 cm3 0,0100-molowego roztworu EDTA?
Na etykiecie odczynnika chemicznego zawarte są następujące informacje: Z informacji wynika, że odczynnik ten może być zastosowany do sporządzenia roztworu o stężeniu około 0,1 mol/dm3 z dokładnością do
| NH4SCN amonu tiocyjanian | 0,1 mol/dm3 |
| Stężenie po rozcieńczeniu do 1000 cm3 w 20°C | 0,1 mol/dm3 ± 0,2 % |
Roztwór zawierający aniony I grupy analitycznej poddano identyfikacji metodą chromatografii cienkowarstwowej. Na chromatogramie uwidoczniono dwie plamki w odległości 5,6 cm i 3,5 cm od linii startu. Odległość czoła eluenta od linii startu wyniosła 10,1 cm, a wartości wskaźników Rf wzorców anionów wynoszą jak w tabeli. Które z anionów zawierała badana próbka?
| Anion | Cl- | Br- | I- | SCN- |
|---|---|---|---|---|
| Wskaźnik Rf | 0,243 | 0,352 | 0,554 | 0,648 |
W próbce wody pitnej o objętości 100 cm3 oznaczono zawartość azotanów 4 mg, chlorków 23 mg, manganu 0,006 mg i żelaza 0,01 mg. Korzystając z danych zawartych w tabeli, można stwierdzić, że badana woda
| Tabela. Wybrane parametry, jakim powinna odpowiadać woda do picia | ||
|---|---|---|
| Wskaźnik jakości wody | Jednostka | Najwyższe dopuszczalne stężenie lub zakres |
| Barwa | mgPt/l | 15 |
| Mętność | NTU | 1 |
| Zapach | - | akceptowalny |
| Odczyn | pH | 6,5 – 9,5 |
| Przewodność | μS/cm w 20°C | 2500 |
| Azotany | mg/l | 50 |
| Chlorki | mg/l | 250 |
| Chlor – wolny | mg/l | 0,1 – 0,3 |
| Mangan | mg/l | 0,05 |
| Twardość ogólna | mg CaCO₃/l | 60 - 500 |
| Twardość niewęglanowa | mval/l | - |
| Utlenialność | mgO₂/l | 5 |
| Żelazo | mg/l | 0,2 |
Wyznacz refrakcję molową (Rm) dla kwasu octowego korzystając z danych zawartych w tabeli.
Rm = ∑a ∙ Ra gdzie: a – liczba atomów jednego rodzaju, Ra – refrakcja atomowa

Białka, których cząsteczki mają wiązania peptydowe, w reakcji z jonami miedzi(II) w środowisku zasadowym tworzą kompleks o barwie fioletowej. Stopień intensywności barwy jest proporcjonalny do liczby wiązań peptydowych. Tę zależność można wykorzystać do oznaczeń
Która z podanych metod analitycznych jest klasyfikowana jako technika łączona?
Określ typ destylacji, który polega na przemianie składnika mieszaniny substancji organicznych w stan pary w temperaturze niższej od jego temperatury wrzenia.
Do analizy pobrano próbkę o masie 200 mg. Na podstawie informacji zamieszczonych w tabeli określ, w jakiej skali będzie wykonana ta analiza.
| Wielkość próbki | Skala analizy |
|---|---|
| > 0,1 g | makro |
| 0,01 – 0,1 g | semimikro |
| 0,0001 – 0,01 g | mikro |
| < 10-4 g | ultramikro |
Izomerazy uczestniczą w reakcjach przekształceń wewnętrznych cząsteczek, nie powodując rozkładu struktury związku ani zmiany składu atomowego. Proces ten przedstawia schemat
Najmniejsze stężenie lub ilość badanego składnika w analizowanej próbce, przy którym można jeszcze wykonać jego oznaczenie, to
Skróconym badaniom poddano próbki wody z 4 ujęć. Wyniki zapisano w tabeli. Na podstawie analizy danych zawartych w tabelach wskaż zestaw próbek spełniających wymagania jakościowe.
| Wyniki badań próbek wody z 4 ujęć | ||||
|---|---|---|---|---|
| Wskaźnik organoleptyczny | Próbka 1 | Próbka 2 | Próbka 3 | Próbka 4 |
| Barwa (Pt) | 10 | 20 | 15 | 20 |
| Odczyn (pH) | 7,5 | 6,5 | 6,8 | 8,8 |
| Mętność | 5 | 4 | 3 | 5 |
| Zapach | 3 – naturalny, nieuciążliwy | 3 – naturalny, nieuciążliwy | 3 – nieuciążliwy, wyczuwalny zapach chloru | 3 – naturalny, nieuciążliwy |
| Zawiesiny, plamy oleju, itp. | Niewidoczne w szklanych naczyniach | Niewidoczne w szklanych naczyniach | Niewidoczne w szklanych naczyniach | Niewidoczne w szklanych naczyniach |
| Warunki organoleptyczne, jakim powinna odpowiadać woda do picia i na potrzeby gospodarcze | ||||
| Lp. | Wskaźniki organoleptyczne, Nazwa substancji | Jednostka miary | Najwyższa dopuszczalna dawka lub przedział | |
| 1 | Barwa (Pt) | mg · dm-3 | 20 | |
| 2 | Odczyn (pH) | ---- | 6,5 – 8,5 | |
| 3 | Mętność | mg · dm-3 | 5 | |
| 4 | Zapach | ---- | 3 – naturalny, nieuciążliwy, dopuszczalny zapach chloru przy dezynfekcji chlorem | |
| 5 | Zawiesiny, plamy oleju itp. | ---- | Niewidoczne w szklanych naczyniach | |
Jakie jednostki stosuje się do określenia tzw. indeksu nadmanganianowego, który symbolicznie reprezentuje ilość związków organicznych w wodzie pitnej?
Przy pomocy polarymetru wykonuje się pomiar
Przedstawione reakcje zachodzą w produktach żywnościowych podczas fermentacji
| C12H22O11 + H2O → C6H12O6 + C6H12O6 |
| C6H12O6 → 2 CH3 −CH(OH) −COOH |
W świadectwie jakości roztworu amoniaku cz. podana jest informacja: zawartość amoniaku 30÷32% m/m Uwzględniając informacje zawarte w tabeli, określ gęstość tego roztworu w temperaturze 20°C.
| Zależność gęstości roztworu amoniaku od stężenia w 20°C | |||||||
|---|---|---|---|---|---|---|---|
| % wagowy | 1 | 6 | 10 | 16 | 20 | 26 | 30 |
| gęstość [g/cm³] | 0,9939 | 0,9730 | 0,9575 | 0,9362 | 0,9229 | 0,9040 | 0,8920 |