Pytanie 1
Co zostało uwidocznione na zamieszczonym radiogramie?
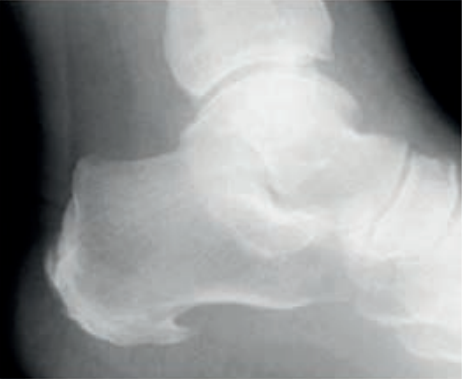
Wynik: 3/40 punktów (7,5%)
Wymagane minimum: 20 punktów (50%)
Co zostało uwidocznione na zamieszczonym radiogramie?

Zamieszczony rentgenogram został zarejestrowany podczas wykonania
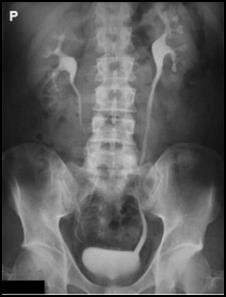
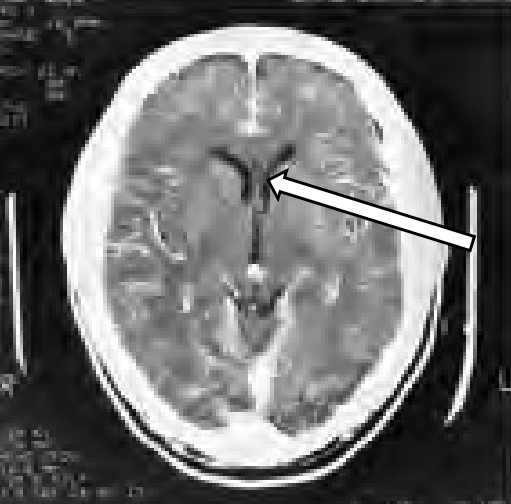
Na radiogramie TK głowy strzałką wskazano
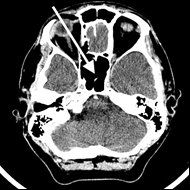
Zamieszczony obraz został wykonany metodą
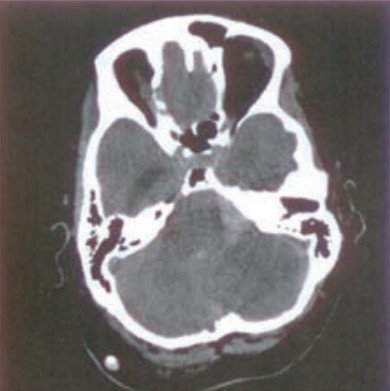
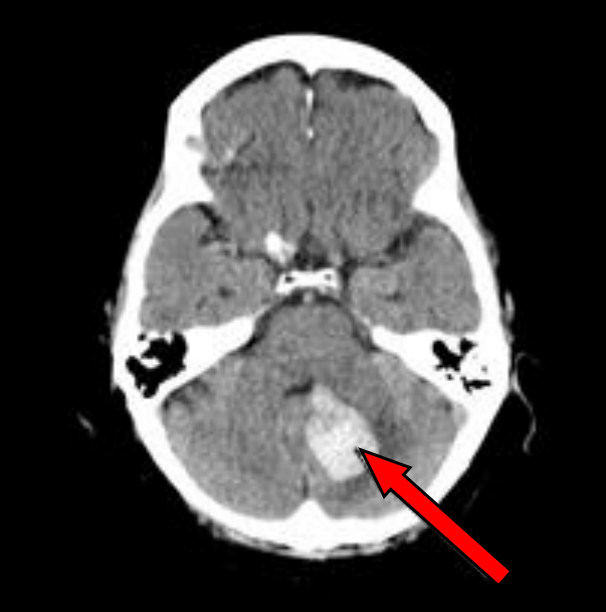
Którą strukturę anatomiczną oznaczono na skanie TK głowy?
W brachyterapii MDR stosowane są dawki promieniowania
Brak odpowiedzi na to pytanie.
Chorobą układu oddechowego typu obturacyjnego jest
Brak odpowiedzi na to pytanie.
Na przekroju poprzecznym TK mózgu strzałką wskazano obszar
Brak odpowiedzi na to pytanie.
Gdzie znajduje się węzeł zatokowo-przedsionkowy wywołujący rytmiczne skurcze mięśnia serca?
Brak odpowiedzi na to pytanie.
Przy ułożeniu do zdjęcia AP czaszki płaszczyzna
Brak odpowiedzi na to pytanie.
W badaniu EEG w systemie „10-20” elektrody w okolicy skroniowej oznaczone są literą
Brak odpowiedzi na to pytanie.
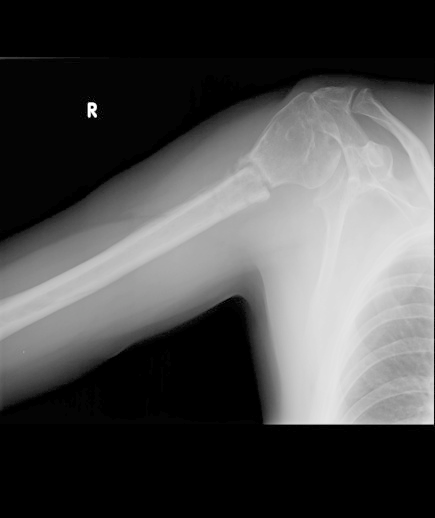
Na radiogramie uwidoczniono złamanie
Brak odpowiedzi na to pytanie.
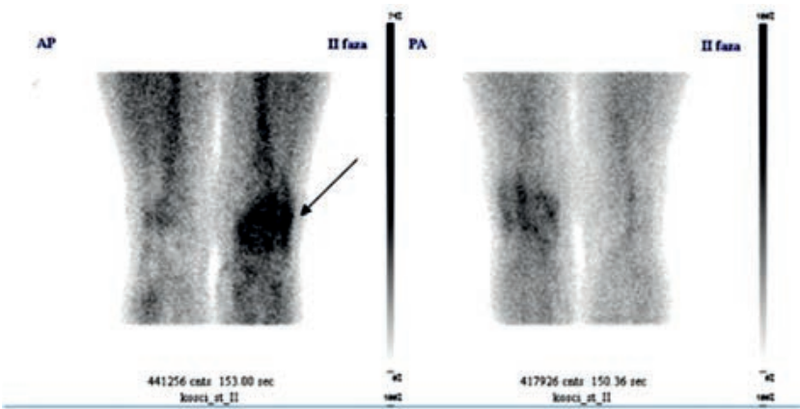
„Ognisko zimne” w obrazie scyntygraficznym określa się jako
Brak odpowiedzi na to pytanie.
Planowany obszar napromieniania PTV obejmuje
Brak odpowiedzi na to pytanie.
Na przedstawionym scyntygramie ukazano duży obszar
Brak odpowiedzi na to pytanie.
Na rentgenogramie przedstawione jest złamanie Saltera-Harrisa typu
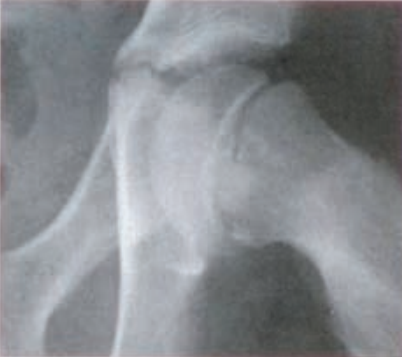
Brak odpowiedzi na to pytanie.
Przy podejrzeniu ciała obcego w oczodole należy wykonać
Brak odpowiedzi na to pytanie.
Na radiogramie czaszki strzałką zaznaczono
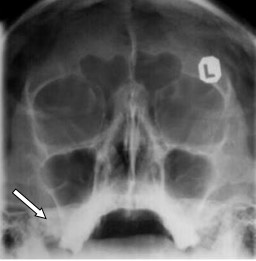
Brak odpowiedzi na to pytanie.
Który system informatyczny służy do archiwizacji i transmisji obrazów radiologicznych?
Brak odpowiedzi na to pytanie.
Który parametr ekspozycji ma decydujący wpływ na kontrast obrazu rentgenowskiego?
Brak odpowiedzi na to pytanie.
Na obrazie ultrasonograficznym jamy brzusznej uwidoczniono
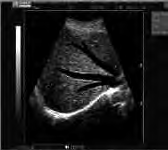
Brak odpowiedzi na to pytanie.
W pozytonowej emisyjnej tomografii komputerowej PET radioznacznik podawany jest pacjentowi najczęściej
Brak odpowiedzi na to pytanie.
Na obrazie RM uwidoczniono odcinek kręgosłupa
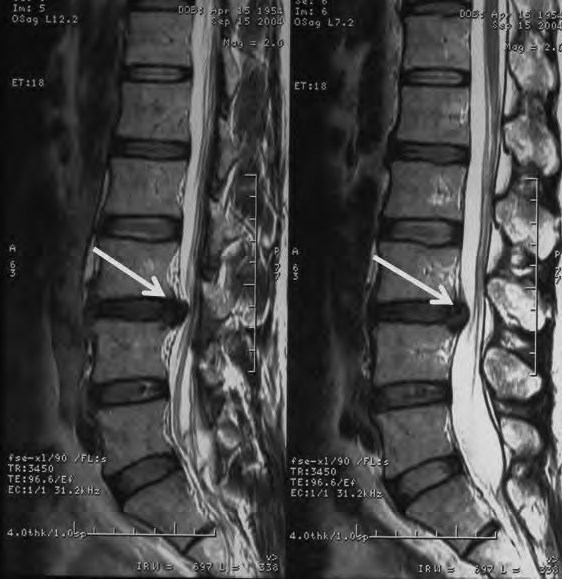
Brak odpowiedzi na to pytanie.
Podczas wykonywania badania EEG elektrodę P4 umieszcza się w okolicy
Brak odpowiedzi na to pytanie.
Na zamieszczonym obrazie TK strzałką zaznaczono zatokę
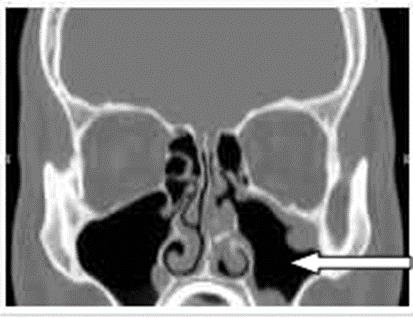
Brak odpowiedzi na to pytanie.
W celu maksymalnego ograniczenia dawki promieniowania badanie rentgenowskie u dzieci należy wykonać
Brak odpowiedzi na to pytanie.
Teleradioterapia 4D na etapie planowania leczenia wykorzystuje obrazy
Brak odpowiedzi na to pytanie.
Brachyterapia polegająca na wielokrotnym wsuwaniu i wysuwaniu źródła promieniowania do tego samego aplikatora nosi nazwę
Brak odpowiedzi na to pytanie.
Zgodnie z obowiązującymi przepisami powierzchnia gabinetu rentgenowskiego, w którym jest zainstalowany zestaw rentgenowski do badań naczyniowych, powinna wynosić
Brak odpowiedzi na to pytanie.
Obrazowanie portalowe w radioterapii służy do
Brak odpowiedzi na to pytanie.
Zamieszczone badanie elektrokardiograficzne wykazało u pacjenta
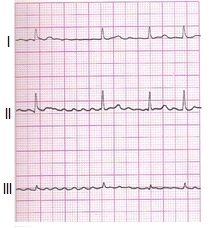
Brak odpowiedzi na to pytanie.
W badaniu EKG różnice potencjałów pomiędzy lewym podudziem a lewym przedramieniem rejestruje odprowadzenie
Brak odpowiedzi na to pytanie.
Jak oznacza się w radioterapii obszar tkanek zawierający GTV i mikrorozsiewy w fazie niewykrywalnej klinicznie?
Brak odpowiedzi na to pytanie.
Artefakty zarejestrowane na elektrokardiogramie zostały wywołane przez
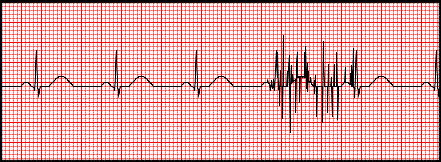
Brak odpowiedzi na to pytanie.
Na prawidłowo wykonanym zdjęciu zatok w projekcji PA górny zarys piramid rzutuje się
Brak odpowiedzi na to pytanie.
Testy specjalistyczne aparatów rentgenowskich do zdjęć wewnątrzustnych są przeprowadzane
Brak odpowiedzi na to pytanie.
Przyczyną zaniku kostnego jest
Brak odpowiedzi na to pytanie.
Podczas badania EEG w systemie „10-20” literą A oznacza się elektrody
Brak odpowiedzi na to pytanie.
Zamieszczony elektrokardiogram przedstawia
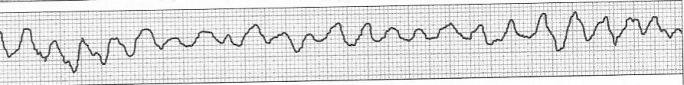
Brak odpowiedzi na to pytanie.
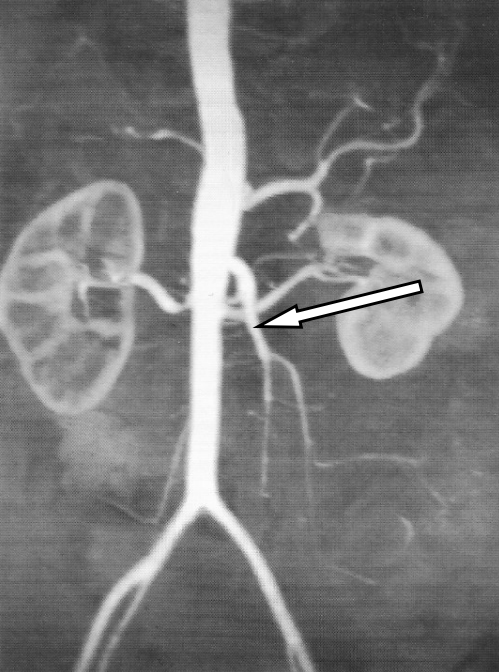
Którą tętnicę zaznaczono strzałką na obrazie MR?
Brak odpowiedzi na to pytanie.