Pytanie 1
Która sekwencja obrazowania MR wykorzystuje impulsy RF o częstotliwości rezonansowej tłuszczu do tłumienia sygnału pochodzącego z tkanki tłuszczowej?
Wynik: 27/40 punktów (67,5%)
Wymagane minimum: 20 punktów (50%)
Która sekwencja obrazowania MR wykorzystuje impulsy RF o częstotliwości rezonansowej tłuszczu do tłumienia sygnału pochodzącego z tkanki tłuszczowej?
Kiedy w procesie terapii wykonuje się badanie CBCT (cone beam computed tomography)?
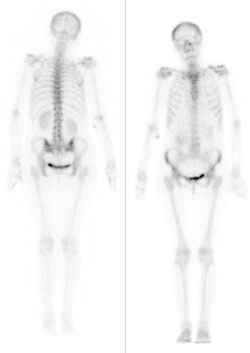
Na obrazie uwidoczniono
Elementem systemu rejestracji obrazu, w którym fotony promieniowania X są bezpośrednio konwertowane na sygnał elektryczny, jest
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
W badaniu PETCT radioizotop ulega
Na zamieszczonej rycinie przedstawiono
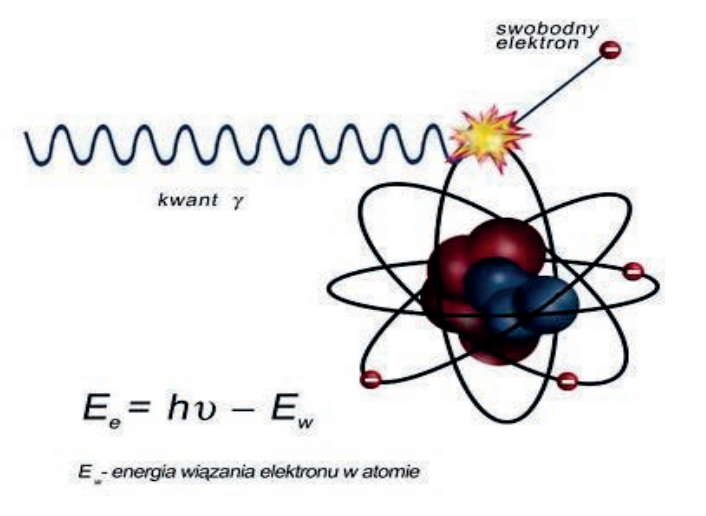
Na ilustracji przedstawiono zjawisko
Ligand stosuje się
Warstwa półchłonna (WP) jest wyrażona w mm Cu dla
W obrazowaniu metodą rezonansu magnetycznego T1 oznacza czas
Jaki czas należy ustawić do wykonania zdjęcia rentgenowskiego dwójki górnej lewej?
| Tabela ekspozycji | |||
|---|---|---|---|
| wartości | czasu (s) | napięcia (kV) | natężenia (mA) |
| zęby przedtrzonowe i kły | 0,160 | 60 | 8 |
| siekacze | 0,120 | 60 | 8 |
| zęby trzonowe | 0,200 | 60 | 8 |
| ekspozycja zgryzowo-skrzydełkowa | 0,180 | 66 | 6 |
Zwiększenie napięcia na lampie rentgenowskiej powoduje
Który obszar napromieniania w radioterapii oznacza się skrótem PTV?
Powierzchnia gabinetu rentgenowskiego, w którym zainstalowany jest aparat rentgenowski wyposażony w oddzielną lampę, nie może być mniejsza niż
Objawem późnego odczynu popromiennego po teleradioterapii jest
Który radiofarmaceutyk może zostać podany pacjentowi w scyntygrafii perfuzyjnej mózgu?
Elementem pomocniczym w radioterapii, zapewniającym powtarzalność ułożenia w pozycji terapeutycznej, a także unieruchomienie pacjenta, jest
Na którym obrazie TK uwidoczniony jest artefakt spowodowany ruchami oddechowymi pacjenta?
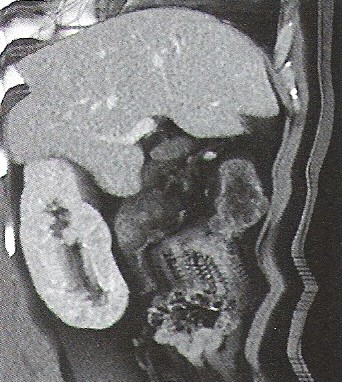
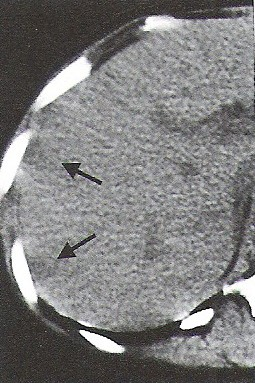

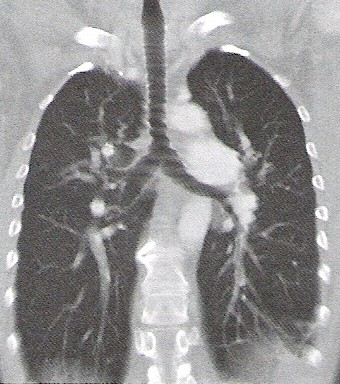
W której technice brachyterapii stosuje się źródła promieniowania o mocy dawki 2-12 Gy/h?
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
Przedstawiony obraz został zarejestrowany podczas wykonywania
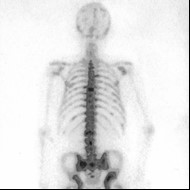
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Testy specjalistyczne aparatów rentgenowskich do zdjęć wewnątrzustnych są przeprowadzane
Największa wartość energii promieniowania stosowanego w radioterapii jest generowana przy użyciu
Na zarejestrowanych obrazach badania renoscyntygraficznego widać, że prawa nerka pacjenta
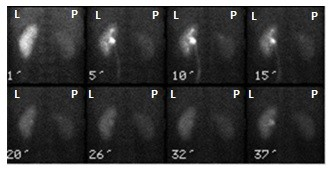
W medycynie nuklearnej wykorzystuje się:
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Folia wzmacniająca umieszczona w kasecie rentgenowskiej emituje pod wpływem promieniowania X światło
W leczeniu izotopowym tarczycy podaje się
Centratory laserowe zamontowane w kabinie aparatu terapeutycznego służą do
W celu maksymalnego ograniczenia dawki promieniowania badanie rentgenowskie u dzieci należy wykonać
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
Która struktura może być oknem akustycznym w badaniu ultrasonograficznym?
Wskaż roczną dawkę graniczną dla osób zatrudnionych w warunkach narażenia na promieniowanie jonizujące.
Planowany obszar napromieniania PTV obejmuje
Pracownia radioterapii z przyspieszaczem liniowym jest obszarem
Osłony na gonady dla osób dorosłych powinny posiadać równoważnik osłabienia promieniowania nie mniejszy niż
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Glukoza podawana pacjentowi w badaniu PET jest znakowana radioaktywnym