Pytanie 1
Zamieszczony piktogram przedstawia substancję o klasie i kategorii zagrożenia:

Wynik: 28/40 punktów (70,0%)
Wymagane minimum: 20 punktów (50%)
Zamieszczony piktogram przedstawia substancję o klasie i kategorii zagrożenia:

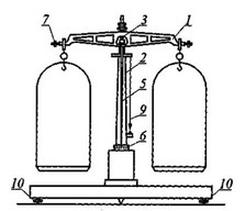
Rysunek przedstawia wagę techniczną. Numerem 7 oznaczono
Zamieszczony piktogram odnosi się do substancji o klasie i kategorii zagrożenia:
Podstawowa substancja w analizie miareczkowej charakteryzuje się następującymi właściwościami:
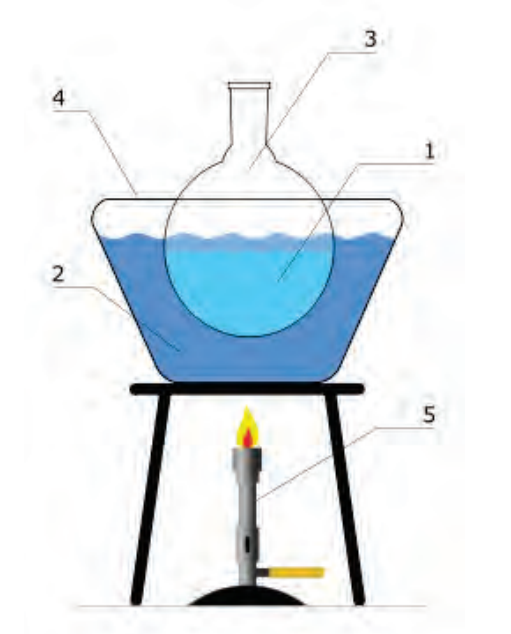
Jak nazywa się naczynie o płaskim dnie, które wykorzystuje się do pozyskiwania substancji stałej poprzez stopniowe odparowanie rozpuszczalnika z roztworu?
Mając wagę laboratoryjną z dokładnością pomiaru 10 mg, nie da się wykonać odważki o masie
Podczas analizowania zmienności składu wód płynących w skali rocznej, próbki wody powinny być zbierane i badane przynajmniej raz na
Aby przygotować 0,5 dm3 roztworu HCl o stężeniu 0,2 mol/dm3, jaką kolbę miarową o pojemności należy wykorzystać?
Na podstawie informacji zawartych w tabeli określ, który parametr spośród podanych należy oznaczyć w pierwszej kolejności.
| Tabela. Sposoby utrwalania próbek wody i ścieków, miejsce analizy, dopuszczalny czas przechowywania próbek | ||||
|---|---|---|---|---|
| Oznaczany parametr | Rodzaj naczynia do przechowywania próbki | Sposób utrwalania próbki | Miejsce wykonania analizy | Dopuszczalny czas przechowywania próbki |
| Chlorki | szklane lub polietylenowe | - | laboratorium | 96 godzin |
| Chlor pozostały | szklane | - | w miejscu pobrania próbki | - |
| ChZT | szklane | zakwaszenie do pH<2, schłodzenie do temperatury 2-5°C | laboratorium | 24 godziny |
| Kwasowość | szklane lub polietylenowe | schłodzenie do temperatury 2-5°C | laboratorium | 4 godziny |
| Mangan | szklane lub polietylenowe | zakwaszenie do pH<2, schłodzenie do temperatury 2-5°C | laboratorium | 48 godziny |
Podczas reakcji chlorku żelaza(III) z wodorotlenkiem potasu dochodzi do wytrącenia wodorotlenku żelaza(III) w formie
Aby uzyskać wodorotlenek wapnia, odważono 30 g węglanu wapnia, który następnie wyprażono. Powstały tlenek wapnia dodano do 100 cm3 wody, a otrzymany osad wysuszono i zważono, uzyskując 18,5 g wodorotlenku wapnia. Jaką wydajność miała ta reakcja?
Ca – 40 g/mol; O – 16 g/mol; C – 12 g/mol; H – 1 g/mol
Opis w ramce przedstawia sposób oczyszczania substancji poprzez
| Próbke substancji stałej należy umieścić w kolbie kulistej, zaopatrzonej w chłodnicę zwrotną, dodać rozpuszczalnika - etanolu i delikatnie ogrzewać do wrzenia. Po lekkim ostudzeniu dodać do roztworu niewielką ilość węgla aktywnego, zagotować i przesączyć na gorąco. Przesącz pozostawić do ostygnięcia, a wydzielony osad odsączyć pod zmniejszonym ciśnieniem, przemyć niewielką ilością rozpuszczalnika, przenieść na szalkę, pozostawić do wyschnięcia, a następnie zważyć. |
W trakcie kalibracji stężenia roztworu kwasu solnego na przynajmniej przygotowany roztwór zasady sodowej ma miejsce reakcja
Na etykiecie odważki analitycznej znajduje się napis: Z odważki tej można przygotować
Odważka analityczna azotan(V) srebra(I) AgNO3 0,1 mol/dm3 |
Jakie jest stężenie molowe kwasu siarkowego(VI) o zawartości 96% i gęstości 1,84 g/cm3?
Elementami brakującymi w zestawie przedstawionym na rysunku są
Na etykiecie próbki środowiskowej należy umieścić datę jej pobrania, lokalizację poboru oraz
Etykiety chemikaliów zawierają zwroty H, które informują o rodzaju zagrożenia. Cyfra "3" pojawiająca się po literze "H" w oznaczeniu, definiuje rodzaj zagrożenia?
Jakiego koloru nabierze lakmus w roztworze NaOH?
Czego się używa w produkcji z porcelany?
Kalibracja pH-metru nie jest potrzebna po
Próbkę uzyskaną z próbki ogólnej poprzez jej zmniejszenie nazywa się
Aby przygotować 500 g roztworu o stężeniu 10% (m/m), ile substancji należy odważyć?
Aby podnieść temperaturę roztworu do 330 K, jakie wyposażenie jest potrzebne?
Które równanie przedstawia reakcję otrzymywania mydła?
| CH3COOH + NaOH →CH3COONa + H2O | 2 CH3COOH + Na2O →2 CH3COONa + H2O | 2 C2H5COOH + 2 Na →2 C2H5COONa + H2↑ | C17H35COOH + NaOH →C17H35COONa + H2O |
Jakim przyrządem nie jest możliwe określenie gęstości cieczy?
Jakie urządzenie wykorzystuje się do określania lepkości płynów?
Wskaź zestaw reagentów oraz przyrządów wymaganych do przygotowania 0,5 dm3 roztworu HCl o stężeniu 0,2 mol/dm3?
Jakie są zalecenia dotyczące postępowania z odpadowymi roztworami kwasów oraz zasad?
Aby wykonać chromatografię cienkowarstwową, należy przygotować eluent składający się z toluenu, acetonu oraz kwasu mrówkowego w proporcjach objętościowych 10:4:1. Jakie ilości poszczególnych składników powinny być wykorzystane do uzyskania 300 cm3 eluentu?
Z próbki zawierającej siarczany(VI) należy najpierw wydzielić metodą filtracji zanieczyszczenia, które są nierozpuszczalne w wodzie. Dokładność wypłukania tych zanieczyszczeń weryfikuje się za pomocą roztworu
Jaką próbkę stanowi woreczek gleby pobranej zgodnie z instrukcją?
| Instrukcja pobierania próbek glebowych | |
| Próbki pierwotne pobiera się laską glebową z wierzchniej warstwy gleby 0-20 cm, kolejno wykonując czynności: – w miejscu pobierania próbki pierwotnej (pojedynczej), rolę świeżo zaoraną przydeptać, – pionowo ustawić laskę do powierzchni gleby, – wcisnąć laskę do oporu (na wysokość poprzeczki ograniczającej), – wykonać pełny obrót i wyjąć laskę, – zawartość wgłębienia (zasobnika) przenieść do pojemnika skrobaczki. Po pobraniu próbek pojedynczych, całość wymieszać i napełnić kartonik lub woreczek. | |
Przedstawiony schemat ideowy ilustruje proces syntezy z propanu C3H8 → C3H7Cl → C3H6 → C3H6(OH)2 → C3H5(OH)2Cl → C3H5(OH)3
Aby ustalić miano roztworu wodnego NaOH, należy zastosować
W którym z podanych równań reakcji dochodzi do zmiany stopni utlenienia atomów?
300 cm3 zanieczyszczonego benzenu poddano procesowi destylacji. Uzyskano 270 cm3 czystej substancji. Jaką wydajność miało oczyszczanie?
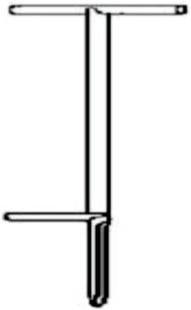
Jakie urządzenie wykorzystuje się do pobierania próbek gazów?
Na rysunku przedstawiony jest przyrząd do poboru próbek
Które z poniższych działań należy wykonać przed rozpoczęciem pracy z nowym szkłem laboratoryjnym?
Podczas przygotowywania roztworu mianowanego kwasu solnego o określonym stężeniu należy: