Pytanie 1
Laboratoryjna apteczka powinna zawierać m.in.
Wynik: 19/40 punktów (47,5%)
Wymagane minimum: 20 punktów (50%)
Laboratoryjna apteczka powinna zawierać m.in.
W trakcie destylacji cieczy wykorzystuje się tzw. kamienie wrzenne, ponieważ
Gdzie należy przechowywać cyjanek potasu KCN?
Proces oddzielania składników jednorodnej mieszaniny, polegający na eliminacji jednego lub większej ilości składników z roztworu lub substancji stałej przy użyciu odpowiednio wybranego rozpuszczalnika, to
Jaką masę chlorku sodu można znaleźć w 150 g roztworu soli o stężeniu 5% (m/m)?
Metoda oczyszczania substancji oparta na różnicach w rozpuszczalności poszczególnych składników w określonym rozpuszczalniku to
Które z wymienionych reakcji chemicznych stanowi reakcję redoks?
Która część małej partii materiału jest najczęściej pobierana w celu przygotowania próbki ogólnej?
Jaką metodę wykorzystuje się w laboratorium do rozdzielenia osadu AgCl od cieczy macierzystej w probówkach?
Opis w ramce przedstawia sposób oczyszczania substancji poprzez
| Próbke substancji stałej należy umieścić w kolbie kulistej, zaopatrzonej w chłodnicę zwrotną, dodać rozpuszczalnika - etanolu i delikatnie ogrzewać do wrzenia. Po lekkim ostudzeniu dodać do roztworu niewielką ilość węgla aktywnego, zagotować i przesączyć na gorąco. Przesącz pozostawić do ostygnięcia, a wydzielony osad odsączyć pod zmniejszonym ciśnieniem, przemyć niewielką ilością rozpuszczalnika, przenieść na szalkę, pozostawić do wyschnięcia, a następnie zważyć. |
Na rysunku przedstawiono próbnik do pobierania próbek

Urządzeniem pomiarowym nie jest
Aby przygotować zestaw do filtracji, należy zebrać
Między wodorotlenkiem baru a chlorkiem amonu dochodzi do spontanicznej reakcji, która powoduje silne schłodzenie mieszaniny oraz wydobycie się charakterystycznego zapachu amoniaku.
Ba(OH)2(s) + 2 NH4Cl(s) → BaCl2(aq) + 2 H2O(c) + 2 NH3(g) Wskaź, które sformułowanie właściwie wyjaśnia to zjawisko.
nieodwracalnie jej równowagę.
Jakie urządzenie jest wykorzystywane do oczyszczania próbki gazowej?
Czułość bezwzględna wagi definiuje się jako
Podczas łączenia bezwodnego etanolu z wodą występuje zjawisko kontrakcji. Gdy zmieszamy 1000 cm3 wody oraz 1000 cm3 etanolu, otrzymujemy roztwór o objętości
Kalibracja pH-metru nie jest potrzebna po
Reakcja neutralizacji wodorotlenku sodu z kwasem solnym zrealizowana jest zgodnie z równaniem:
NaOH + HCl → NaCl + H2O Masy molowe: MNaOH = 40 g/mol, MHCl = 36,5 g/mol Aby zneutralizować 10 g wodorotlenku sodu, wymagane jest
Proces wydobywania składnika z cieczy lub ciała stałego w mieszance wieloskładnikowej poprzez jego rozpuszczenie w odpowiednim rozpuszczalniku to
Podczas pobierania skoncentrowanego roztworu kwasu solnego konieczne jest pracowanie w włączonym dygestorium oraz zastosowanie
Rozdział składników mieszaniny w chromatografii odbywa się dzięki ich różnym
Jakim narzędziem dokonuje się poboru próbki wody?
Po zakończeniu pomiarów pH, elektrody powinny być przepłukane
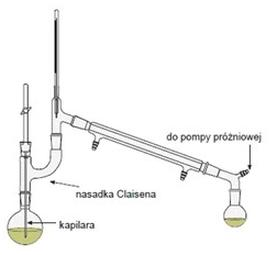
Przedstawiony na rysunku zestaw służy do destylacji
Próbki pobrano z materiału o objętości \( 100 \, \text{m}^3 \), wysypanego z opakowania. Liczba miejsc poboru próbek pierwotnych z tego materiału wynosi:
$$ n = 0{,}5 \cdot \sqrt{V} $$ gdzie:
\( V \) – objętość jednostki badanej w \( \text{m}^3 \)
\( n \) – liczba miejsc poboru próbek
Elementami brakującymi w zestawie przedstawionym na rysunku są
Zestaw do filtracji nie zawiera
Nie należy używać gorącej wody do mycia
Na podstawie informacji zawartych w tabeli określ, który parametr spośród podanych należy oznaczyć w pierwszej kolejności.
| Tabela. Sposoby utrwalania próbek wody i ścieków, miejsce analizy, dopuszczalny czas przechowywania próbek | ||||
|---|---|---|---|---|
| Oznaczany parametr | Rodzaj naczynia do przechowywania próbki | Sposób utrwalania próbki | Miejsce wykonania analizy | Dopuszczalny czas przechowywania próbki |
| Chlorki | szklane lub polietylenowe | - | laboratorium | 96 godzin |
| Chlor pozostały | szklane | - | w miejscu pobrania próbki | - |
| ChZT | szklane | zakwaszenie do pH<2, schłodzenie do temperatury 2-5°C | laboratorium | 24 godziny |
| Kwasowość | szklane lub polietylenowe | schłodzenie do temperatury 2-5°C | laboratorium | 4 godziny |
| Mangan | szklane lub polietylenowe | zakwaszenie do pH<2, schłodzenie do temperatury 2-5°C | laboratorium | 48 godziny |
Jakie urządzenie wykorzystuje się do pomiaru lepkości cieczy?
Rozpuszczalniki organiczne powinny być składowane
Na podstawie danych w tabeli wskaż, którego środka suszącego można użyć do osuszenia związku o wzorze (CH3)2CO
| Środek suszący | Stosowany do suszenia | Nie nadaje się do suszenia |
|---|---|---|
| Na | Eter, węglowodory, aminy trzeciorzędowe | Chlorowcopochodne węglowodorów |
| CaCl₂ | Węglowodory, aceton, eter, gazy obojętne | Alkohole, amoniak, aminy |
| Żel krzemionkowy | W eksykatorze | HF |
| H₂SO₄ | Gazy obojętne i kwasowe | Związki nienasycone, alkohole, substancje zasadowe |
Ile gramów 80% kwasu mrówkowego trzeba zważyć, aby uzyskać 200 g 20% roztworu tego kwasu?
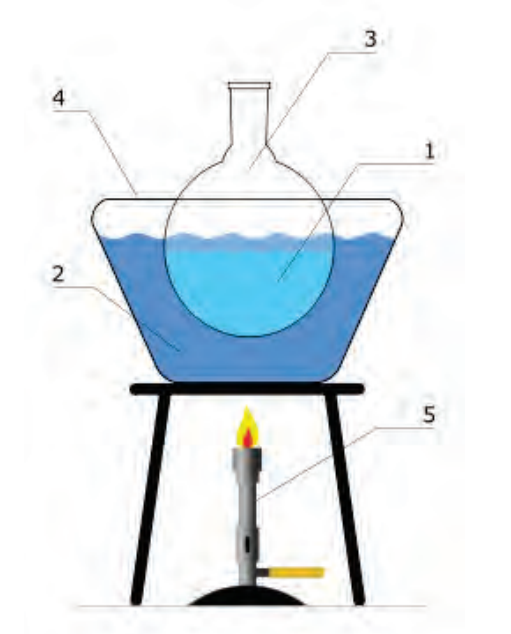
Przedstawiony na ilustracji zestaw służy do

W przypadku odczynnika, w którym nawet najczulsze techniki analizy chemicznej nie są w stanie wykryć zanieczyszczeń, a jego badanie wymaga zastosowania metod opartych na zjawiskach fizycznych, zalicza się on do kategorii czystości
Aby oszacować czystość MgCO3, poddano prażeniu próbkę o wadze 5 g tej soli aż do osiągnięcia stałej masy. W trakcie prażenia zachodzi reakcja:
MgCO3 → MgO + CO2 Całkowity ubytek masy wyniósł 2,38 g.
(Masy molowe reagentów to: MgCO3 – 84 g/mol, MgO – 40 g/mol, CO2 – 44 g/mol) Jaką czystość miała próbka węglanu magnezu?
Piktogram ukazujący czaszkę oraz skrzyżowane kości piszczelowe jest typowy dla substancji o działaniu
Oblicz, ile moli gazu można zebrać w pipecie gazowej o pojemności 500 cm3, jeśli gaz będzie gromadzony w warunkach normalnych. (W normalnych warunkach jeden mol gazu ma objętość 22,4 dm3)
Wody pobrane ze studni powinny być przewożone w szczelnie zamkniętych butelkach z przezroczystego materiału