Pytanie 1
Podczas wykonywania zdjęć wewnątrzustnych zębów górnych linia Campera powinna przebiegać w stosunku do płaszczyzny podłogi
Wynik: 37/40 punktów (92,5%)
Wymagane minimum: 20 punktów (50%)
Podczas wykonywania zdjęć wewnątrzustnych zębów górnych linia Campera powinna przebiegać w stosunku do płaszczyzny podłogi
W standardowym badaniu EEG elektrody P3, P4 i Pz umieszcza się na skórze głowy pacjenta nad płatami
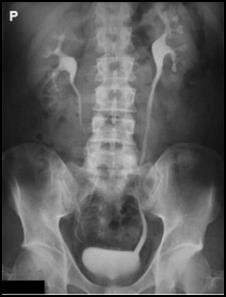
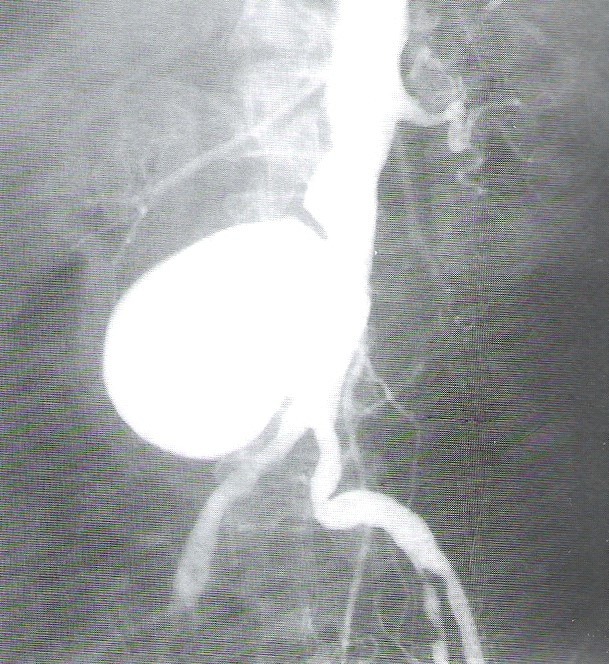
Zamieszczony rentgenogram został zarejestrowany podczas wykonania
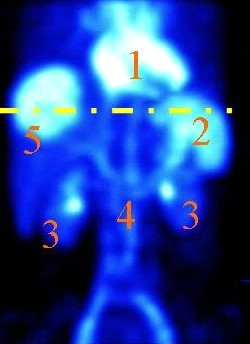
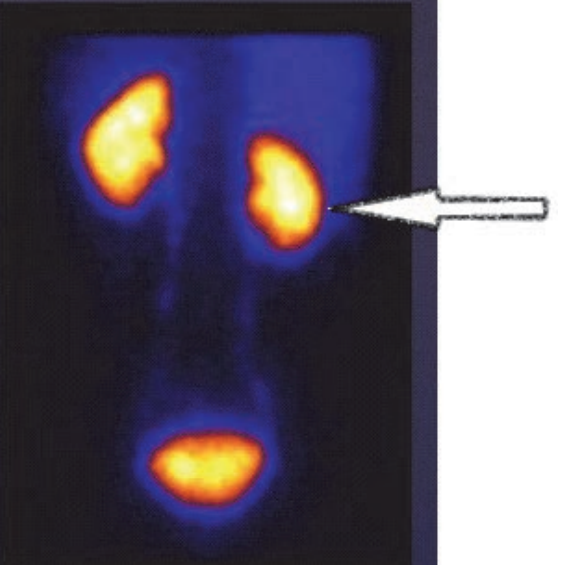
Który narząd na obrazie scyntygrafii znakowanej erytrocytami zaznaczono cyfrą 2?
W których projekcjach podstawowych wykonuje się standardowe badanie mammograficzne?
Parametr SNR w obrazowaniu MR oznacza
Które zdjęcie RTG stawu łokciowego zostało wykonane w projekcji skośnej w rotacji zewnętrznej?
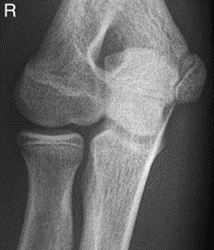
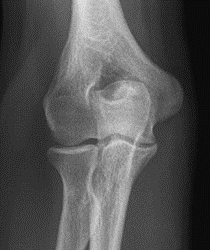
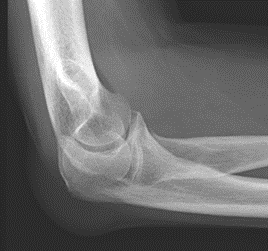
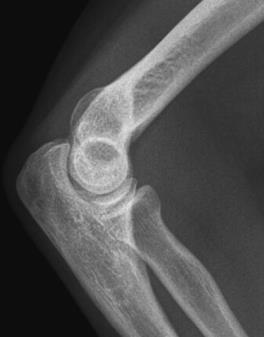
Na obrazie rentgenowskim strzałką zaznaczono
W zapisie EKG zespół QRS odzwierciedla
W obrazowaniu metodą rezonansu magnetycznego T1 oznacza czas
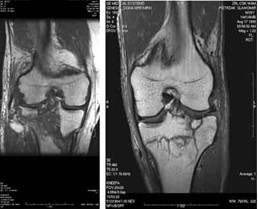
Którą metodą i w której płaszczyźnie zostało wykonane badanie stawu kolanowego zobrazowane na zdjęciach?
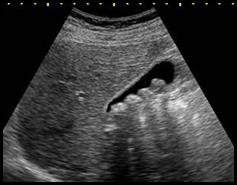
Którą strukturę anatomiczną uwidoczniono na zamieszczonym obrazie USG?
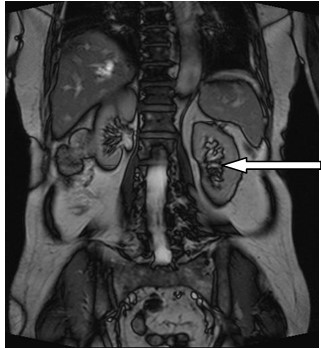
Który narząd został oznaczony strzałką na obrazie rezonansu magnetycznego?
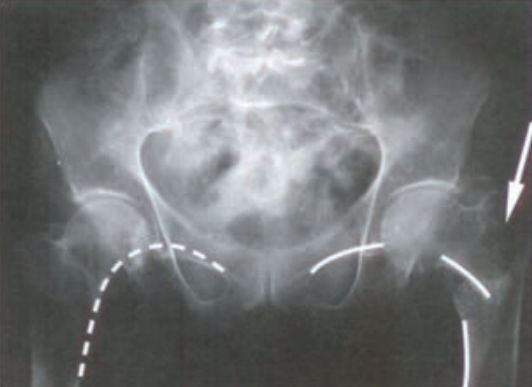
Podczas wykonywania zdjęcia rentgenowskiego lewobocznego czaszki promień centralny powinien przebiegać
W badaniu PET CT wykorzystuje się radioizotopy emitujące promieniowanie
Który materiał światłoczuły należy zastosować w rentgenodiagnostyce analogowej, by zminimalizować dawkę promieniowania jonizującego otrzymaną przez pacjenta?
W badaniu EEG elektrody referencyjne przymocowane do płatka ucha to
Radiogram przedstawia
W obrazowaniu MR wykorzystuje się moment magnetyczny
Jak określa się rekonstrukcję obrazów TK, której wynikiem są obrazy dwuwymiarowe tworzone w dowolnej płaszczyźnie przez wtórną obróbkę zestawionych ze sobą wielu przekrojów poprzecznych?
Na prawidłowo wykonanym zdjęciu zatok w projekcji PA górny zarys piramid rzutuje się
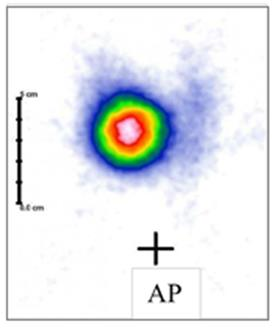
Na scyntygramie strzałką oznaczono
Brachyterapia polega na napromieniowaniu pacjenta promieniowaniem
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem
Bezwzględnym przeciwwskazaniem do wykonania badania rezonansem magnetycznym jest
Na scyntygramie tarczycy został uwidoczniony guzek
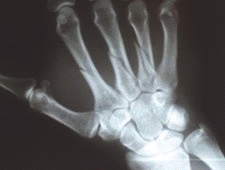
Na radiogramie uwidoczniono złamanie
Który system informatyczny służy do archiwizacji i transmisji obrazów radiologicznych?
Jakie wiązki promieniowania emituje medyczny akcelerator liniowy?
Wskazaniem do wykonania przesiewowego badania densytometrycznego jest
W radiologii stomatologicznej ząb o numerze 23 to kieł
W technice napromieniania SSD mierzona jest odległość źródła promieniowania
Warstwa półchłonna (WP) jest wyrażona w mm Cu dla
W badaniu EKG elektrodę przedsercową V4 należy umocować
Zgodnie ze standardami do wykonania zdjęcia bocznego czaszki, należy zastosować kasetę o wymiarze
Radioizotopowa terapia medycyny nuklearnej polega na wprowadzeniu do tkanek lub narządów radiofarmaceutyku
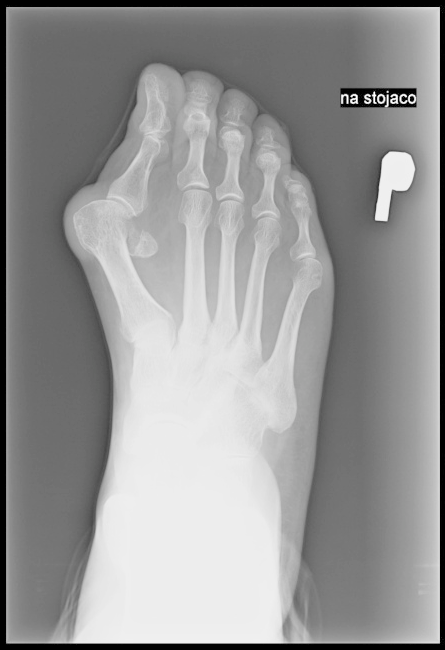
Na radiogramie uwidoczniono
Zgodnie z obowiązującą procedurą radiologiczną zdjęcie jamy brzusznej przy podejrzeniu zapalenia nerek zostanie wykonane w projekcji
Który radiofarmaceutyk może zostać podany pacjentowi w scyntygrafii perfuzyjnej mózgu?
Hałas podczas badania tomografii rezonansu magnetycznego jest efektem ubocznym pracy