Pytanie 1
Równanie przedstawia reakcję zachodzącą podczas oznaczania żelaza metodą miareczkowania
| 5Fe2+ + MnO4- + 8H+ ⇆ 5Fe3+ + Mn2+ + 4H2O |
Wynik: 28/40 punktów (70,0%)
Wymagane minimum: 20 punktów (50%)
Równanie przedstawia reakcję zachodzącą podczas oznaczania żelaza metodą miareczkowania
| 5Fe2+ + MnO4- + 8H+ ⇆ 5Fe3+ + Mn2+ + 4H2O |
Wzrost dyfuzyjny bakterii w hodowli płynnej przedstawia probówka oznaczona na rysunku jako

Próbkę tłuszczu poddano analizie, której wyniki zapisano w tabeli. Która substancja była zawarta w próbce?
| Odczynnik | Obserwacje |
|---|---|
| woda bromowa | odbarwienie wody bromowej |
Jakie urządzenie wykorzystuje się do hodowli bakterii w warunkach beztlenowych?
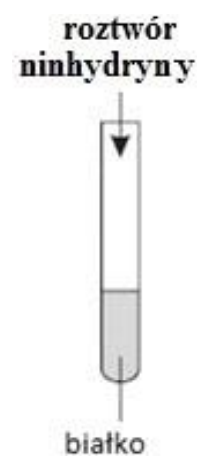
Na zamieszczonym schemacie trawienia białek cyfrą 1 oznaczono

Oznaczona twardość ogólna wody wynosi 2 mval/dm3. Wartość ta przeliczona na stopnie niemieckie, zgodnie z zamieszczonym przelicznikiem jednostek, wynosi
| 1 mval/dm3 – 2,8°dH (stopni niemieckich) |
Z opisu wynika, że do oznaczenia wapnia w glukonianie wapnia stosuje się miareczkowanie
| Opis oznaczania zawartości wapnia w glukonianie wapnia |
|---|
| Oznaczenie polega na strąceniu jonów wapnia szczawianem amonu w postaci szczawianu wapnia CaC2O4 zgodnie z równaniem reakcji: Ca2+ + C2O42- → CaC2O4. Odsączony osad CaC2O4 rozpuszcza się w kwasie siarkowym(VI) zgodnie z równaniem reakcji: CaC2O4 + 2H+ → H2C2O4 + Ca2+ Wydzielony kwas szczawiowy, w ilości równoważnej ilości wapnia w próbce, odmiareczkowuje się mianowanym roztworem KMnO4. |
W równaniu dotyczącym iloczynu rozpuszczalności siarczanu(VI) baru: Kso = [Ba2+][SO42-], jonowe stężenia Ba2+ oraz SO42- są przedstawione jako
Lepkość oleju napędowego w temperaturze 40°C wynosi 3 mm2/s. Jaką lepkość to określa?
Proces kondensacji i osuszania substancji termolabilnych, takich jak białka oraz kwasy nukleinowe, za pomocą suszenia zamrożonego materiału w obniżonym ciśnieniu poprzez sublimację lodu, określany jest jako
Po przeprowadzeniu analizy wagowej uzyskano 253 mg Mg2P2O7. Jaką ilość gramów magnezu zawierała zbadana próbka, jeśli współczynnik analityczny wynosi 0,2185?
Związek chemiczny, który posiada skrót Gly-Ala-Leu-Ala-Tyr i został zidentyfikowany w trakcie badań analitycznych, to
Jakie właściwości mierzą wiskozymetry?
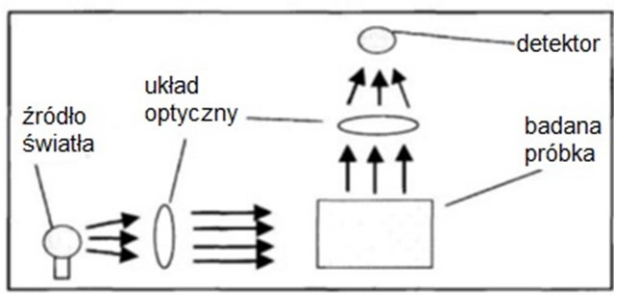
Na schemacie przedstawiono bieg promieni świetlnych
Sprzyja tworzeniu osadów grubokrystalicznych w czystszej formie oraz umożliwiających łatwiejsze sączenie
Który z kationów można wykryć przy użyciu metody płomieniowej?
Aby przygotować oznaczenia spektrofotometryczne kwasu acetylosalicylowego w zakresie nadfioletu, należy sporządzić cztery wzorce o objętości 50 cm3 każdy. Wzorce te powinny być stworzone poprzez odważenie kwasu salicylowego z dokładnością do 0,0001 g oraz rozpuszczenie odważonych ilości w 0,1000 mol/dm3 roztworze NaOH. Jaki sprzęt oraz w jakiej ilości, oprócz wagi analitycznej i łyżeczki, trzeba użyć do przygotowania tych wzorców?
W trakcie analizy przeprowadzonej metodą fotometrii płomieniowej próbkę nawozu o wadze 0,1000 g rozpuszczono w 250 cm3 wody destylowanej. Po wykonaniu badań uzyskano zawartość potasu równą 0,0830 mg/cm3. Jaką wartość procentową K2O ma badany nawóz i czy mieści się ona w normie, jeśli współczynnik przeliczeniowy K na K2O wynosi 1,205, a zawartość procentowa K2O w nawozie powinna być w zakresie 40-50%?
Jakie pH ma roztwór buforu węglanowego występującego we krwi, którego wartość wynosi 6,6, oraz jaki jest jego odczyn?
Który z kationów nadaje płomieniowi palnika barwę ceglastoczerwoną?
W trakcie zmiareczkowania próbki roztworu NaOH zużyto 15,0 cm3 roztworu HCl o stężeniu 0,1 mol/dm3. Ilość NaOH (M = 40 g/mol) w analizowanej próbce wyniosła
W trakcie mikrobiologicznych analiz żywności przed posiewem konieczne jest dokonanie rozcieńczenia próbki. W tym celu po dokładnym wymieszaniu badanego płynu pobiera się 10 cm3 za pomocą jałowej pipety, umieszcza w kolbie z 90 cm3 płynu rozcieńczającego i starannie miesza. Następnie z pierwszego rozcieńczenia przenosi się 1 cm3 do probówki, wzbogaconej o 9 cm3 płynu rozcieńczającego. W ten sposób uzyskuje się rozcieńczenie
Podczas reakcji ksantoproteinowej obecność białka jest potwierdzana przez zmianę koloru na żółty, co wskazuje na obecność w białku
Absorbancja barwnego roztworu o stężeniu 0,0004 mol/dm3, zmierzona w kuwecie o grubości 1 cm wynosi 0,30. Korzystając z zamieszczonego wzoru, oblicz wartość molowego współczynnika absorpcji £.
| A = ε · l · c |
| gdzie: |
| A – wartość absorbancji |
| ε – molowy współczynnik absorpcji; dm3/mol · cm |
| c – stężenie molowe roztworu; mol/dm3 |
| l – grubość kuwety; cm |
Zgodnie z zamieszczonym fragmentem metodyki postępowania analitycznego mineralizację próbki paszy należy przeprowadzić w kolbie
| Fragment metodyki postępowania analitycznego: |
| (...) Metoda służy do oznaczania zawartości białka w paszach na podstawie zawartości oznaczonego azotu. Próbka jest mineralizowana kwasem siarkowym(VI) w obecności katalizatora. Kwaśny roztwór jest alkalizowany za pomocą wodorotlenku sodu. Amoniak oddestylowany z zasadowego roztworu jest zbierany w znanej ilości roztworu kwasu siarkowego(VI), którego nadmiar jest z kolei miareczkowany roztworem wodorotlenku sodu. (...) |
W jakiej proporcji molowej EDTA reaguje z jonami Zn2+?
Badanie obecności pałeczek Salmonella w produktach spożywczych klasyfikuje się jako analiza
Aby wykryć obecność jonów SO42- w wodzie, należy zastosować roztwór
Jaką substancję stanowi płyn Lugola, używaną w mikrobiologii do barwienia preparatów według metody Grama?
Przeprowadzono doświadczenie zgodnie ze schematem.
Roztwór w probówce zabarwił się na kolor
Rozpraszanie promieniowania świetlnego przez cząstki koloidalne, które mają wymiary mniejsze od długości fali światła, to zjawisko
Jakie urządzenia są wykorzystywane do segregacji materiału na frakcje, które zawierają ziarna o różnych rozmiarach?
W przedstawionym na rysunku urządzeniu próbki są poddawane

Jakim odczynnikiem grupowym IV grupy analitycznej kationów jest?
Aby określić gęstość na podstawie siły wyporu działającej na pływak zanurzony w analizowanej cieczy, należy użyć
Piknometr umożliwia określenie
Na podstawie przeprowadzonych badań wiadomo, że dany odczynnik chemiczny ma czystość równą 99,998%. Jak się go oznacza?
Twardość ogólna badanej wody wynosi 2,5 mval/l. Wartość ta wyrażona w mg CaCO3/l wynosi
| Tabela. Jednostki twardości wody | |||||
| Jednostka twardości | mmol/l | mval/l | mg CaCO3/l | °f stopień francuski | °n stopień niemiecki |
|---|---|---|---|---|---|
| 1 mmol/l | 1 | 2 | 100 | 10 | 5,6 |
| 1 mval/l | 0,5 | 1 | 50 | 5,0 | 2,8 |
| 1 mg CaCO3/l | 0,01 | 0,02 | 1 | 0,1 | 0,056 |
| 1 stopień francuski (°f) | 0,1 | 0,2 | 10 | 1 | 0,56 |
| 1 stopień niemiecki (°n) | 0,178 | 0,357 | 17,8 | 1,78 | 1 |
Maksymalne dzienne przyjęcie (ADI) benzoesanu sodu wynosi 0,5 mg/kg wagi ciała. Ile maksymalnie benzoesanu sodu może dziennie spożywać osoba ważąca 70 kg?
Dla czterech różnych próbek gleb lekkich o odczynie kwaśnym oznaczono zawartość metali w mg/kg suchej masy. Wyniki zestawiono w tabeli:
Graniczne zawartości metali śladowych w powierzchniowej warstwie gleb bardzo lekkich | |||||
|---|---|---|---|---|---|
| Stopień zanieczyszczenia gleb | Zawartość metali w mg/kg suchej masy | ||||
| Pb | Cd | Zn | Cu | Ni | |
| 0 zawartość naturalna | 30 | 0,3 | 50 | 15 | 10 |
| 1 zawartość podwyższona | 70 | 1 | 100 | 30 | 30 |
| 2 słabe zanieczyszczenie | 100 | 2 | 300 | 50 | 50 |
| 3 średnie zanieczyszczenie | 500 | 3 | 700 | 150 | 100 |
| 4 silne zanieczyszczenie | 2500 | 5 | 3000 | 300 | 400 |
| 5 bardzo silne zanieczyszczenie | >2500 | >5 | >3000 | >300 | >400 |
| Metal | Próbka 1. | Próbka 2. | Próbka 3. | Próbka 4. |
|---|---|---|---|---|
| Pb | 180,0 | 15,0 | 25,0 | 29,0 |
| Cd | 1,6 | 0,3 | 0,2 | 0,6 |
| Zn | 40,0 | 55,5 | 48,0 | 37,0 |
| Cu | 328,0 | 25,0 | 8,0 | 56,0 |
| Ni | 135,0 | 8,0 | 8,0 | 19,0 |