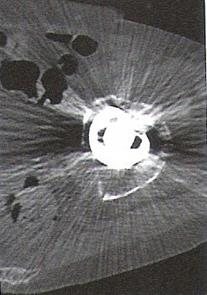
Pytanie 1
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
Wynik: 34/40 punktów (85,0%)
Wymagane minimum: 20 punktów (50%)
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
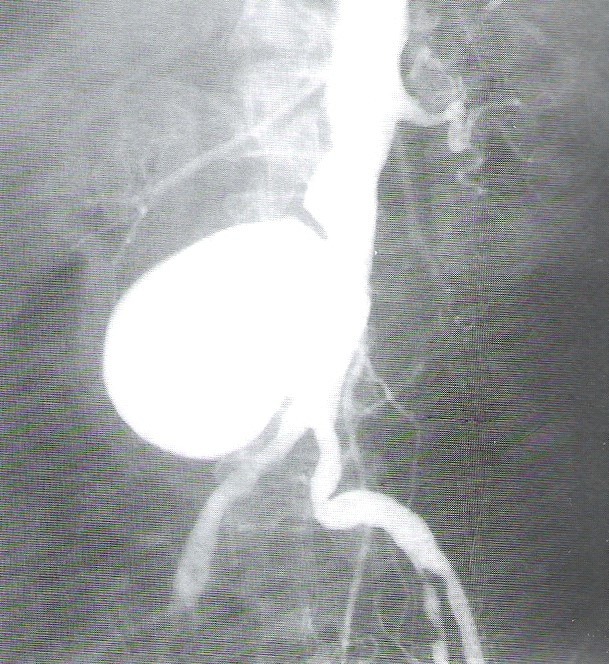
Celiakografia jest badaniem kontrastowym
W jakiej pozycji układa się pacjenta do standardowego badania MR kręgosłupa szyjnego?
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
Kasety do pośredniej radiografii cyfrowej CR są wyposażone
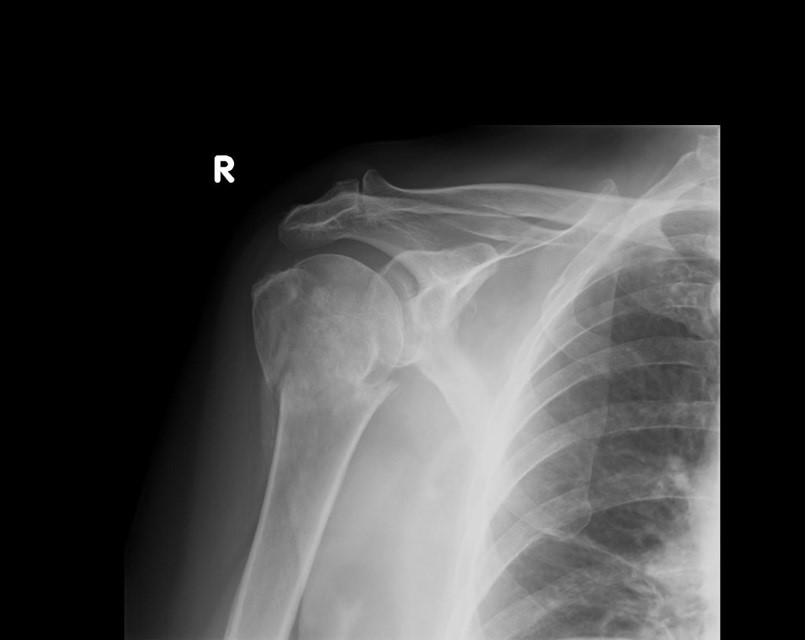
Na radiogramie uwidoczniono złamanie
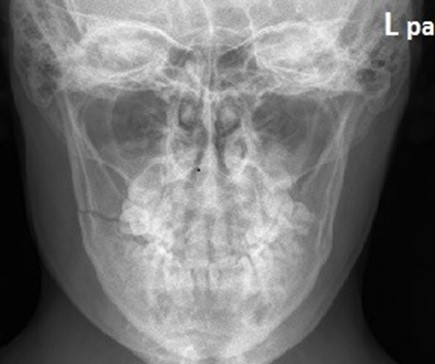
Na radiogramie żuchwy uwidoczniono złamanie w okolicy
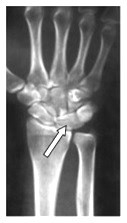
Na obrazie radiologicznym nadgarstka strzałką zaznaczona jest kość
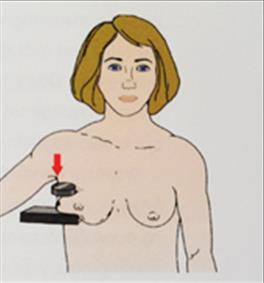
Ilustracja przedstawia pozycjonowanie pacjentki do badania mammograficznego w projekcji
W której technice obrazowania zostają zarejestrowane jednocześnie dwa przeciwbieżne kwanty promieniowania gamma o równej energii 511 keV?
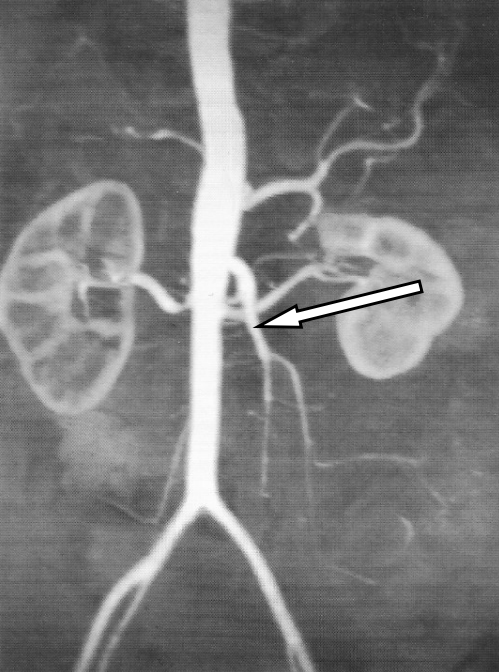
Którą tętnicę zaznaczono strzałką na obrazie MR?
Na zamieszczonym przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano

Wskaż osłonę radiologiczną, która jest stosowana w pracowniach radiodiagnostyki stomatologicznej.




Która właściwość promieniowania X pozwala na skierowanie promienia centralnego na wybrany punkt topograficzny podczas wykonywania badania radiologicznego?
Jaka jest standardowa odległość OF do wykonania rentgenowskich zdjęć kości i stawów kończyny górnej?
Głowica typu convex w USG służy do badania
Którą ochronę radiologiczną należy zastosować podczas wykonywania zdjęcia rentgenowskiego przeglądowego klatki piersiowej u pacjentki w okresie rozrodczym?
Zwiększenie napięcia na lampie rentgenowskiej powoduje
Osłony na gonady dla osób dorosłych powinny posiadać równoważnik osłabienia promieniowania nie mniejszy niż
Scyntygrafia kości „whole body” jest wskazana podczas diagnostyki
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
W obrazowaniu MR do uwidocznienia naczyń krwionośnych jest stosowana sekwencja
Parametrem krwi, który powinien zostać oznaczony u pacjenta przed wykonaniem badania MR z kontrastem jest
W jaki sposób należy ustawić promień centralny w stosunku do ramienia i przedramienia, by wykonać zdjęcie rentgenograficzne stawu łokciowego u pacjenta z przykurczem?
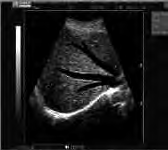
Na obrazie ultrasonograficznym jamy brzusznej uwidoczniono
W których projekcjach podstawowych wykonuje się standardowe badanie mammograficzne?
Którym skrótem oznacza się tomografię komputerową wysokiej rozdzielczości?
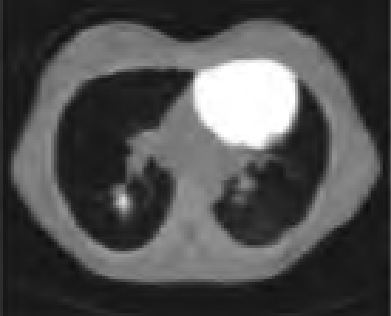
Na którym obrazie zarejestrowano badanie scyntygraficzne?
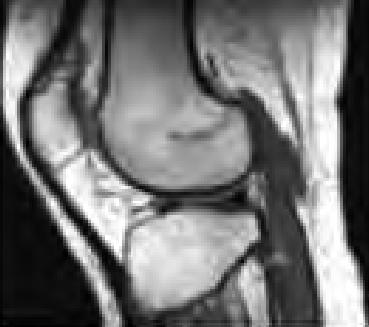
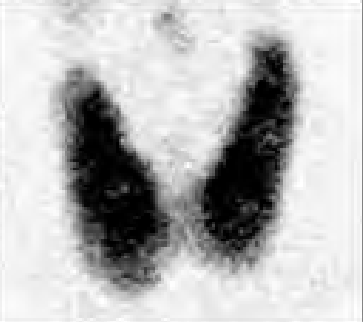
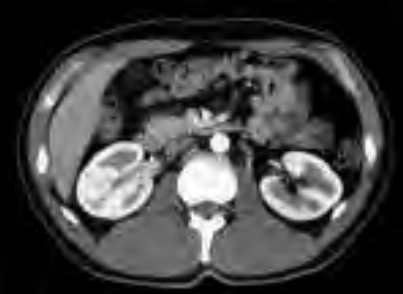
Którą metodą i w której płaszczyźnie zostało wykonane badanie stawu kolanowego zobrazowane na zdjęciach?
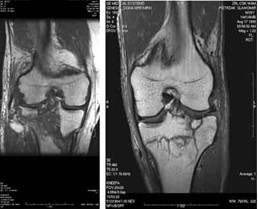
Na radiogramie stopy strzałką wskazano kość
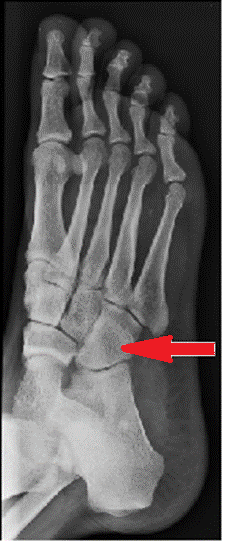
Na zamieszczonym rentgenogramie strzałką zaznaczono
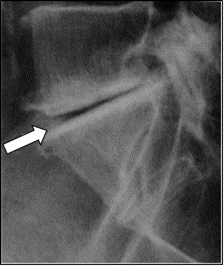
Na obrazie rentgenowskim strzałką zaznaczono
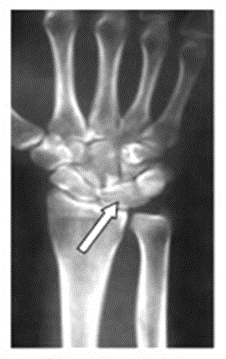
Na zamieszczonym obrazie radiologicznym nadgarstka strzałką wskazano kość
Który artefakt uwidoczniono na skanie RM głowy?
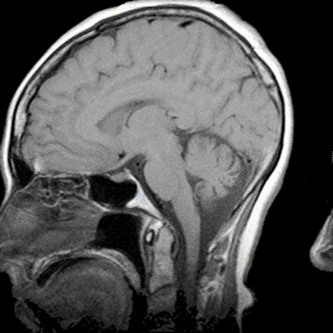
Badanie metodą Dopplera umożliwia
Na przedstawionym radiogramie TK głowy strzałką zaznaczono
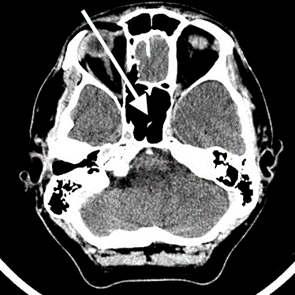
W jaki sposób należy ustawić promień centralny w stosunku do ramienia i przedramienia, by wykonać zdjęcie rentgenograficzne stawu łokciowego u pacjenta z przykurczem?
Na zamieszczonej rycinie przedstawiono
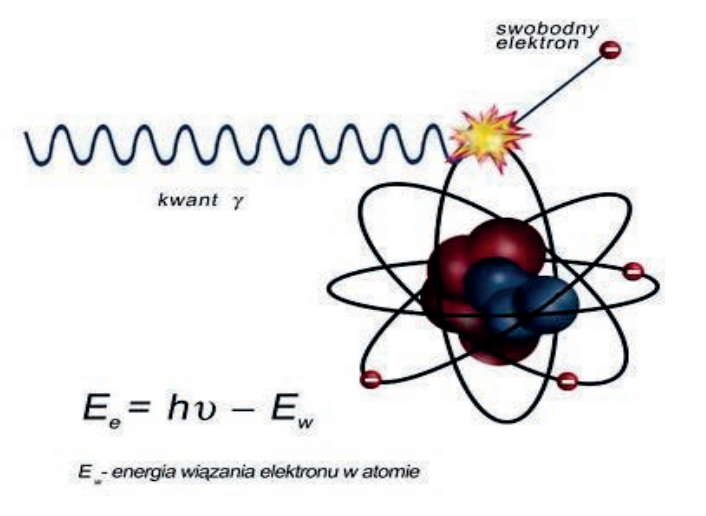
Elementem systemu rejestracji obrazu, w którym fotony promieniowania X są bezpośrednio konwertowane na sygnał elektryczny, jest
Zarejestrowany na obrazie TK artefakt jest spowodowany