Pytanie 1
pH wodnego roztworu gleby jest miarą kwasowości
Wynik: 29/40 punktów (72,5%)
Wymagane minimum: 20 punktów (50%)
pH wodnego roztworu gleby jest miarą kwasowości
Która z podanych metod analitycznych jest klasyfikowana jako technika łączona?
W analizie najczęściej oznacza się parametry CHZT i BZT
Jedną z kluczowych cech enzymów jest
Jak określane są enzymy, które katalizują przenoszenie różnych grup funkcyjnych?
Czym jest wskaźnik metalochromowy?
Wskaż urządzenia, które powinny być przygotowane do przeprowadzenia analizy jakościowej kationów?
Metody graficzne, pierwsza pochodna oraz Hahna znajdują zastosowanie w wyznaczaniu punktu końcowego miareczkowania?
Metoda obrączkowa jest wykorzystywana do rozpoznawania jonu
| Zawartość chlorowodoru w próbce można obliczyć wg wzoru: mB = CA · VA⁄1000 · pB⁄pA · MB w którym: mB – masa analizowanej substancji [g] CA – stężenie titranta [mol/dm3] VA – objętość titranta [cm3] pA i pB – współczynniki stechiometryczne reakcji, odpowiednio titranta i substancji oznaczanej MB – masa molowa substancji oznaczanej; 36,46 g/mol Do oznaczenia zużyto średnio 20,0 cm3 titranta, którego stężenie wynosiło 0,1000 mol/dm3. Obliczono masę próbki, która wyniosła 0,07292 g. |
| A. | HCl + NaOH → NaCl + H2O |
| B. | 3HCl + Al(OH)3 → AlCl3 + 3H2O |
| C. | 2HCl + Na2CO3 → 2NaCl + H2O + CO2 |
| D. | 2HCl + Na2B4O7 + 5H2O → 4H3BO3 + 2NaCl |
W próbce wody oznaczono zawartość rozpuszczonego tlenu metodą Winklera. Wyniki zestawiono w tabeli. Korzystając z zamieszczonego wzoru, określ zawartość rozpuszczonego tlenu (x) w badanej próbce wody.
$$ x = \frac{V_1 \cdot 0,2 \cdot 1000}{V_p} $$
\( x \) – zawartość tlenu rozpuszczonego; \( \text{mgO}_2/\text{dm}^3 \)
\( V_1 \) – objętość roztworu \( \text{Na}_2\text{S}_2\text{O}_3 \) o stężeniu \( 0,025 \, \text{mol}/\text{dm}^3 \) zużyta do miareczkowania; \( \text{cm}^3 \)
\( V_p \) – objętość próbki wody użytej do miareczkowania; \( \text{cm}^3 \)
\( 0,2 \) – ilość tlenu odpowiadająca \( 1 \, \text{cm}^3 \) roztworu \( \text{Na}_2\text{S}_2\text{O}_3 \) o stężeniu \( 0,025 \, \text{mol}/\text{dm}^3 \); \( \text{mg} \)
| Objętość próbki; \( V_p \) | Objętość roztworu \( \text{Na}_2\text{S}_2\text{O}_3 \) o stężeniu \( 0,025 \, \text{mol}/\text{dm}^3 \) zużyta do miareczkowania; \( V_1 \) |
| \( 100 \, \text{cm}^3 \) | \( 8,4 \, \text{cm}^3 \) |
W trakcie analizy przeprowadzonej metodą fotometrii płomieniowej próbkę nawozu o wadze 0,1000 g rozpuszczono w 250 cm3 wody destylowanej. Po wykonaniu badań uzyskano zawartość potasu równą 0,0830 mg/cm3. Jaką wartość procentową K2O ma badany nawóz i czy mieści się ona w normie, jeśli współczynnik przeliczeniowy K na K2O wynosi 1,205, a zawartość procentowa K2O w nawozie powinna być w zakresie 40-50%?
Podział anionów na grupy analityczne według Bunsena obejmuje ile grup?
Jaka była zawartość jonów żelaza (II) w oznaczanym roztworze, jeżeli na jego zmiareczkowanie zużyto \( 10 \, \text{cm}^3 \) roztworu \( \text{KMnO}_4 \) o stężeniu \( 0{,}02 \, \text{mol/dm}^3 \)?
Wzór do obliczeń:
$$ m_{Fe} = 5 \cdot c_{mol} \cdot V \cdot M_{Fe} $$
gdzie: \( V \) – objętość roztworu \( \text{KMnO}_4 \) zużyta w czasie miareczkowania [\( \text{dm}^3 \)], \( M_{Fe} = 56 \, \text{g/mol} \), \( c_{mol} \) – stężenie molowe roztworu \( \text{KMnO}_4 \) [\( \text{mol/dm}^3 \)]
Jakie kationy wchodzą w skład II grupy analitycznej?
W trakcie oznaczania węglanu sodu przy użyciu wodorotlenku sodu metodą Wardera warto miareczkować próbkę od razu przy umiarkowanym mieszaniu, ponieważ mogą się rozpuszczać cząsteczki CO2 z atmosfery, co skutkuje
Na jakich materiałach wykonuje się podłoża mikrobiologiczne?
Aby określić całkowitą zawartość żelaza w próbce wody, konieczne jest zredukowanie żelaza(III) do żelaza(II), a następnie wykorzystanie metody analitycznej, która nazywa się
Na schemacie przedstawiono bieg promieni świetlnych
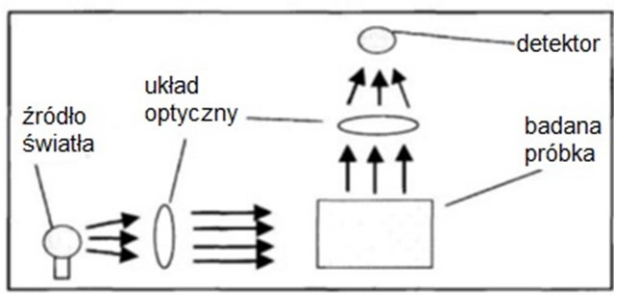
Przedstawiona na rysunku komora laminarna jest stosowana w laboratorium w celu bezpiecznego wykonywania prac

Sekcja analizy objętościowej dotycząca reakcji zobojętniania nosi nazwę
W trakcie mikrobiologicznych analiz żywności przed posiewem konieczne jest dokonanie rozcieńczenia próbki. W tym celu po dokładnym wymieszaniu badanego płynu pobiera się 10 cm3 za pomocą jałowej pipety, umieszcza w kolbie z 90 cm3 płynu rozcieńczającego i starannie miesza. Następnie z pierwszego rozcieńczenia przenosi się 1 cm3 do probówki, wzbogaconej o 9 cm3 płynu rozcieńczającego. W ten sposób uzyskuje się rozcieńczenie
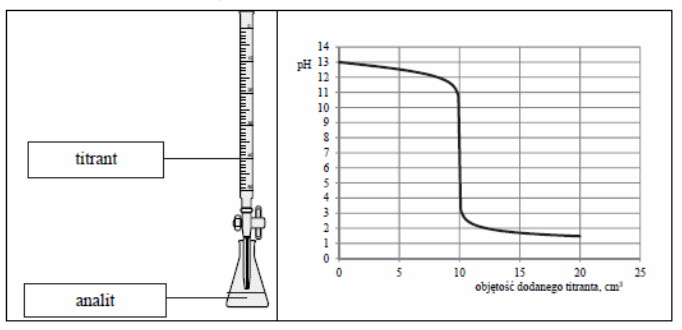
Na rysunku przedstawiono schemat układu do miareczkowania
O - elektroda odniesienia
W - elektroda wskaźnikowa
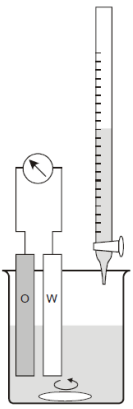
Eliminacja twardości wody w metodzie fizyko-chemicznej polega na użyciu
Na schemacie przedstawiającym sposób pobierania hodowli do badań ze skosu agarowego literą D oznaczono
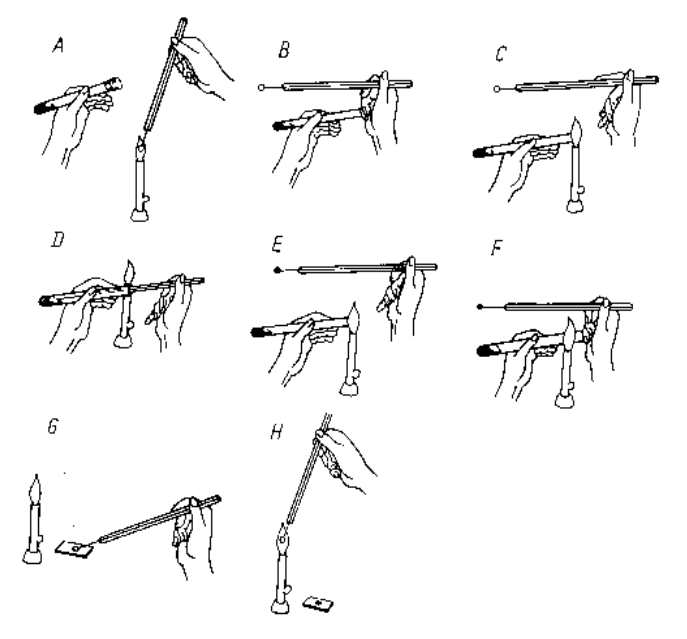
Jakie urządzenie wykorzystuje się do hodowli bakterii w warunkach beztlenowych?
Ebuliometr to przyrząd używany do pomiaru temperatury
Do kationów trzeciej grupy analitycznej, wytrącanych w formie siarczków roztworem AKT w środowisku amoniakalnym, należą:
| A. | Ni2+, Co2+, Fe2+, Fe3+, Mn2+, Zn2+ |
| B. | Mn2+, Cu2+, Cd2+, Cr3+, Ag+, Zn2+ |
| C. | Fe2+, Mg2+, Pb2+, Al3+, Ca2+ |
| D. | Ba2+, Ca2+, Sr2+ |
W naczyniu rozdzielającym umieszczono wodę oraz eter etylowy (d20 = 0,7138 g/cm3) i dokładnie je wymieszano.
Po chwili można zauważyć
Z opisu wynika, że do oznaczenia wapnia w glukonianie wapnia stosuje się miareczkowanie
| Opis oznaczania zawartości wapnia w glukonianie wapnia |
|---|
| Oznaczenie polega na strąceniu jonów wapnia szczawianem amonu w postaci szczawianu wapnia CaC2O4 zgodnie z równaniem reakcji: Ca2+ + C2O42- → CaC2O4. Odsączony osad CaC2O4 rozpuszcza się w kwasie siarkowym(VI) zgodnie z równaniem reakcji: CaC2O4 + 2H+ → H2C2O4 + Ca2+ Wydzielony kwas szczawiowy, w ilości równoważnej ilości wapnia w próbce, odmiareczkowuje się mianowanym roztworem KMnO4. |
Do osadów amorficznych serowatych zalicza się
Do zmiany objętości próbki roztworu NaOH wykorzystano 10,0 cm3 roztworu HCl o stężeniu 0,1000 mol/dm3. Jaką ilość NaOH (M = 40 g/mol) zawierała próbka?
Przedstawiony na rysunku zestaw jest stosowany podczas oznaczania
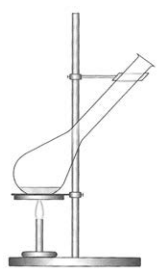
Karminowoczerwony kolor płomienia palnika w trakcie analiz chemicznych sugeruje obecność w roztworze jonów
Glebę uprawną o pHKCl = 6,7 należy zakwalifikować jako
| Podział gleb uprawnych i leśnych w zależności od odczynu, wykazywanego w wyniku działania na glebę roztworu KCl (pHKCl) | |||
|---|---|---|---|
| pHKCl | Gleby uprawne | pHKCl | Gleby leśne |
| <4,0 | Bardzo kwaśne | <3,5 | Bardzo silnie kwaśne |
| 4,1 – 4,5 | Kwaśne | 3,6 – 4,5 | Silnie kwaśne |
| 4,6 – 5,0 | Średnio kwaśne | 4,6 – 5,5 | Kwaśne |
| 5,1 – 6,0 | Słabo kwaśne | 5,6 – 6,5 | Słabo kwaśne |
| 6,1 – 6,5 | Obojętne | 6,6 – 7,2 | Obojętne |
| 6,6 – 7,0 | Słabo alkaliczne | 7,3 – 8,0 | Słabo alkaliczne |
| 7,1 – 7,5 | Średnio alkaliczne | >8,0 | Alkaliczne |
| >7,5 | Alkaliczne | ||
Które równanie przedstawia reakcję wytrącania osadu?
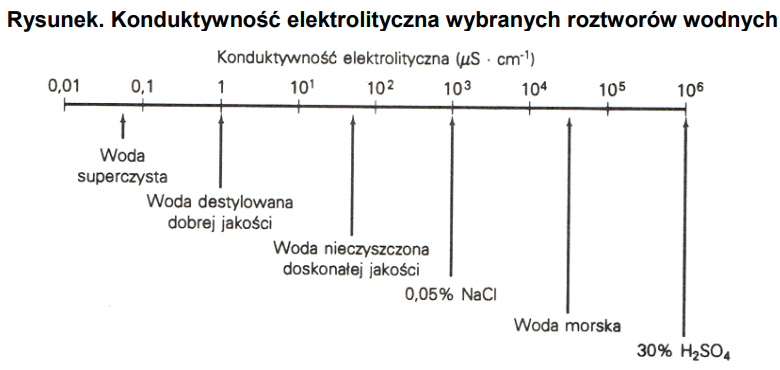
Konduktywność elektrolityczna wody destylowanej stosowanej w laboratorium chemicznym wynosi 0,001 mS cm-1. Z analizy danych przedstawionych na rysunku wynika, że woda ta jest
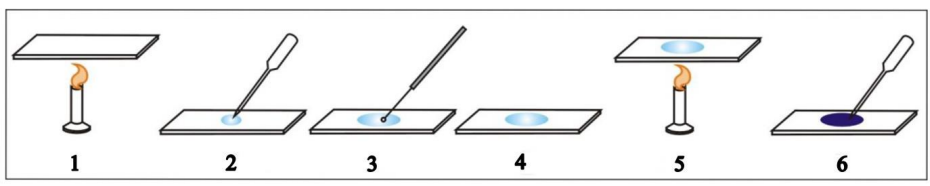
Na ilustracji przedstawiono poszczególne etapy wykonania preparatu mikroskopowego utrwalonego. Cyfrą 3 oznaczono
Na zmiareczkowanie 10 cm3 roztworu KOH zużyto 10 cm3 0,1000-molowego roztworu H2SO4. Oblicz ilość KOH w badanej próbce w g/100 cm3.
| MK = 39 g/mol, MO = 16 g/mol, MH = 1 g/mol, MS = 32 g/mol |
Który zbiór zawiera jedynie odczynniki grupowe używane w analizie jakościowej jonów?